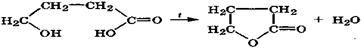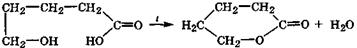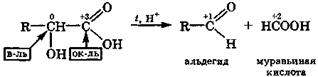Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Некоторые биогенные гидроксикарбоновые кислоты и их кислотные свойстваСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Примечание. Звездочкой отмечены хиральные центры, т. е. асимметрические углеродные атомы.
По взаимному расположению функциональных групп гидроксикислоты подразделяются на α-, β-, γ-кислоты и т. д:
СН3—СН2—СНСООН СН3—СН—СН2СООН СН2—СН2—СН2СООН ОН ОН ОН α -гидроксимасляная β-гидроксимасляная γ-гидроксимасляная кислота кислота кислота
Многие гидроксикислоты, например молочная, яблочная, винная, изолимонная, имеют в молекуле хиральные центры, вследствие чего для них характерна оптическая изомерия. Так, молочная кислота существует в трех формах: две оптически активные, т. е. энантиомеры (зеркальные изомеры), а третья - оптическая неактивная, являющаяся рацемической смесью энантиомеров. Молочная кислота, выделенная из мышечной ткани, называемая мясо-молочной кислотой, является L-энантиомером. D-Молочная кислота образуется из сахаров при помощи особых бактерий-возбудителей брожения. Под действием молочнокислых бактерий в прокисшем молоке, при созревании сыров, при квашении овощей и в процессе силосования образующаяся молочная кислота является рацемической смесью обоих энантиомеров и не проявляет оптической активности:
D-молочная L-молочная кислота кислота
D,L – молочная кислота (D,L-рацемат)
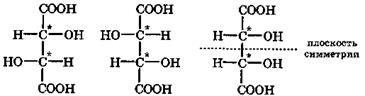
D-винная L-винная мезовинная кислота
виноградная кислота (D,L-рацемат)
Яблочная кислота подобно молочной также существует в трех формах: D-энантиомер, L-энантиомер и их D, L-рацемат. Молекула винной кислоты содержит два одинаковых хиральных центра, между которыми может проходить плоскость симметрии этой молекулы. Поэтому винная кислота в природе существует в четырех формах: D-винная, L-винная, D,L-рацемат, называемый виноградной кислотой, а также мезовинная кислота, являющаяся оптически неактивным стереоизомером вследствие внутримолекулярной компенсации из-за симметричности ее структуры. Оптические изомеры гидроксикислот отличаются не только физическими свойствами, но и тем, что их биологические и физиологические функции различны. В организме обычно присутствует один стереоизомер гидроксикислоты. Среди специфических свойств гидроксикислот прежде всего следует отметить их склонность к реакции дегидратации при нагревании. При этом дегидратация для α-, β- и γ-гидроксикислот происходит различно.
α-Гидроксикислоты дегидратируются межмолекулярно, при этом спиртовые группы взаимодействующих молекул взаимно ацилируются карбоксильными группами этих кислот с образованием устойчивых циклических сложных эфиров, называемых лактидами (от латинского названия молочной кислоты):
лактид
В этой электрофильно-нуклеофильной реакции каждая молекула за счет спиртовой группы выступает нуклеофилом, а за счет карбоксильной группы - электрофилом. Лактиды, как и сложные эфиры, при кипячении с водой в присутствии кислот или щелочей гидролизуются с образованием исходных кислот.
β-Гидроксикислоты при нагревании дегидратируются внутримолекулярно за счет протона α-метиленовой группы, имеющего повышенную подвижность, образуя α,β -непредельные кислоты: Эта реакция сопровождается внутримолекулярной окислительно-восстановительной дисмутацией за счет углеродных атомов. Подобные реакции дегидратации протекают в организме при участии дегидратаз. Они имеют место при β-окислении жирных кислот и дегидратации лимонной кислоты в цикле Кребса.
γ- и δ-Гидроксикислоты, вследствие пространственной близости —ОН и СООН-групп, очень неустойчивы и легко отщепляют молекулу воды вследствие внутримолекулярного ацилирования спиртовой группы с образованием устойчивых пяти- и шестичленных циклических внутренних сложных эфиров - лактонов: γ-гидроксимасляная γ-бутиролактон кислота
δ-гидроксивалериановая δ-валеролактон кислота Наличие в гидроксикислотах двух или более электроотрицательных групп способствует реакциям окислительно-восстановительной дисмутации, так как в их молекулах увеличивается число углеродных атомов, имеющих промежуточные степени окисления. Внутримолекулярная окислительно-восстановительная дисмутация α-гидроксикис- лот происходит при их нагревании в присутствии H2SО4 и сопровождается разрывом связи С—С. При этом образуются муравьиная кислота и соответствующее карбонильное производное — альдегид или кетон:
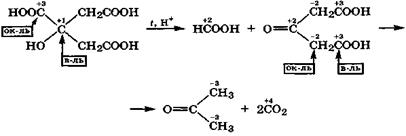
Лимонная кислота в этих условиях, наряду с муравьиной кислотой, образует ацетондикарбоновую кислоту, которая в результате внутримолекулярной окислительно-восстановитель
ной дисмутации легко декарбоксилируется с образованием ацетона: Приведенные реакции еще раз демонстрируют, что углеродный атом карбоксильной группы может быть и окислителем (первая реакция), и восстановителем (вторая реакция). В организме гидроксикислоты дегидрируются под действием дегидрогеназ с окисленной формой кофермента НАД+, причем водородные атомы отщепляются от спиртовой группы и связанного с ней углеродного атома. При этом образуются соответствующие оксокислоты.
Так, важной стадией β-окисления жирных кислот является дегидрирование β-гидроксикислот в виде производных с коферментом А в соответствующие производные β-оксокислот. Подобная реакция межмолекулярной окислительно-восстановительной дисмутации протекает с изолимонной кислотой в цикле Кребса:
Таким образом, гидроксикислоты чрезвычайно склонны к реакциям окислительно-восстановительной дисмутации, протекающей как внутримолекулярно, так и межмолекулярно.
Оксокарбоновые кислоты Оксокарбоновыми кислотами называют соединения, содержащие одновременно карбоксильную и карбонильную группы. Они подразделяются на альдегидо- и кетонокислоты. Наиболее часто встречающиеся в живых системах оксокарбоновые кислоты приведены в табл. 18. Таблица 18
|
|||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-10; просмотров: 988; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.248 (0.008 с.) |

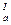 =3,5
рК
=3,5
рК 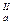 =5,0
=5,0
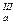 =6,4
=6,4
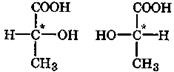
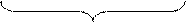
 кислота кислота (оптически неактивная)
кислота кислота (оптически неактивная)