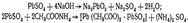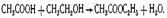Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Обнаружение уксусной кислотыСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Реакция с хлоридом железа (III). От прибавления хлорида железа (III) к ацетат-ионам появляется красная окраска, обусловленная образованием основного ацетата железа:
Реакция с нитратом лантана и иодом. При взаимодействии ацетат-ионов с нитратом лантана La(NO 3) 3 в присутствии иода и аммиака раствор приобретает темно-синюю окраску или выпадает такого же цвета осадок. Реакция образования индиго. При нагревании уксусной кислоты или ацетатов с солями кальция образуется ацетон:
Образовавшийся ацетон в присутствии щелочей взаимодействует с о -нитробензальдегидом. При этом образуется ряд промежуточных продуктов. Конечным продуктом реакции является индиго. Реакция образования уксусно-этилового эфира. При нагревании ацетатов с этиловым спиртом в присутствии серной кислоты образуется уксусно-этиловый эфир (этилацетат):
СИНИЛЬНАЯ КИСЛОТА Синильная кислота (цианистоводородная кислота) — газ или бесцветная жидкость (г. кип. 25,6 °С, т. пл.— 13,3 °С, плотность 0,699), имеет запах горького миндаля, легко смешивается с водой и с рядом органических растворителей. При — 13,3 °С синильная кислота затвердевает, образуя волокнистую кристаллическую массу. Синильная кислота угнетает внутриклеточные железосодержащие дыхательные ферменты. При угнетении цитохромоксидазы синильной кислотой клетки организма не усваивают кислород, поступающий с кровью. В результате этого наступает клеточное кислородное голодание, несмотря на то, что кровь насыщенна кислородом. Цианиды также могут блокировать гемоглобин крови, нарушая его функции. Метаболизм. Метаболитом синильной кислоты является тиоцианат (роданид), который образуется в организме при конъюгации цианидов с серой под влиянием фермента роданазы. Обнаружение синильной кислоты и цианидов Изолирование синильной кислоты и цианидов из биологического материала производят перегонкой с водяным паром. Для этой цели собирают 3—5 мл первого дистиллята в пробирку, содержащую 2 мл 2 %-го раствора гидроксида натрия. Поскольку синильная кислота быстро разлагается в организме, исследование биологического материала на наличие этой кислоты и ее солей желательно проводить сразу же после вскрытия трупов. При отравлении синильной кислотой и цианидами на химико-токсикологическое исследование берут желудок с содержимым, печень и почки. Ввиду быстрого разложения синильной кислоты и цианидов в тканях организма эти яды можно обнаружить в содержимом желудка и не обнаружить в паренхиматозных органах.
Реакция образования берлинской лазури. От прибавления сульфата железа (II) к щелочному раствору цианидов, образуется цианид железа (II), который при взаимодействии с избытком цианидов, а затем с сульфатом или хлоридом железа (III) образует берлинскую лазурь:
Реакция образования роданида железа. При нагревании цианидов с раствором полисульфида аммония образуется роданид, от прибавления к которому раствора хлорида железа (Ш) появляется кроваво-красная окраска:
Реакция образования бензидиновой сини. Соли меди (II) с цианидами образуют дициан (CN) 2, при взаимодействии которого с водой выделяется кислород, окисляющий бензидин. Продуктом окисления бензидина является бензидиновая синь:
Реакция с пикриновой кислотой. От прибавления пикриновой кислоты и щелочи к цианидам образуется соль изопурпуровой кислоты, имеющая красную окраску:
Серная кислота. Изолирование: Подлежащие исследованию органы трупов измельчают, заливают водой до получения кашицеобразной массы, которую оставляют на 1—2 ч. Полученную вытяжку отфильтровывают, подвергают диализу, а затем из диализата отгоняют серную кислоту. При исследовании серной кислоты на одежде или на других объектах эту кислоту можно извлечь этиловым спиртом, в котором растворяется эта кислота и не растворяются ее соли. С этой целью исследуемый материал измельчают и прибавляют к нему этиловый спирт. Через некоторое время жидкость отфильтровывают от твердых частиц исследуемого материала. Фильтрат на водяной бане выпаривают досуха. К сухому остатку прибавляют 10 мл воды, кипятят несколько минут, а затем охлаждают жидкость до комнатной температуры. Из полученной жидкости отгоняют серную кислоту и исследуют ее в дистилляте. Качественное обнаружение: 1.Способность обугливать углеводы. 2.Реакция с хлоридом бария. К дистилляту прибавляют раствор хлорида бария. Появление белого осадка сульфата бария указывает на наличие серной кислоты. 3.Отгонка серной кислоты. К диализатам прибавляют медные опилки и нагревают. При этом образуется ангидрид сернистой кислоты SO 2, который отгоняют и собирают в приемник, содержащий раствор иода. При взаимодействии ангидрида сернистой кислоты с водой и иодом образуется серная кислота: Способ отгонки серной кислоты состоит в следующем: в колбу аппарата для отгонки жидкостей, состоящего из колбы, холодильника с форштосом и приемника, вносят диализат и медные опилки. Конец форштоса опускают в приемник, содержащий раствор иода. Колбу устанавливают на масляную или песочную баню и нагревают. Если во время перегонки происходит быстрое обесцвечивание иода, то его раствор небольшими порциями дополнительно вносят в приемник. После окончания отгонки серной кислоты в приемник прибавляют 2—3 мл разбавленной соляной кислоты и нагревают жидкость до полного исчезновения иода, не вступившего в реакцию с ангидридом сернистой кислоты. Освобожденный от иода дистиллят используют для обнаружения в нем серной кислоты. 4.Реакция с ацетатом свинца. К нескольким каплям дистиллята раствор ацетата свинца. При наличии серной кислоты выпадает белый осадок сульфата свинца, который не растворяется в азотной кислоте, но растворяется в едких щелочах и в растворе ацетата аммония при нагревании: 4.Реакция с родизонатом натрия основана на том, что родизо-нат натрия с солями бария образует родизонат бария, имеющий красную окраску. От прибавления серной кислоты или сульфатов к родизонату бария он разлагается. При этом образуется осадок сульфата бария и исчезает красная окраска родизоната:
Количественое определение:Аликводу водного извлечения титруют 0.1н раствором едкого натра в присутствии метилового оранжевого.Затем в определенной части извлечения определяют количество сульфатов весовым методом. Найденный количества серной кислоты сопоставляют. Азотная кислота Изолирование: Для выделения азотной кислоты из органов и тканей трупов их измельчают, заливают дистиллированной водой. Полученную смесь настаивают в течение 1—2 ч, затем отфильтровывают вытяжку, которую подвергают диализу. При наличии азотной кислоты полученный диализат должен иметь кислую реакцию и давать положительные реакции на нитрат-ионы. Качественное определение: 1.Свободная азотная кислота фиксируется белками, окрашивая их в желтый цвет. 2.Реакция с дифениламином основана на окислении дифениламина азотной кислотой. При этом вначале образуется бесцветный дифенилбензидин, который при дальнейшем окислении превращается в соединение, имеющее синюю окраску. 3.Отгонка азотной кислоты из диализатов. Азотная кислота сразу не перегоняется из разбавленных растворов. Вначале отгоняется вода, а под конец отгоняется и азотная кислота. Поэтому диализаты, содержащие азотную кислоту, отгоняют почти досуха. Прибавление медных опилок к диализатам способствует перегонке азотной кислоты. При взаимодействии азотной кислоты с медными опилками образуется оксид азота (II), который кислородом воздуха окисляется до оксида азота (IV). Оксид азота (IV) в приемнике реагирует с водой. В результате этого образуется смесь азотной и азотистой кислот: 4.Реакция с бруцином. На часовое стекло или капельную пластинку наносят несколько капель дистиллята и прибавляют 2— 3 капли 0,02 %-го свежеприготовленного раствора бруцина в концентрированной серной кислоте. При наличии азотной кислоты в исследуемом растворе появляется красная окраска. Такую же окраску с бруцином дают нитриты, перхлораты и некоторые другие окислители. Соляная кислота Изолирование:При исследовании биологического материала на наличие соляной кислоты исследуемые объекты измельчают, заливают дистиллированной водой, настаивают 1—2 ч и фильтруют, полученный фильтрат подвергают диализу. Качественное определение: 1.Реакция с нитратом серебра. К дистилляту прибавляют раствор нитрата серебра и разбавленную азотную кислоту. Появление белого осадка хлорида серебра, растворимого в аммиаке, указывает на наличие соляной кислоты в дистилляте. 2.Часть водного извлечения помещают в колбу, соединенную с нисходящим холодильником и приемником. Колбу нагревают(лучше на водяной бане). Вначале отгоняется вода; затем при повышении содержания хлористого водорода до 10% последний начинает перегонятся, поэтому жидкость должна быть выпарена по возможности вся.Дистиллят исследуют на наличие хлористого водорода. 3.Реакция с хлоратом калия. К 1 мл дистиллята прибавляют несколько кристалликов хлората калия (КСlО 3) и нагревают. При наличии соляной кислоты в дистилляте выделяется свободный хлор, который можно обнаружить по посинению иод-крахмальной бумажки:
Количественное определение: Определенную часть водного извлечения подвергают перегонки выпаривая содержимое колбы,как описано выше, досуха. В дистилляте определяют количество хлористого водорода титрованием по Фольгарду или весовым путем, взвешивая хлорид серебра. Гидроксид нартрия Изолирование: Исследуемые объекты измельчают, заливают дистиллированной водой и настаивают 2—3 ч. Затем смесь воды и измельченного объекта фильтруют. К фильтрату прибавляют 2—3 капли спиртового раствора фенолфталеина. Появление розовой или красной окраски указывает на наличие едких щелочей или карбонатов щелочных металлов в вытяжках. После этого исследуют вытяжки на наличие карбонатов щелочных металлов (реакция с хлоридом бария) и на присутствие в них катионов калия, натрия. Качественное определение: 1.Реакция с гидроксостибиатом калия.Этот реактив в нейтральной или слабощелочной среде с ионами натрия дает белый кристаллический осадок Na[Sb(OH) 6 ]. 2.Реакция с цинк-уранилацетатом. Уранилацетат UO 2 (СН 3 СОО) 2 в нейтральных или уксусно-кислых растворах с солями натрия дает зеленовато-желтый кристаллический осадок NaUO 2 (CH 3 COO) 3.
Гидроксид калия Изолирование: Исследуемые объекты измельчают, заливают дистиллированной водой и настаивают 2—3 ч. Затем смесь воды и измельченного объекта фильтруют. К фильтрату прибавляют 2—3 капли спиртового раствора фенолфталеина. Появление розовой или красной окраски указывает на наличие едких щелочей или карбонатов щелочных металлов в вытяжках. После этого исследуют вытяжки на наличие карбонатов щелочных металлов (реакция с хлоридом бария) и на присутствие в них катионов калия, натрия.
Качественное определение: 1.Реакция с гидротартратом натрия. Гидротартрат натрия в нейтральных или уксусно-кислых растворах с ионами калия дает белый кристаллический осадок КНС4Н4О6. Этот осадок растворяется в горячей воде, минеральных кислотах и щелочах.
2.Реакция с кобальтинитритом натрия. Кобальтинитрит натрия Na 3 [Co(NO 2) 6 ] из нейтральных или слабокислых растворов осаждает ионы калия в виде желтого кристаллического осадка K 2 Na[Co(NO 2) 6 ].
Аммиак
Изолирование: Исследуемые объекты измельчают, заливают дистиллированной водой и настаивают 2—3 ч. Затем смесь воды и измельченного объекта фильтруют. К фильтрату прибавляют 2—3 капли спиртового раствора фенолфталеина. Появление розовой или красной окраски указывает на наличие едких щелочей или карбонатов щелочных металлов в вытяжках. После этого исследуют вытяжки на наличие карбонатов щелочных металлов (реакция с хлоридом бария) и на присутствие в них катионов калия, натрия. Обнаружение аммиака в биологическом материале не всегда позволяет сделать вывод об отравлении этим препаратом. Это объясняется тем, что при гниении органов трупов и других объектов биологического происхождения всегда образуются определенные количества аммиака. Кроме аммиака при гниении биологического материала образуется сероводород и ряд других веществ. Поэтому прежде чем приступить к исследованию водных вытяжек из биологического материала или диализатов на наличие аммиака, химик-эксперт должен проверить эти жидкости на присутствие сероводорода как одного из продуктов гниения белковых веществ. Обнаружение сероводорода в вытяжках из биологического материала указывает на протекание процессов гниения исследуемых объектов, в результате чего образуется как сероводород, так и аммиак. Поэтому при наличии сероводорода в биологическом материале эти объекты на присутствие аммиака не исследуют. На присутствие аммиака подвергают анализу только те органы трупов, которые не подверглись гнилостным изменениям и не содержат сероводорода. Качественное определение: 1.Обнаружение сероводорода. 3—5 мл вытяжки из биологического материала или диализата вносят в колбу вместимостью 50 мл, в которую прибавляют 10 %-й раствор соляной кислоты до кислой реакции на лакмус. Колбу сразу же закрывают пробкой, в прорезы на нижней поверхности которой вставлена полоска фильтровальной бумаги, смоченная раствором ацетата свинца. При наличии сероводорода образуется сульфид свинца, в результате чего бумага чернеет. 2.Реакция с сульфатом меди и лакмусом. В колбу вместимостью 50 мл вносят 10—15 мл водной вытяжки из биологического материала или диализата. Колбу закрывают пробкой, на нижней поверхности которой в прорезы вставляют две индикаторные бумажки (влажная красная лакмусовая бумажка и бумажка, смоченная раствором сульфата меди). Посинение лакмусовой бумажки и бумажки, смоченной раствором сульфата меди (образуется [Cu(NH 3) 4 ]SO 4), указывает на наличие аммиака в вытяжке из биологического материала. 3.Реакция с реактивом Несслера. От прибавления реактива Несслера к диализату или щелочной водной вытяжке из биологического материала, содержащей аммиак, выпадает осадок иодида дииододимеркураммония: Нитриты Изолирование: Для выделения нитритов из биологического материала применяют метод настаивания исследуемых объектов с водой, который используется для выделения минеральных кислот и щелочей. Водные вытяжки, полученные при настаивании биологического материала с водой, фильтруют. Полученные фильтраты подвергают диализу. Диализаты доводят до нейтральной реакции, а затем определяют наличие нитритов при помощи реакций Качественное определение: 1.Реакция с сульфаниловой кислотой и β-нафтолом. После подкисления диализатов, содержащих нитриты, выделяется азотистая кислота HNO 2, которая с сульфаниловой кислотой (I) или с другими первичными ароматическими аминами образует соль диазония (II): При сочетании полученной соли диазония с β-нафтолом (III) в щелочной среде образуется азокраситель (IV): 2.Реакция с реактивом Грисса. Этот реактив состоит из суль-фаниловой кислоты и α-нафтиламина. При взаимодействии реактива Грисса с нитритами образуется азокраситель: 3.Обнаружение нитритов с помощью иод-крахмальной бумажки. На иод-крахмальную бумажку наносят каплю 1 %-го раствора соляной кислоты и 3—4 капли нейтрализованного дистиллята. При наличии нитритов в дистилляте иод-крахмальная бумажка синеет. Количественное опеределение Колориметрический метод. Пестициды Метафос
Метафос (метилпаратион, вофатокс, метацид, фолидол) —0,0-диметил-0-(4-нитро-фенил) -тиофосфат — является ядохимикатом, принадлежащим к органическим соединениям фосфора (производным тиофосфорной кислоты). Метафос — белое кристаллическое вещество (т. пл. 35— 36 °С). Слабо растворяется в воде (при 25°С в 1 л воды растворяется 55 мг препарата) и парафиновых углеводородах, хорошо растворяется в большинстве других органических растворителей. При гидролизе метафоса в воде образуется n -нитрофенол и диметилтиофосфорная кислота. В щелочной среде скорость гидролиза метафоса увеличивается. В растениях он гидролизуется быстрее, чем в воде. При нагревании до 140—160 °С метафос почти полностью превращается в тиоловый изомер: Изолирование: В колбу вместимостью 500 мл вносят 100 г мелкоизмельченного биологического материала, прибавляют воду до получения кащицеобразной массы и 100 мл хлороформа. Содержимое колбы оставляют на 4 ч при частом взбалтывании. Затем отделяют хлороформную вытяжку, а биологический материал еще 2 раза настаивают с хлороформом (порциями по 50 мл) в течение 2 ч при частом взбалтывании. Хлороформные вытяжки соединяют, фильтруют и выпаривают досуха. Сухой остаток растворяют в 10 мл хлороформа. В полученном растворе определяют наличие метафоса. Качественное определение: 1.Реакция с о -дианизидииом и перборатом натрия. В пробирку вносят 1 мл ацетонового раствора исследуемого вещества, прибавляют 0,5 мл 3%-го свежеприготовленного ацетонового раствора о-дианизидина и 2 мл 1,25 %-го свежеприготовленного раствора пербората натрия. В зависимости от содержания метафоса через 5—30 мин раствор приобретает желтую или красноватую окраску. 2.Обнаружение метафоса методом хроматографии. На пластинку, покрытую тонким слоем силикагеля КСК, закрепленным гипсом, наносят каплю раствора исследуемого вещества и каплю раствора «свидетеля» (0,01 %-го раствора метафоса в хлороформе). Пластинку подсушивают на воздухе, а затем вносят в камеру для хроматографирования, насыщенную парами смеси н -гексана и ацетона (2: 1). После того как система растворителей поднимется на пластинке на 10 см выше линии старта, пластинку вынимают из камеры, подсушивают на воздухе и опрыскивают раствором бромтимолового синего, содержащим нитрат серебра. После подсушивания пластинки на воздухе ее вносят на 20 мин в термостат, нагретый до 60 °С. После указанного времени пластинку охлаждают и для обесцвечивания фона опрыскивают 10 %-м раствором уксусной кислоты. При наличии метафоса и ряда других фосфорсодержащих органических соединений на желтом фоне пластинки появляются лилового цвета пятна. Карбофос Карбофос (малатион, фосфотион, фостион и др.) —0,0-диметил-5-(1,2-дикар-бэтоксиэтил)-дитиофосфат — относится к ядохимикатам, принадлежащим к органическим соединениям фосфора (производным дитиофосфорной кислоты). Карбофос — бесцветная жидкость (т. кип. 156—157 С С при 0,09 кПа) с характерным неприятным запахом. Он слабо растворяется в воде, хорошо — в большинстве органических растворителей, кроме предельных углеводородов. При продолжительном нагревании (около 150 °С) карбофос изомеризуется, превращаясь в тиоловый изомер: Карбофос медленно гидролизуется водой. Гидролиз ускоряет, ся в присутствии кислот и щелочей. Карбофос при длительном контакте с железом разлагается и теряет инсектицидные свойства. Технический препарат представляет собой темно-бурую жидкость с неприятным запахом, содержит примеси диэтилдитио-фосфорной кислоты, ксилола и др. Карбофос выпускается в виде концентрата эмульсии, содержащего 30—60 % действующего вещества. Применяется в качестве контактного инсектицида и акарицида для борьбы с тлей, клещами на плодовых деревьях и полевых культурах и др. В организме карбофос окисляется с образованием малаоксона, обладающего выраженной антихолинэстеразной активностью. При отравлении карбофосом появляются слюнотечение, рвота, понос, одышка, цианоз и т. д. Изолирование: В колбу вместимостью 500 мл вносят 100 г мелкоизмельченного биологического материала, прибавляют воду до получения кащицеобразной массы и 100 мл хлороформа. Содержимое колбы оставляют на 4 ч при частом взбалтывании. Затем отделяют хлороформную вытяжку, а биологический материал еще 2 раза настаивают с хлороформом (порциями по 50 мл) в течение 2 ч при частом взбалтывании. Хлороформные вытяжки соединяют, фильтруют и выпаривают досуха. Сухой остаток растворяют в 10 мл хлороформа. В полученном растворе определяют наличие карбофоса. Качественное определение: 1.Реакция с диазотированной сульфаниловой кислотой. Несколько миллилитров хлороформного раствора или хлороформной вытяжки вносят в пробирку и жидкость выпаривают досуха. К сухому остатку прибавляют 2 мл воды, 1 мл раствора диазотированной сульфаниловой кислоты и 0,5 мл 5 %-го раствора гидроксида натрия. Появление вишнево-красной окраски указывает на наличие карбофоса в исследуемом растворе. 2.Реакция с реактивом Марки. В фарфоровую чашку вносят несколько миллилитров хлороформного раствора исследуемого препарата, который выпаривают досуха. К сухому остатку прибавляют 5—10 капель реактива Марки. Появление оранжевой окраски, которая через некоторое время переходит в темно-коричневую, указывает на наличие карбофоса в исследуемом растворе. 3.Обнаружение карбофоса методом хроматографии. На пластинку, покрытую тонким слоем силикагеля КСК, закрепленным гипсом, наносят каплю раствора исследуемого вещества и каплю раствора «свидетеля» (0,01 %-го раствора карбофоса в хлороформе). Пластинку подсушивают на воздухе, а затем вносят в камеру для хроматографирования, насыщенную парами смеси н -гексана и ацетона (2: 1). После того как система растворителей поднимется на пластинке на 10 см выше линии старта, пластинку вынимают из камеры, подсушивают на воздухе и опрыскивают раствором бромтимолового синего, содержащим нитрат серебра. После подсушивания пластинки на воздухе ее вносят на 20 мин в термостат, нагретый до 60 °С. После указанного времени пластинку охлаждают и для обесцвечивания фона опрыскивают 10 %-м раствором уксусной кислоты. При наличии карбофоса и ряда других фосфорсодержащих органических соединений на желтом фоне пластинки появляются лилового цвета пятна.
Хлорофос Хлорофос (дилокс, диптерекс, рицифон, тувон, трихлорофон) — 0,0-диметил- (2, 2, 2-трихлор-1-оксиэтил)-фосфонат — принадлежит к широко применяемым в сельском хозяйстве фосфорорганическим соединениям (ФОС). Хлорофос—белый кристаллический порошок (т. пл. 84 °С). Он растворяется в воде, бензоле, хлороформе и других органических растворителях, хуже — в парафиновых углеводородах. Хлорофос медленно разлагается в кислой среде и более быстро — в щелочной. Он относительно быстро разлагается в разбавленных растворах на свету. При разложении хлорофоса в кислой среде образуется метиловый спирт и О-метил-(2, 2, 2-трихлор-1-оксиэтил)-фосфорная кислота.
В щелочной среде при разложении хлорофоса образуется довольно токсичное соединение О,О-диметил-О-(2,2-дихлорвинил)-фосфат (ДДВФ):
В растворах продукты разложения хлорофоса подвергаются дальнейшим превращениям. Разрушение хлорофоса усиливается в присутствии окислителей, а также железа. Поэтому этот препарат нельзя хранить в железной таре. Технический хлорофос — это кристаллическая или пастообразная масса, содержащая около 80 % действующего вещества. При хранении кристаллизуется. Этот препарат выпускается в виде 80 %-го смачивающего порошка или в виде гранул. Он применяется как контактный или кишечный инсектицид для обработки садов, виноградников, зерновых, бахчевых и др. 0,1— 0,3 %-й раствор хлорофоса применяется для борьбы с мухами, паразитами человека и животных, для обработки жилых помещений и т. д. Хлорофос относится к ядохимикатам средней токсичности. Проявляет раздражающее действие на кожу, понижает активность холинэстеразы в крови. Более выраженный холинэстераз-ный эффект имеет продукт разложения хлорофоса — ДДВФ. При хронических отравлениях хлорофосом наблюдается нарушение функции печени, заболевание сердечно-сосудистой системы и др. Изолирование: В колбу вместимостью 500 мл вносят 100 г измельченного биологического материала и 150 мл воды, подкисленной серной кислотой до рН = 2,0...2,5. Смесь оставляют на 2 ч, часто перемешивая, затем процеживают через марлю. К биоматериалу еще два раза прибавляют воду, подкисленную до рН = 2,0...2,5 (по 75 мл) и каждый раз настаивают по 1 ч, а затем сливают водные вытяжки. Объединенные кислые водные вытяжки центрифугируют. Центрифугат переносят в делительную воронку, прибавляют 30 мл хлороформа и смесь взбалтывают 10 мин. Хлороформную вытяжку сливают. Хлорофос из кислой водной вытяжки еще 4 раза экстрагируют хлороформом (по 30 мл). Хлороформные вытяжки соединяют и выпаривают при комнатной температуре досуха. Сухой остаток растворяют в 5 мл воды, затем раствор фильтруют через бумажный фильтр. Фильтрат используют для обнаружения хлорофоса. Качественное определение: 1.Реакция с пиридином и щелочью (реакция Фудживара). В пробирку вносят 1 мл исследуемого раствора, 1 мл пиридина и 1 мл 30 %-го раствора гидроксида натрия. Смесь нагревают на кипящей водяной бане 5 мин. При наличии хлорофоса в пробе появляется красная или розовая окраска. Предел обнаружения: 10 мкг хлорофоса. Эту реакцию дает также ряд хлорсодержащих соединений алифатического ряда
Для обеспечения возможности протекания реакции рН должно равняться 9—11. 3.Реакция образования изонитрила. В пробирку вносят 0,01— 0,03 г исследуемого вещества и 1 мл этилового спирта. Смесь взбалтывают, затем прибавляют 2 мл 10 %-го спиртового раствора гидроксида натрия и 1 каплю анилина. При нагревании смеси ощущается характерный запах изонитрила. Реакция неспецифична. Ее дают хлороформ, ДДВФ и некоторые другие хлорсодержащие вещества. 4.Реакция с о -толидином. В фарфоровую чашку вносят 0,2— 0,5 мл водного или спиртового раствора исследуемого вещества, 1 мл 0,5 %-го раствора о -толидина в ацетоне и 1 мл смеси растворов пероксида водорода и гидроксида натрия. В присутствии хлорофоса появляется желтая или оранжевая окраска. Эту реакцию дают метафос, тиофос и др. 5.Реакция с 2,4-динитрофенилгидразином. В пробирку вносят 1—10 капель исследуемого раствора и 2 капли 1 н. раствора гидроксида натрия. Через 20 мин прибавляют 1 каплю 0,1 %-го раствора 2,4-динитрофенилгидразина в 4 н. растворе соляной кислоты. Пробирку выдерживают в кипящей водяной бане 30 мин. После этого смесь охлаждают, прибавляют 1 каплю 4 н. раствора гидроксида натрия и 0,5 мл этилового спирта. При наличии хлорофоса в пробе появляется синяя или сине-фиолетовая окраска. Эту реакцию дают ДДВФ, тиофос и др. 6.Реакция с ацетоном. В пробирку вносят 0,1—0,5 мл раствора исследуемого вещества в этиловом спирте, прибавляют 1 мл ацетона и 0,5 мл 0,5 н. спиртового раствора гидроксида натрия. При наличии хлорофоса в пробе через 5—15 мин появляется розовая окраска, переходящая в оранжевую. 7.Холинэстеразная проба. Хлорофос понижает активность ацетилхолинэстеразы, которая теряет способность разлагать ацетилхолин. 8.Обнаружение хлорофоса методом хроматографии. На пластинку, покрытую тонким слоем силикагеля КСК, закрепленным гипсом, наносят каплю спиртового раствора исследуемого вещества и каплю раствора «свидетеля». Пятна подсушивают на воздухе. Затем пластинку вносят в камеру, насыщенную парами системы растворителей (смесь равных объемов н -гексана и ацетона). После того как система растворителей поднимется на пластинке на 10 см выше линии старта, пластинку вынимают из камеры, подсушивают на воздухе и опрыскивают смесью 2 %-го водного раствора резорцина и 10 %-го раствора карбоната натрия, взятых в соотношении 2: 3. Подсушенную пластинку нагревают 7—10 мин в сушильном шкафу при 100 °С. При этом пятна на пластинке приобретают оранжевую окраску. Количетсвенно определение основано на реакции с 2,4-динитрофенилгидразином. Фотоэлектроколориметрия. Гексахлорциклогексан
Гексахлорциклогексан (бензолгексахлорид, гаммек-сан, вермексан и др.) — 1, 2, 3, 4, 5, 6-гексахлорцик-логексан — принадлежит к галогенпроизводным алициклических углеводородов. ГХЦГ представляет собой смесь нескольких сте-реоизомеров. В чистом виде получено восемь изомеров этого вещества, из которых только γ-изомер обладает выраженными инсектицидными свойствами. Гексахлорциклогексан — темновато-серое или светло-серое кристаллическое вещество с, запахом плесени. Запах этого препарата обусловлен примесями пентахлорциклогексана и тетра-хлорциклогексана. Очищенный гексахлорциклогексан не имеет запаха. В зависимости от соотношения количеств изомеров гек-сахлорциклогексана в смеси она плавится в интервале температур 90—309 ° C. ГХЦГ слабо растворяется в воде, парафиновых и циклопара-финовых углеводородах, хорошо — в спиртах, кетонах и эфирах. При повышенной температуре ГХЦГ возгоняется, при этом часть этого препарата разлагается с образованием трихлорбен-зола и хлороводорода, он хорошо сохраняется в почве. ГХЦГ относится к токсичным соединениям кожнорезорбтив-ного действия. Обладает выраженными кумулятивными свойствами. Вызывает гиперемию кожи, отечность, появление пузырьков и пустул, раздражение конъюктивы глаз. ГХЦГ длительно задерживается в органах и тканях организма (особенно в жировой ткани), выделяется через почки, пищевой канал, переходит в молоко кормящих женщин и г. д.
Изолирование гексахлорциклогексана из трупного материала. В круглодонную колбу вместимостью 500 мл вносят 100 г тщательно измельченного трупного материала (органы трупов, желудок и кишки с содержимым), прибавляют воду до получения кашицеобразной массы. Эту смесь подкисляют водным раствором щавелевой кислоты до явно выраженной кислой реакции (по лакмусу). Колбу присоединяют к аппарату для перегонки с водяным паром, затем устанавливают ее на кипящую водяную баню и производят перегонку ГХЦГ с водяным паром. В приемник собирают 300 мл дистиллята. В ходе перегонки ГХЦГ с водяным паром на внутренней стенке холодильника может появиться белый налет, а в дистилляте — твердые белые частицы. По окончании отгонки холодильник отделяют от аппарата и промывают диэтиловым эфиром. Эфир, использованный для промывки, присоединяют к дистилляту. Дистиллят переносят в делительную воронку вместимостью 500 мл и три раза взбалтывают с новыми порциями эфира по 100 мл. Соединенные эфирные вытяжки вносят в другую такую же делительную воронку, прибавляют воду и взбалтывают. Водную фазу отбрасывают, а эфирный слой переносят в колбу и отгоняют эфир до небольшого объема. Остаток вносят в фарфоровую чашку и при комнатной температуре выпаривают эфир до тех пор, пока в чашке не останется немного жидкости. В этой жидкости определяют наличие ГХЦГ. Качественное определение: 1.Реакция с янтарной кислотой и сульфатом железа (III). В микропробирку вносят несколько сантиграммов янтарной или фталевой кислоты и небольшое количество исследуемого вещества или 1—2 капли его раствора (в этом случае растворитель выпаривают досуха). Отверстие пробирки накрывают кружком фильтровальной бумаги, смоченной 0,1 %-м раствором сульфата железа (III). Пробирку погружают в глицериновую баню, нагретую до 200 °С. При наличии ГХЦГ в пробе на бумаге появляется синее пятно. Предел обнаружения: 30 мкг ГХЦГ в пробе. Реакция неспецифична для обнаружения ГХЦГ. Ее дают и некоторые другие хлорпроизводные углеводородов. 2.Реакция отщепления хлора и обнаружение его с нитратом серебра. 5—10 мл раствора препарата вносят в колбу вместимостью 50 мл и прибавляют двукратный объем 10 %-го спиртового раствора гидроксида калия. Колбу соединяют с воздушным холодильником, устанавливают ее на кипящую водяную баню и нагревают 1 ч. Затем открывают пробку и продолжают нагревать до удаления основного количества жидкости. Оставшуюся жидкость охлаждают до комнатной температуры, подкисляют разбавленной азотной кислотой до кислой реакции (по лакмусу), затем прибавляют раствор нитрата серебра. При этом выпадает белый осадок, растворимый в водном растворе аммиака. 3.Реакция дехлорирования ГХЦГ и последующего нитрования образовавшегося бензола. При нагревании ГХЦГ со спиртовым раствором щелочи происходит отщепление хлора (дехлорирование) от молекулы этого препарата и образуется бензол. При действии нитрата натрия и концентрированной серной кислоты происходит нитрование образовавшегося бензола (образуется м -динитробензол). От прибавления гидроксида калия появляется фиолетовая окраска. 4.Обнаружение ГХЦГ методом хроматографии. На линию старта на хроматографической пластинке наносят несколько капель исследуемой жидкости. Через 2 см правее на линию старта наносят каплю раствора «свидетеля». Пятна подсушивают на воздухе, затем пластинку вносят в камеру для хроматографирования, на дно которой налит слой н -гексана. Пластинку оставляют в камере для хроматографирования до тех пор, пока жидкость не поднимется на 10 см выше линии старта. Затем пластинку вынимают из камеры, подсушивают на воздухе, опрыскивают водно-ацетоновым раствором аммиаката серебра. После этого пластинку в течение 10—15 мин облучают УФ-светом. Источник облучения должен находиться на расстоянии 20 см от пластинки. При наличии ГХЦГ в исследуемой пробе пятна на пластинке приобретают серовато-черную окраску. Количественное онределение: Определяют аргентометрическим способом (индикатор — железо-аммонийные квасцы) по количеству хлори-иона, образовавшегося при нагревании ГХЦГ на кипящей водяной бане в течении 2 часов с 0.3 н раствором едкого натра. Кол
|
||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-19; просмотров: 4621; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 13.59.82.60 (0.012 с.) |