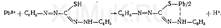Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Исследование относительно больших осадков сульфата свинцаСодержание книги
Поиск на нашем сайте
Реакция с иодидом калия. При наличии ионов свинца выпадает желтый осадок PbI 2, который растворяется при нагревании и вновь появляется в виде желтых пластинок при охлаждении раствора. Реакция с хроматом калия. Образование оранжево-желтого осадка хромата бария указывает на наличие ионов свинца в растворе. Предел обнаружения: 2 мкг свинца в пробе. Реакция с сероводородной водой. Появление черного осадка сульфида свинца (или мути) указывает на наличие ионов свинца в растворе. Предел обнаружения: 6 мкг свинца в пробе. Реакция с серной кислотой. Появление белого осадка указывает на наличие ионов свинца в растворе. Предел обнаружения: 0,2 мг ионов свинца в пробе. Исследование малых осадков сульфата свинца Выделение ионов свинца из минерализата. К раствору, содержащему ацетат свинца, прибавляют хлороформный раствор дитизона и взбалтывают. При этом образуется однозамещенный дитизонат свинца Pb(HDz) 2, хлороформный раствор которого имеет оранжево-красную окраску:
Образовавшийся в хлороформной фазе однозамещенный дитизонат свинца разлагают азотной кислотой. При этом образуется нитрат свинца, который переходит в водную фазу, Реакция с хлоридом цезия и иодидом калия. При наличии ионов свинца образуются желто-зеленые игольчатые кристаллы, собранные в виде сфероидов:
Предел обнаружения: 0,01 мкг свинца в пробе. Реакция с ацетатом меди и нитритом калия. Образование черных или коричневых кристалликов, имеющих форму куба, указывает на наличие ионов свинца в водной фазе:
Предел обнаружения: 0,01 мкг свинца в пробе. Количественное определение РЬ2+ после выделения его в виде сульфата свинца возможно несколькими методами: а) бихроматно-йодометрическим по избытку бихро- 2РЬ(ОСОСН3)2 + К2Сг207 + НОН = 2РЬСЮ4 + 2СН3СООК + 2СИ3СООН; К2Сг207 + 6KI + 7H2S04 ^=± 3I2 + Cr2(S04)3 + 4K2S04 + 7Н20, I2 + 2Na2S203 = 2NaI -f Na2S40s б) экстракционно-фотометрически и по дитизонату свинца. В основу метода положена приведенная выше чувствительная и довольно специфичная реакция. Pb(0C0CH3)2 + 2H2Dz (при рН 7-10) = Pb(HDz)2 + 2СН3С00Н. в) комплексонометрическим, являющимся общим для многих двухвалентных и некоторых трехвалентных катионов. Принцип комплексонометрического титрования сводится к следующему: к исследуемому раствору, содержащему определенный катион, прибавляют при строго определенном значении рН небольшое количество соответствующего индикатора — образуется хорошо растворимое в воде окрашенное комплексное соединение индикатора с катионом. При титровании трилонюм Б (комплексов III) —динатриевой солью зтилендиаминтетрауксусной кислоты— комплекс катиона с индикатором разрушается, так как трилон Б образует более прочный комплекс с определяемым катионом. В эквивалентной точке выделяется свободный индикатор, окрашивая раствор в цвет, присущий индикатору при данном значении рН среды. Большинство катионов определяется в щелочной среде, для чего в титруемый раствор вводят аммиачный буфер (смесь аммиака и хлорида аммония). ТЕТРАЭТИЛСВИНЕЦ ТЭС — прозрачная бесцветная жидкость с неприятным, раздражающим запахом (в ничтожно малых концентрациях имеет приятный фруктовый запах). Он почти нерастворим в воде, легко растворяется в керосине, бензине, хлороформе. Изолирование тетраэтилсвинца производится различными методами в зависимости от характера объекта. а) При исследовании внутренних органов трупа изолирование производят дистилляцией с водяным паром. Дистиллят в количестве 50—100 мл собирают в приемник, содержащий 30 мл насыщенного спиртового раствора йода; приемник соединяют с уловителем, содержащим также насыщенный спиртовой раствор йода. После отгонки содержимое уловителя и дистиллят объединяют, покрывают часовым стеклом и оставляют на 30 минут при комнатной температуре, затем упаривают досуха в фарфоровой чашке на водяной бане. Остаток обрабатывают азотной кислотой (1:2) и вновь упаривают на водяной бане. Кристаллический остаток растворяют в небольшом количестве дистиллированной воды и подвергают качественному и количественному исследованию на ион свинца по описанному выше методу. Для целей химико-токсикологического анализа метод разработан А. Н. Крыловой. Исследование на ТЭС следует производить немедленно по получении объекта. Положительный результат получается при содержании 0,3 мг ТЭС в 100 г исследуемого объекта. В случае отрицательного результата при исследовании на ТЭС необходимо произвести анализ на продукты разложения тетраэтилсвинца — нелетучие соединения свинца, для чего содержимое колбы после отгонки ТЭС помещают в большую фарфоровую чашку и выпаривают на водяной бане. Остаток подвергают минерализации серной и азотной кислотами и исследуют, как описано выше. Положительный результат наблюдают еще при наличии 0,3 мг неорганического свинца в 100 г трупного материала. б) Изолирование из растительных объектов. При исследовании одежды на наличие ТЭС ее подвергают извлечению органическим растворителем с дальнейшим переведением ТЭС в неорганические соединения свинца, обнаружением и количественным определением его. в) Изолирование из бензинов. Все способы изолирования ТЭС из бензина сводятся к разрушению молекулы тетраэтилсвинца и обнаружению и определению РЬ2+. В качестве примера приведем один из способов. Смешивают 20 мл исследуемо Качественное обнаружение и количественное определение. После разрушения молекулы ТЭС обнаружение и определение РЬ2+ не представляет никаких особенностей. Пригодны все описанные выше реакции и методы. Йодометрически удается определить до 1 мг ТЭС в исследуемой навеске (А. Н. Крылова). СОЕДИНЕНИЯ БАРИЯ Растворимые соединения бария, поступившие в организм через пищевой канал, всасываются в желудке и вызывают отравление. Соединения бария выделяются из организма главным образом через кишки. Следы этих соединений выводятся через почки и частично откладываются в костях. Сведения о содержании бария как нормальной составной части клеток и тканей организма в литературе отсутствуют.
|
||||
|
Последнее изменение этой страницы: 2016-04-19; просмотров: 2918; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.226.28.97 (0.007 с.) |