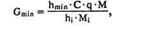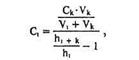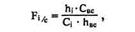Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Приготовление эталонных растворовСодержание книги
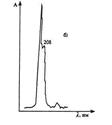
Поиск на нашем сайте а) В мерной посуде готовится раствор ортофосфорной кислоты в дистиллированной воде (0,2 М). Для этого: — на аналитических весах берется навеска ортофосфорной кислоты; — навеска переносится в колбу на 100 мл, объем доводится дистиллированной водой до метки, и смесь встряхивается до полного растворения (раствор № 1). б) В мерный цилиндр на 100 мл переносится 75 мл раствора № 1, 20 мл метанола и 1 мл свежеперегаанного при 5б°С диэтиламина. Смесь хорошо перемешивается. в) Для приготовления эталонных растворов анализируемых фенилалкиламинов используются чистые субстанции норэфедрина, эфедрона, эфедрина, амфетамина и метамфетамина, и проводят — на лабораторных весах взвешивается по 25 ± 1 мг указанных веществ; — навеска каждого вещества переносится в соответствующую маркированную отдельную колбу на 50 см и заполняется элюентом до метки; — содержимое колбы встряхивается до полного растворения осадка. Элюеыт и эталонные растворы сравнения перед использованием необходимо очистить от механических примесей (пыль из атмосферы, частицы вещества), которые могут забивать фильтры колонки и нарушать нормальную работу насоса и хроматографической колонки. Для удаления этих примесей используется владипоровская мембрана с размером пор 0,15 — 0,25 мкм или мелкопористый стеклянный фильтр. Элюент перед работой необходимо продегазировать в течение 10 минут. Для этого используется ток газообразного гелия при расходе 40 — 50 мл/мин, обработка на ультразвуковой бане или вакуумный насос. АНАЛИЗ МОДЕЛЬНОЙ СМЕСИ ФЕНИЛАЛКИЛАМИНОВ И ОПРЕДЕЛЕНИЕ ИХ ПАРАМЕТРОВ УДЕРЖИВАНИЯ Тестовая модельная смесь норэфедрина, эфедрона, эфедрина, амфетамина, метамфетамина готовится в растворе подвижной фазы. Для этого: а) берется навеска норэфедрина, эфедрина, эфедрона, амфетамина, метамфетамина; б) навески переносятся в колбу 50см, объем доводится до метки, смесь встряхивается до полного растворения и фильтруется.. Хроматографирование модельной смеси проводится при следующих условиях: расход элюента — 100 мкг/мл; объем вводимой пробы — 7 мкл; масштаб чувствительности — 0,4 е.о.п.; время измерения — 0,3 с; длина волны — 210 нм. ОПРЕДЕЛЕНИЕ ПРЕДЕЛОВ ОБНАРУЖЕНИЯ АНАЛИЗИРУЕМЫХ ВЕЩЕСТВ Предел обнаружения анализируемого вещества устанавливается по величине такого количества вещества, которое вызывает сигнал, превышающий в 5 раз уровень флкжтуационных шумов, который на шкале чувствительности составляет 2 мм. Значение пределов обнаружения (Gmin, мг) рассчитывается по формуле
АНАЛИЗ БИОПРОБ НА СОДЕРЖАНИЕ ФЕНИЛАЛКИЛАМИНОВ Качественный анализ Идентификация фенилалкиламинов, содержащихся в биопробах, производится следующим образом: а) сопоставляются время (объемы) удерживания и коэффициенты емкости определяемого компонента и образца сравнения (эталонный раствор) индивидуальных фенилалкиламинов;
б) сравниваются УФ-спектры предполагаемого компонента и об в) оценивается совпадение значений времени удерживания определяемого компонента и образца сравнения при добавлении эталонного раствора в раствор экстракта из биопробы (концентрация г) сопоставляются УФ-спектры определяемого компонента и образца сравнения при двух длинах волн, и оценивается их спектральное отношение.
Количественный анализ Для количественного анализа фенилалкиламинов в биощюбах можно использовать различные методы, в том числе метод добавки, метод внешнего стандарта, метод внутреннего стандарта и т.д. а) Метод добавки. В соответствии с методом добавки проводят анализ раствора экстракта биопробы из этого же раствора, но с добавкой в него раствора известной концентрации предполагаемого фенилалкиламина (эталонного раствора). Анализы растворов "без добавки" и "с добавкой" должны проводиться в одном масштабе регистрации. Концентрация определяемого вещества (О) в растворе экстракта из биопробы определяется но формуле
где Ск —- концентрация "добавки" в растворе подвижной фазы; Vk —- объем добавленного эталонного раствора; Vi — объем раствора экстракта с определяемым веществом; hi — высота сигнала определяемого вещества в растворе экстракта из биопробы; hi+k—- высота сигнала определяемого вещества после добавки в раствор экстракта эталонного раствора. б) Метод внешнего стандарта. В соответствии с методом внешнего стандарта и с учетом линейной зависимости выходного сигнала от массы вещества последовательно, сразу же после анализа раствора экстракта биопробы проводят анализ эталонного раствора идентифицированного вещества. Концентрация эталонного раствора (Ск) должна быть близка к концентрации определяемого вещества в растворе экстракта. Анализы эталонного раствора и экстракта биопробы должны проводиться в одном масштабе регистрации.
где hi — высота сигнала определяемого наркотического вещества в растворе экстракта биопробы; hk — высота пика вещества эталонного раствора. в) Метод внутреннего стандарта. В соответствии с методом внутреннего стандарта к биообъекту до операции пробоподготовки добавляется известное количество вещества, принятого за стандарт. Концентрация определяемого вещества (СО рассчитывается по формуле
где Свс — концентрация внутреннего стандарта; hi — высота пика (или площадь) определяемого вещества; hBc — высота пика (или площадь) стандарта; Fi/bc— относительный калибровочный фактор. Относительный калибровочный фактор компонента Fi/с вычисляется по формуле
где hi — высота пика (или площадь) компонента известной концентрации (калибровочный раствор); Q —концентрация калибровочного раствора определяемого компонента; hue — высота пика (или площадь) внутреннего стандарта; Свс — концентрация внутреннего стандарта.
СЕЛЕКТИВНЫЙ АНАЛИЗ ЭФЕДРОНА Используя значительное различие в коэффициентах молярного поглощения эфедрона и других соединений этой группы при 250 нм, можно провести селективный анализ эфедрона в смеси с другими компонентами этой группы — норэфедрином, эфедрином, амфетамином, метамфетамином. При этом анализ проводится путем детектирования при двух длинах волн: 210 нм для регистрации всех определяемых фенилал-киламинов и 250 нм для селективно определяемого эфедрона с последующим сопоставлением полученных хроматограмм для количественного определения эфедрона в биопробах. При детектировании при длине волны 250 нм имеет место селективная чувствительность спектрофотометрического детектора к определяемому эфедрону и практически полное отсутствие чувствительности к сопутствующим компонентам.
Эфедрин
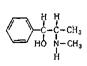
Эфедрин (1-фенил-2-метиламинопропанола-1-. гидрохлорид) относится к ациклическим алкалоидам, в молекуле которых аминогруппа находится в боковой цепи. Эфедрин и его стереоизомер псевдоэфедрин находится в некоторых видах эфедры. Эфедрин также содержится в тиссе ягодном и в некоторых других растениях. Находящийся в растениях эфедрин является левовращающим, а синтетический — правовращающим. К числу синтетических препаратов относится эфетонин, являющийся рацематом эфедрина. Основание эфедрина растворяется в этиловом спирте (1: 1), воде (1:36), диэтиловом эфире и хлороформе. Гидрохлорид эфедрина растворяется в воде (1:4), этиловом спирте (1: 17), практически не растворяется в диэтиловом эфире и хлороформе. Эфедрин экстрагируется органическими растворителями из щелочных водных растворов. Он повышает артериальное давление, сужает сосуды, расширяет зрачок и бронхи, уменьшает перистальтику кишок, возбуждает центральную нервную систему. В медицине эфедрин применяется при бронхиальной астме, в глазной практике и при ряде других заболеваний. Метаболизм. Эфедрин быстро всасывается из пищевого канала и накапливается в печени, почках, легких и мозге. Через 24 ч 80 % принятой дозы эфедрина выделяется из организма с мочой в неизмененном виде. Незначительная часть дозы эфедрина подвергается N-деметилированию с образованием феиилпропаноламина. Этот метаболит эфедрина выделяется из организма с мочой. Эфедрин — в неизмененном виде выделяется 55—75%. Основными метаболитами являются: 8 — 20%— норэфедрин, 4 — 13%—безаминные метаболиты (бензойная и гиппуровая кислоты, фенилпропандиол). При щелочной моче выведение эфедрина снижается до 20—35%, соответственно увеличивается содержание норэфедрина. рКа = 9,6. Т ½ = 9-11ч. Обнаружение эфедрина 1. Реакция с солями меди и сероуглеродом. При взаимодействии эфедрина с сероуглеродом и щелочным раствором сульфата меди образуется производное дитиокарбаминовой кислоты, растворимое в бензоле:
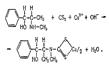
2. Реакция с 2,4-Динитрохлорбензолом. При этом образуется фенилэтилкетон и амин:
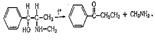
Образовавшийся при этой реакции метиламин с 2,4-динитро-хлорбензолом дает соединение желтого цвета, которое экстрагируется хлороформом:
3. Реакция с реактивом Драгендорфа. При взаимодействии эфедрина с реактивом Драгендорфа образуются кристаллы, напоминающие тонкие иглы, собранные в пучки.
|
|||
|
Последнее изменение этой страницы: 2016-04-19; просмотров: 1248; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.214 (0.009 с.) |