
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Пространствеая структура биоорганических молекул. Виды изомерииСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
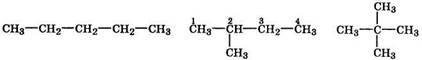
(Материал для самоподготовки) Многообразие органических соединений обусловлено в значительной мере явлением изомерии. Изомерами называются соединения с одинаковым качественными количественным составом, но отличающиеся последовательностью связывания атомов или расположением их в пространстве. Даже минимальные структурные различия между изомерами биомолекул приводят к заметным различиям в их физических и химических свойствах и очень сильно влияют на их биологическую активность. Возможны следующие типы изомерии: структурная и пространственная (стереоизомерия). Структурная изомерия. Этот тип изомерии обусловлен различным взаимным расположением атомов в молекулах. При этом различают изомерию углеродного скелета и изомерию положения. Изомерия углеродного скелета обусловлена способностью атомов углерода образовывать как прямые (нормальные) углеродные цепи, так и разветвленные цепи с различной степенью разветвления. Например, у пентана имеются три изомера:
н-пентан 2-метилбутан 2,2-диметилпропан
Изомерия положения обусловлена различным положением заместителей, функциональных групп или кратных связей в молекулах органических соединений одинакового состава. Например:
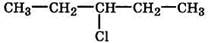
— перемещение заместителя по цепи:
1-хлорпентан 2-хлорпентан 8-хлорпентан
— перемещение кратной связи по цепи: пентен-1 пентен-2 — взаимное расположение заместителей в соединениях ароматического ряда:
1,2-диметилбензол 1,8-диметилбензол 1,4-диметилбензол (opтo -ксилол) (мета -ксилол) (пара -ксилол)
Для рассмотренных видов структурной изомерии взаимное превращение изомеров друг в друга при обычных условиях отсутствует. Классовая изомерия также является примером структурной изомерии и определяется различной очередностью расположения атомов в молекулах веществ, относящихся к различным классам. Примером изомерии данного вида могут молекулы этилового спирта и диметилового эфира: молекулярная формула которых – C2H6O, а структурные формулы веществ соответственно можно представить следующим образом: CH3-CH2-OH и CH3-O-CH3
Особым случаем структурной изомерии является таутомерия. Таутомерия — явление равновесной динамической изомерии, при которой происходит быстрое обратимое самопроизвольное превращение структурных изомеров, сопровождаемое миграцией подвижной группы между двумя или несколькими центрами в молекуле. Таутомерия свойственна соединениям, в молекулах которых имеются разные реакционноспособные группировки. Например, в молекулах природных аминокислот имеются две группы с противоположными свойствами: аминогруппа - основные свойства - и карбоксильная группа — кислотные свойства. Между этими группами осуществляется перенос протона, и поэтому такой вид изомерии называется прототропной таутомерией. Для обозначения таутомерного равновесия в учебнике использованы пунктирные стрелки. H2N—CHR—СООН <=> H3 Для всех природных аминокислот в кристаллическом состоянии и в водных растворах наиболее устойчив таутомер, имеющий структуру биполярного иона. Его содержание превышает 99,9%. Поэтому во многих учебных пособиях все природные α-аминокислоты всегда изображены в виде таутомера с биполярно-ионной структурой. Прототропная таутомерия бывает разных видов: кето-енольная, лактим-лактамная и др. Кроме прототропной таутомерии в природных соединениях наблюдается кольчато-цепная таутомерия, которая особенно характерна для углеводов. Данные виды изомерии будут более подробно рассмотрены в соответствующих главах. ГЛАВА 2. ЭЛЕКТРОННОЕ СТРОЕНИЕ ОРГАНИЧЕСКИХ МОЛЕКУЛ. КИСЛОТНОСТЬ И ОСНОВНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ. Вопросы к занятию.
1. Понятие об оптической изомерии органических соединений. 2. Асимметрические атомы углерода. Хиральные молекулы. 3. Относительная и абсолютная конфигурация молекул. Проекции Фишера. 4. Индуктивный электронный эффект. 5. Мезомерный электронный эффект. Сопряженные системы. 6. Понятие об ароматичности (бензол и небензоидные системы). 7. Электронно-донорные и электронно-акцепторные заместители в ароматическом кольце. 8. Кислотность и основность органических молекул. 9. Понятие о С-Н, О-Н, S-H, N-H кислотах. 10. Влияние электронных эффектов на кислотность и основность.
|
|||||||||
|
Последнее изменение этой страницы: 2016-12-10; просмотров: 511; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.135.249.119 (0.008 с.) |


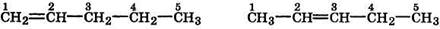

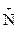 —CHR—СОО-
—CHR—СОО-


