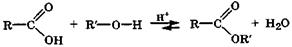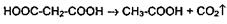Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Карбоновые кислоты как ацилирующие реагентыСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
При реакции ацилирования карбоновыми кислотами в их карбоксильной группе происходит нуклеофильное замещение группы —ОН на другую нуклеофильную частицу
Ацилирование - это реакция нуклеофильного замещения по карбонильному углеродному атому в карбоновых кислотах или их производных, сопровождающаяся образованием связи между их ацилъным остатком
Галогенацилирование. При взаимодействии карбоновых кислот или их солей с галогенидами серы (SOCl2) или фосфора (PCl5, РОС13, РС13, РВr3), содержащими сильнополярные связи S—Тал или Р—Тал, образуются ацилгалогениды, называемые также гало-генангидридами карбоновых кислот, общей формулы
Для ацилгалогенидов характерна высокая электрофильность карбонильного углеродного атома, что вызвано сильными электроноакцепторными свойствами связанного с ним атома галогена. Ацилгалогениды - очень реакционноспособные вещества, неустойчивые к гидролизу, поэтому их хранят в герметичных емкостях, чтобы избежать контакта с парами воды. Ацилгалогениды являются сильными ацилирующими реагентами и используются в органическом синтезе для введения ацильной группы в молекулы органических соединений (карбоновые кислоты, спирты, тиолы, амины, арены).
O-Ацилирование карбоновых кислот. При нагревании карбоновой кислоты с сильными водоотнимающими реагентами (PgOs) происходит реакция ее самоацилирования, сопровождающаяся межмолекулярным отщеплением молекулы воды с образованием ангидрида карболовой кислоты: ангидрид карбоновой кислоты
Карбоновые кислоты или их соли легко ацилируются ацилгалогенидами, так как карбонильный углеродный атом последних более электрофилен, чем в карбоновых кислотах:
Ангидриды карбоновых кислот как ацилирующие реагенты слабее ацилгалогенидов, но сильнее карбоновых кислот.
О-Ацилирование спиртов. Карбоновые кислоты при кислотном катализе ацилируют спирты, образуя сложные эфиры:
Для смещения равновесия вправо необходимо удалять из реакционной смеси воду или связывать ее, используя, например, H2SО4 (конц). В организме реакция ацилирования спиртов карбоновыми кислотами осуществляется с помощью соответствующего фермента, который не только активирует реагенты, но и способствует удалению воды из реакционного центра в результате гидрофобных взаимодействий. Механизм реакции этирификации изложен в разделе «Механизмы реакций органических соединений». S-Ацилирование тиолов. В метаболизме карбоновых кислот большую роль играет их способность при участии АТФ ацилировать кофермент А*( Кофермент А -сложное соединение, содержащее остаток 2-амино-этантиола HSCH2CH2NHR, где R включает пантотеновую кислоту и фосфатное производное аденозина. Кофермент А кратко записывается НВКоА), который содержит тиольную группу (—SH), с образованием сложных тиоэфиров, называемых ацилкоферментами А (ацил-КоА или RCOSKoA):
карбоновая кофермент А ацилкофермент А кислота
В качестве карбоновой кислоты чаще всего выступает уксусная кислота, которая образует ацетилкофермент А (ацетил-КоА или CH3COSKoA):
уксусная кофермент А ацетилкофермент А кислота
Образование ацилкоферментов А в организме способствует активации карбоновых кислот не только в реакциях ацилиро-вания, но и в реакциях их конденсации и декарбоксилирования, сопровождаемых окислительно-восстановительной дисмутацией. В организме S-ацилирование протекает не только с коферментами А, но и с белками, имеющими фрагмент, аналогичный по структуре фрагменту кофермента А, и также содержащими остатки 2-аминоэтантиола и пантотеновой кислоты. Поскольку после ацилирования такие белки способны переносить ацильные группы, то их называют ацилпереносящими белками и обозначают исходную форму НSАПБ, а ацильную форму RСОSАПБ:
ацилпереносящий белок
Ацилпереносящие белки осуществляют перенос различных ацильных групп, но особенно эффективно они переносят ацетильную группу.
N-Ацилирование аминов. Карбоновые кислоты, реагируя с аминами - первичными (R'NH2) или вторичными (R2'NH), - образуют вначале аммониевые соли, которые при нагревании выше температуры их плавления внутримолекулярно отщепляют воду, превращаясь в амиды карбоновых кислот: аммонийная соль амид карбоновой кислоты карбоновой кислоты Ацилирование аминов сложными эфирами, ангидридами или галогенангидридами карбоновых кислот происходит в одну стадию:
Эффективнее и легче всего ацилирование аминов происходит с помощью галогенангидридов кислот. Третичные амины NR3' не образуют амидов. Рассмотренные реакции ацилирования карбоновыми кислотами и их производными, в которых они выступают электрофилами, являются типичными электрофильно-нуклеофильными реакциями, так как они не сопровождаются ни кислотно-основными, ни окислительно-восстановительными, ни комплексообразующими превращениями. С-Ацилирование. Реакции С-ацилирования карбоновыми кислотами и их производными всегда сопровождаются окислительно-восстановительной дисмутацией углеродных атомов участников реакции. В организме реакции ацилирования чаще всего протекают со спиртами, тиолами, аминами, а также с карбонилсодержащими соединениями. В качестве ацилирующих реагентов в живых системах особенно активны тиоэфиры кофермента А и ацилпереносящие белки, а в органическом синтезе - галогенангидриды и ангидриды карбоновых кислот.
Реакции декарбоксилирования При сильном нагревании карбоновых кислот наблюдается их декарбоксилирование:
Способность к этому превращению определяется прочностью связи карбоксильной группы с радикалом, которая понижается, если в нем содержатся электроноакцепторные заместители. Поэтому, например, щавелевая кислота декарбоксилируется уже при слабом нагревании:
малоновую кислоту для этого нужно нагреть значительно сильнее:
Янтарную кислоту (как и уксусную или другие предельные кислоты) практически уже не удается декарбоксилировать нагреванием. Однако декарбоксилирование любых кислот легко осуществляется ферментативным путем и является одной из необходимых стадий превращения органических веществ в организме. Реакции карбоновых кислот по радикалу
Электроноакцепторный эффект карбоксильной группы заключается в повышенной склонности к замещению атомов Н в α-положении молекул предельных кислот. В результате можно вводить атомы галогена в это положение за счет радикального замещения (SR):
Еще легче осуществляется замещение с образованием из уксусной кислоты монофтор-, дифтор- или трифторуксусной кислот. Следует отметить, что ядовитая монофторуксусная кислота содержится в соке некоторых тропических растений. Её соли - монофторацетаты применяются как средства борьбы с грызунами. Особенно сильно проявляется влияние на α-положение в молекуле малоновой кислоты и её эфиров. Суммарный эффект двух карбоксильных групп приводит к тому, что на α-атоме углерода формирукется активный С-Н кислотный центр, т.е. атом водорода может проявлять "кислый" характер и замещаться активными металлами. Это используется в синтетических целях для получения из малоновой кислоты и ее эфиров α-замещенных гомологов:
малоновый эфир
В непредельных кислотах эффект группы -СООН заключается в том, что электрофильное присоединение идет вопреки правилу Марковникова:
Покажите схематически перераспределениие электронной плотности в молекуле акриловой кислоты, назовите электронные эффекты, укажите эффективные заряды на атомах углерода при кратной связи, объясняющие, почему присоединение галогеноводорода (механизм АЕ) происходит подобным образом.
В ароматических кислотах карбоксильная группа выступает как заместитель второго рода, ориентируя дальнейшее замещение в мета- положение и затрудняя реакцию м - сульфобензойная кислота
|
||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-10; просмотров: 1783; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.166.223 (0.008 с.) |

 .
.
 и новым нуклеофилом, содержащим атомы: галогенов (галогенацилирование), кислорода (О-ацилирование), серы (S-ацилирование), азота (N-ацилирование) или углерода (С-ацилирование).
и новым нуклеофилом, содержащим атомы: галогенов (галогенацилирование), кислорода (О-ацилирование), серы (S-ацилирование), азота (N-ацилирование) или углерода (С-ацилирование). :
:

 ; (δ'+> δ''+> δ+)
; (δ'+> δ''+> δ+)