
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Жидкость-воздух или жидкость-жидкость».Содержание книги
Поиск на нашем сайте
Цель работы: 1) измерить поверхностное натяжение растворов ПАВ; 2) построить изотермы поверхностного натяжения и адсорбции; 3) вычислить константы уравнения Ленгмюра и размеры ПАВ. Необходимые реактивы и оборудование; сталагмометр, резиновая груша, термометр, четыре колбы по 50 – 100 мл, стакан вместимостью 100 – 200 мл, водные растворы концентрации 0,02; 0,04; 0,06; 0,08 моль/л.
Ход работы. Поверхностное натяжение приготовленных растворов определяют методом отрыва капель (сталагмометрическим методом). Сталагмометр представляет собой стеклянную трубку с расширением в средней части, заканчивающуюся толстостенным капилляром. Метки, нанесённые на стенках, обозначают уровень вытекающей жидкости. Сталагмометр закрепляют в штативе так, что бы нижний срез капилляра располагался строго горизонтально. Исследуемую жидкость наливают в стакан, который поднимают так, чтобы конец капилляра погрузился в жидкость. С помощью груши набирают жидкость выше верхней метки, избегая образования пузырьков воздуха. Закрывают верхнее отверстие трубки. Стакан опускают на стол, осторожно открывают верхнее отверстие, и жидкость начинает капать из капилляра. Когда уровень жидкости совпадает с верхней меткой, начинаю счёт капель. При совпадении уровня жидкости с нижней меткой, счет капель заканчивают.
Сначала проводят серию измерений для воды, а потом для растворов изоамилового спирта начиная с наименьшей концентрации. Измерения повторяют 3 – 5 раз. Данные о концентрациях исследуемых растворов, а также результаты измерений и расчётов заносят в таблицы:
Для двух соседних точек
Обработка результатов эксперимента: Вычисляют поверхностное натяжение для растворов изоамилового спирта по формуле:
где Поверхностное натяжение воды в зависимости от температуры приведено в нижеприведенной таблице:
Поверхностное натяжение воды на границе с воздухом, Дж/м2.
Строят изотерму поверхностного натяжения, зависимость σ = ƒ(с). За начало оси берут не 0, а число близкое к наименьшему значению, полученному в опыте. Пользуясь изотермой поверхностного натяжения рассчитать Г=ƒ(с). Рассчитывают величины Отрезок, отсекаемый на оси ординат при экстраполяции прямой, равен По величине Г∞ можно найти площадь поперечного сечения молекулы ПАВ и её длину:
где М – молярная масса изоамилового спирта, г/моль; ρ – плотность раствора, 0,89 г/мл.
ГЛАВА 13. АДСОРБЦИЯ НА НЕПОДВИЖНОЙ ГРАНИЦЕ РАЗДЕЛА ФАЗ. ИЗОТЕРМА АДСОРБЦИИ УКСУСНОЙ КИСЛОТЫ НА УГЛЕ.
Вопросы к занятию.
1. Адсорбция на границе твердое тело – газ и её выражение. 2. Физическая и химическая адсорбции и их особенности. 3. Основные положения теории адсорбции. 4. Понятие о молекулярной и полимолекулярной адсорбции. Уравнение изотермы адсорбции Ленгмюра и его физический смысл. 5. Уравнение изотермы адсорбции Фрейндлиха и его логарифмическая форма. 6. Адсорбция на границе твёрдое тело – раствор. 7. Адсорбция из растворов электролитов. 8. Обменная адсорбция на твердой поверхности и её особенности. Понятие об ионитах.
Адсорбция растворенных веществ твердыми адсорбентами является более сложным процессом, чем выше описанные случаи, так как она осложнена присутствием третьего компонента - растворителя, молекулы которого могут конкурировать с молекулами адсорбтива за места на поверхности адсорбента, взаимодействовать с адсорбтивом и с поверхностью адсорбента, если он является электролитом.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-10; просмотров: 448; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.3 (0.01 с.) |



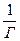

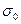 - поверхностное натяжение воды,
- поверхностное натяжение воды, 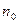 - среднее число капель воды, n – среднее число капель раствора.
- среднее число капель воды, n – среднее число капель раствора.

 , по нему находим Г∞. Вторая константа уравнения Ленгмюра (К) численно равна величине, обратной равновесной концентрации, при которой молекулами адсорбата занята половина адсорбционных центров поверхности адсорбента, т.е. при этой концентрации Г=
, по нему находим Г∞. Вторая константа уравнения Ленгмюра (К) численно равна величине, обратной равновесной концентрации, при которой молекулами адсорбата занята половина адсорбционных центров поверхности адсорбента, т.е. при этой концентрации Г=  . Для определённой величины К на оси ординат вверх от точки пересечения прямой с ней, откладывают отрезок равный
. Для определённой величины К на оси ординат вверх от точки пересечения прямой с ней, откладывают отрезок равный 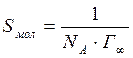 (14)
(14)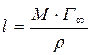 (15)
(15)


