
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Торакоскопия в грудной хирургииСодержание книги
Поиск на нашем сайте
Торакоскопия как самостоятельный хирургический метод имеет почти 100-летнюю историю. В 1910 году в Швеции Ганс Христиан Якобеус ввел термин «торакоскопия» и применил этот метод в клинической практике. Он же впервые при туберкулезе легких наложил лечебный пневмоторакс и сообщил о рассечении спаек в плевральной полости. Правда до конца 50-х годов торакоскопия применялась почти исключительно для создания лечебного пневмоторакса. Лишь в 70-80-е годы торакоскопия нашла применение для диагностики и лечения заболеваний и повреждений груди. До появления эндовидеохирургии торакоскопия имела весьма ограниченные показания, и во многом они определялись опытом, накопленным в отдельных торакальных стационарах. С известной долей иронии можно сказать, что современный этап развития торакоскопии берет свое начало от первой лапароскопической холецистэктомии, выполненной Филиппом Муре в 1987 году. Активное и стремительное развитие видеоторакоскопии (ВТС) приходится на начало 90-х годов. Уже в 1994 году в нашей стране впервые были выполнены успешные видеоторакоскопические лобэктомии и операции по удалению опухолей средостения (Сигал Е.И.). Эндоскопическая хирургия принципиально изменила подходы к лечению многих заболеваний органов грудной клетки. Утверждение некоторых специалистов о возможности выполнения более половины операций на органах груди эндовидеохирургическим способом еще десять лет назад казалось большим преувеличением. Сегодня же видеоторакоскопические операции стали своеобразным «золотым стандартом» и основой тактики при самых различных заболеваниях органов грудной полости. Показания к применению торакоскопии расширяются и вышли за пределы торакальной хирургии. Кардиохирургия, травматология и ортопедия, хирургическая гастроэнтерология берут на вооружение и активно осваивают торакоскопический метод. Общие положения. Для проведения ВТС необходима общая анестезия с раздельной интубацией правого и левого бронхов двухпросветной трубкой. Контроль за положением интубационной трубки осуществляется с использованием фибробронхоскопа, в отдельных случаях при наличии соответствующего оборудования возможен рентгеноскопический контроль. В ходе операции контроль за состоянием пациента предполагает пульсоксиметрию, ЭКГ-мониторинг, измерение артериального давления и концентрации С02 в выдыхаемом воздухе.
Для выполнения ВТС необходима портативная видеокамера и два видеомонитора, что позволяет хирургам находиться друг напротив друга. При использовании одного монитора он должен в зависимости от вида оперативного вмешательства находиться в изголовье или со стороны ножного конца операционного стола. Выполнение большинства ВТС осуществляется в положении на боку с валиком под грудной клеткой. Наиболее часто используются торакопорты диаметром 5,10 и 12 мм. Для ревизии плевральной полости наиболее удобно наложение порта в 4 или 5 межреберье по средней подмышечной линии, при выполнении оперативного приема чаще торакопорты накладываются по передней или задней аксиллярным линиям. При наложении первого порта обязательна пальцевая ревизия плевральной полости. Введение портов в других точках диктуется ходом оперативного вмешательства. Преимущества ВТС по сравнению с традиционными «открытыми» трансторакальными операциями: • Уменьшает операционную травму и кровопотерю • Снижает потребность в аналгетиках и интенсивной терапии в послеоперационном периоде • Существенно не нарушает функцию внешнего дыхания • Уменьшает длительность пребывания в стационаре Показания к выполнению видеоторакоскопии: • Плевральный выпот неясной этиологии • Интерстициальные заболевания легких • Периферические образования в легких • Заболевания средостения • Заболевания перикарда • Оценка состояния лимфатических узлов средостения с целью стадирования рака легкого, молочной железы, пищевода • Закрытые и открытые повреждения грудной клетки • Образования плевры • Внутриплевральное кровотечение и гемоторакс • Хилоторакс • Спонтанный пневмоторакс • Эмпиема плевры и пиопневмоторакс Помимо перечисленных показаний, признаваемых большинством авторов, существуют и другие, которые относятся к смежным хирургическим специальностям или не являются общепринятыми. К ним относятся операции на пищеводе (удаление дивертикулов, лейомиом (Izumi et al 1996), миотомия, эзоф агэктомия (Mafune et al 1997), фундопликация), мобилизация внутренней грудной артерии для шунтирования коронарных сосудов миниинвазивным доступом без искусственного кровообращения, клипирование Боталлова протока (Laborde 1993), дискэктомия при межпозвонковых грыжах в грудном отделе позвоночника, дренирование паравертебральных абсцессов и «холодных натечников» туберкулезной этиологии, дренирование средостения по поводу медиастинитов, стволовая ваготомия, удаление загрудинного зоба и дистопированных паращитовидных желез, медиастинальная лимфодиссекция при раке молочной железы
Противопоказания к торакоскопическим операциям делят на общие и местные. Среди общих противопоказаний основными являются острый инфаркт миокарда, острое нарушение мозгового кровообращения и некорригируемые нарушения в системе гемостаза. Требования к функциональной операбельности пациентов в торакоскопической хирургии, помимо всего прочего, усугубляются необходимостью проведения однолегочной вентиляции. Непереносимость ИВЛ в таком режиме является серьезным сдерживающим фактором расширения показаний для применения торакоскопического метода, даже несмотря на его малую травматичность. Местные противопоказания к проведению ВТС чаще рассматриваются как относительные и их преодоление возможно с накоплением опыта. Относительные противопоказания для видеоторакоскопии: • Плотные плевральные сращения • Зависимость пациента от ИВЛ (неэффективное самостоятельное дыхание) • Невозможность добиться спадения легкого • Тяжелая эмфизема • Поражение корня легкого • Размеры патологических образований в легком менее 5мм и более 5 см (трудности поиска и безопасность атипичной резекции) • Поражение грудной стенки опухолью • Небольшая плевральная полость или значительная анатомическая деформация Основные принципы выполнения видеоторакоскопических операций: • Локализация патологического очага до операции по данным современных методов лучевой диагностики (преимущественно компьютерной томографии с реконструкцией) • Достаточный ателектаз легкого со стороны операции • Порты вводятся на расстоянии от патологического очага для панорамности изображения и эффективного использования инструментов • Необходимо избегать фехтования и резких движений камеры и инструментов • Первый порт вводится под мануальным контролем, а остальные под контролем видеокамеры • Параллельное расположение инструментов и камеры во избежание зеркального отражения • Работа оператора обеими руками • Знание используемого оборудования • Готовность к переходу на открытую торакотомию • Удаление предполагаемых опухолей в специальных контейнерах для исключения ятрогенной диссеминации процесса. Техническое обеспечение торакоскопических вмешательств - оборудование и инструменты. Современный торакальный хирургический стационар должен быть оснащен полноценным комплектом оборудования для эндовидеохирургических вмешательств. Для операций по поводу инфекционных заболеваний внутригрудных органов, послеоперационных инфекционных осложнений следует предусмотреть отдельный комплект оборудования и инструментов.Стандартный эндовидеохирургический комплекс для торакоскопических вмешательств не имеет принципиальных отличий от комплексов, применяемых в лапароскопии. Основная его часть представлена оптической трубкой (торакоскопом) и видеокамерой. Их иногда называют эндовидеосистемой. Используются три вида торакоскопов. Первый стандартная оптическая трубка, не отличающаяся от таковой в лапароскопии. Следует отметить, что в торакоскопии применяется в основном т.н. косая оптика с углом зрения 30-75°, в зависимости от показаний может использоваться и прямая. Незаменимым в практике работы торакального стационара является операционный торакоскоп (с рабочим каналом), позволяющий через один троакар проводить как осмотр плевральной полости, так и минимальные по объему вмешательства (биопсия, иссечение спаек и др.).
Меньшее распространение получили фиброторакоскопы, сочетающие в себе достоинства гибкой волоконной оптики и операционного торакоскопа.Качество изображения, получаемого при торакоскопии, напрямую зависит от характеристик видеокамеры. Большинство современных видеокамер дают двухмерное изображение. Камеры с трехмерным изображением (стереоскопическая эндовидеосистема), давая на первый взгляд явные преимущества, в реальности не нашли кинического применения из-за сложности, высокой стоимости и побочных эффектов в виде мерцания при переводе взгляда хирурга с монитора на операционное поле.Особого внимания заслуживают аппараты для электрохирургических воздействий на ткани. Современный арсенал таких приборов включает высокочастотные электрохирургические комплексы для резки и коагуляции тканей, коагуляции в среде аргона, холодноплазменной коагуляции. Менее широко применяются лазеры, радионож, криоскальпель и др. Для Рис. 299. Передвижной полевой эндовидеохирур- гический комплекс (Производство «эфа», санкт- препаровки сосудов, анатомических Петербург) образований средостения широко используется ультразвуковой диссектор. Определенными особенностями характеризуются инструменты для торакоскопических операций. Кроме обычно используемых в лапароскопии троакаров, зажимов, коагуляторов, диссекторов, очень важно иметь в распоряжении набор биопсийных инструментов, инструменты для препаровки сосудов, мягкие атравматичные зажимы.
Организация работы эндовидеохирургической операционной. Торакоскопические вмешательства относятся к категории сложных операций на органах груди с высоким риском развития интраоперационных осложнений, большой вероятностью конверсии (переход на торакотомию). В связи с этим, они должны проводится только в условиях операционной с возможностью полноценного обеспечения открытых внутригрудных вмешательств. В последние годы разработаны передвижные эндовидеохирургические комплексы, позволяющие проводить торакоскопические операции на органах груди, когда необходим выезд хирургической бригады в стационар, где необходимое оборудование отсутствует, или выполнить операцию в палате
Подготовка кадров. Торакоскопические операции должны производиться торакальным хирургом, имеющим опыт видеоторакоскопических операций и обладающим достаточными навыками выполнения открытых операций. Это требование диктуется стандартом безопасности проведения медицинских манипуляций и абсолютно необходимо для устранения возможных интраоперационных (в том числе ятрогенных) осложнений, а также при выявлении показаний к торакотомии. Следует также упомянуть, что данные многочисленных исследований причин ятрогенных повреждений при эндовидеохирургических вмешательствах показали прямую связь частоты этих осложнений с качеством подготовки специалистов. Кроме того, как показывает опыт, не все хирурги с легкостью овладевают методикой эндоскопических операций, контролируя свои действия по двухмерному изображению на экране монитора.
Обезболивание в торакоскопии. Торакоскопические операции могут быть выполнены под местным, регионарным и общим обезболиванием. Выбор метода обезболивания определяется задачами, которые ставит перед собой хирург, приступая к торакоскопическому вмешательству.Большинство диагностических операций, в том числе биопсий при заболеваниях плевры с успехом выполняются путем сочетания местной инфильтрационной анестезии и регионарной блокады (межреберной, субплевральной, эпидуральной) на фоне медикаментозной седации. При этом, после осмотра плевральной полости и выбора места биопсии в ряде случаев полезным может быть блокада межреберных нервов через пункционную иглу, введенную в торакопорт или терминальная анестезия париетальной плевры орошением концентрированным раствором анестетика. Если производится биопсия легочной ткани можно прибегнуть к введению анестетика в область корня легкого. Для индукции эплевродеза электрохирургическим и механическим способом или плеврэктомии прибегают к субплевральному введению местного анестетика в зоне предполагаемого вмешательства.Общая анестезия в оперативной торакоскопии характеризуется определенными особенностями. Основное и необходимое условие анестезиологического обеспечения торакоскопических операций заключается в том, что легкое на оперируемой стороне должно быть выключено из дыхания. Это, как правило, достигается путем использования двухпросветной интубационной трубки (рис. 300). Такой способ ИВЛ предъявляет дополнительные требования к навыкам анестезиолога, однако не является сложным. Раздельная интубация главных бронхов позволяет сочетать вентиляцию легкого на неоперируемой стороне объемом с высокочастотной ИВЛ на стороне операции. Последний вариант может быть особенно ценным при наличии сомнений в функциональной операбельности пациента. Доказано, что высокочастотная вентиляция коллабированного легкого может обеспечивать не менее 30% газообмена через его паренхиму. Возможны другие варианты ИВЛ при внутригрудных торакоскопических операциях. В редких случаях для коллабирования легкого, осмотра плевральной полости и выполнения несложных манипуляций (биопсия) используют кратковременное прекращение вентиляции. При этом может быть применена однопросветная интубационная трубка. Использование однопросветной трубки также возможно для биопсии плевры или легкого у пациентов с длительно существующим большим по объему выпотом в плевральной полости, когда легкое отодвинуто от грудной стенки и фиксировано в таком положении швартами. Следует лишь отметить, что в большинстве таких ситуаций необходимые манипуляции могут
быть выполнены и под местным обезболиванием. Наконец, в редких случаях интубацию однопросветной трубкой сочетают с окклюзией главного или промежуточного (справа, при вмешательствах на нижних отделах грудной полости) бронхов. Суть методики в интубации трахеи и проведении рядом с интубационной трубкой катетера Фогарти (рис. 301). При этом вначале для коллабирования легкого прекращается вентиляция, баллон катетера раздувают под контролем бронхоскопа, а затем вентиляцию возобновляют. Такая методика используется сравнительно редко и чаще всего вынужденно. Нужно помнить, что, несмотря на обилие вариантов вентиляции легких при торакоскопии, использование обычной двухпросветной интубационной трубки - общее правило и один из стандартов в анестезиологическом обеспечении торакоскопических операций.
Положение пациента на операционном столе. Наиболее распространенным положением для выполнения большинства торакоскопических операций является боковое (рис. 302). При операциях на переднем средостении предпочтительнее располагать пациента в т.н. «полубоковом» положении, которое обеспечивается использованием валика и поворотом операционного стола (Сигал Е.И., 2001 (рис. 303)). В таком положении возможно выполнение также большинства оперативных вмешательств на легких и плевре. Весомым аргументом в пользу применения такого положения является отсутствие смещения средостения в здоровую сторону и компрессии вентилируемого легкого. Вмешательства на заднем средостении, грудная симпатэктомия могут производится в положении лежа на животе или с подворотом на живот. Создание операционного поля при торакоскопии, как правило, достигается наложением пневмоторакса. У пациентов с пневмотораксом различного происхождения, когда операция выполняется под местной анестезией, имеющийся коллапс легкого целесообразно сохранить, используя герметичные троакары. Исключением Осложнения ВТС Длительный сброс воздуха вследствие несостоятельности аппаратных швов Кровотечение Инфекция Межреберные невриты Диссеминация опухоли при вылущивании периферических образований Общая частота осложнений не превышает 9% и в целом они чрезвычайно редко представляют угрозу для жизни пациента (Yim and Liu 1996). Из перечисленных осложнений специфическим, пожалуй, является межреберный неврит. Во избежание его возникновения разрез кожи необходимо делать прямо в проекции межреберного промежутка, чтобы при выполнении операции исключить компрессию нерва ригидным торакопортом. При соблюдении основных принципов выполнения ВТС, безусловно,
следует учитывать особенности операций при отдельных нозологических формах. Вопросы классификации, этиологии и патогенеза различных Плевриты. Boutine et al. (1990) при анализе 1000 пациентов с плевральными выпотами показал, что в 215 наблюдениях после цитологического исследования плевральной жидкости и игловой биопсии плевры диагноз оставался неясным. В ходе цитологического исследования нередко возникают трудности в дифференциальной диагностике мезотелиом плевры и карциноматозных плевритов, особенно в тех случаях, когда причиной опухолевой диссеминации является аденоркарцинома. Таким образом, 20-25% пациентов с плевральными выпотами неясной этиологии являются потенциальными кандидатами для выполнения ВТС и, несомненно, большинство из них составляют пациенты с рецидивирующими плевритами. Следует подчеркнуть, что показания к ВТС у пациентов с плевральным выпотом следует выставлять только после проведения традиционного обследования с изучением биохимического, цитологического и микробиологического состава плевральной жидкости и игловой биопсии плевры. Для принятия решения о выполнении ВТС непреходящее значение имеет детальная лучевая диагностика с применением рентгенографии и компьютерной томографии (КТ) органов грудной клетки. Достоверная визуализация патологических изменений до выполнения ВТС значительно повышает ее эффективность, позволяет избежать осложнений, связанных с неправильным выбором точек для наложения портов, и, безусловно, дает возможность предвидеть возможность перехода на открытую операцию. При отсутствии выраженных патологических изменений со стороны органов грудной полости (по данным КТ) для биопсии плевры используют видеоторакоскоп с рабочим каналом, а исследование допустимо производить под местным обезболиванием. В ходе ВТС по поводу экссудативных рецидивирующих плевритов производится ревизия плевральной полости, возможно разделение сращений. В зависимости от находок выполняется биопсия париетальной и (или) висцеральной плевры, оценивается состояние лимфоузлов средостения. По результатам срочного гитстологического исследования может быть избрана лечебная тактика. Так при карциноматозном или неспецифическом плеврите может быть выполнен плевродез путем обработки париетальной плевры аргоново-плазменным коагулятором, распылением коллагена или талька. Туберкулезные плевриты не требуют проведения плевродеза и после точной диагностики регрессируют на фоне противотуберкулезной терапии. Современные способы плевродеза в настоящее время позволили практически отказаться от применявшейся ранее плеврэктомии. При гнойных плевритах (эмпиеме плевры) показания к ВТС возникают при разграничении гнойных полостей за счет выпадения фибрина, что существенно затрудняет их санацию. В этом случае ВТС позволяет произвести адекватную обработку плевральной полости и декортикацию легкого с последующим полноценным дренированием. В течение первых 2-3 недель от начала заболевания ВТС санация и декортикация легкого не сопровождаются техническими трудностями и осложнениями. В более поздние сроки эффективность вмешательства значительно снижается, а формирование ригидной полости не позволяет использовать все преимущества видеоторакоскопии. В том случае если при эмпиеме имеется бронхоплевральное сообщение, то наряду с санацией можно предпринять попытку клипирования бронхов, открывающихся в полость эмпиемы, и даже совместить эту процедуру с эндобронхиальной окклюзией. В любом случае такой подход повышает эффективность санации и в большинстве случае приводит к уменьшению размеров остаточной плевральной полости. В других наблюдениях поводом для ВТС у больных с эмпиемой плевры является длительное отсутствие эффекта от традиционного лечения, что заставляет думать о вторичной эмпиеме на фоне распадающейся опухоли легкого, пищевода или грудной стенки, карциноматозного плеврита, нагноившегося хилоторакса и т.д. В таких наблюдениях ВТС ревизия и биопсия из патологического очага позволяет установить точный диагноз и выбрать оптимальную тактику лечения в кратчайшие сроки. Периферические образования в легких - термин собирательный, чаще всего основывается на данных рентгенографии грудной клетки и предполагает наличие одного или нескольких образований в проекции легочных полей. Особый интерес представляют периферические образования, не имеющие клинической симптоматики и выявляемые случайно или при плановой флюорографии. Нозологические формы, при которых возможно наличие периферических образований, хорошо известны и включают: • рак легкого и другие злокачественные опухоли • доброкачественные опухоли легких (гамартома, карциноид, нейрофиброма и т.д.) • метастатические опухоли легких • туберкулома • аспергиллема • лимфома • гранулематоз Вегенера • киста легкого • абсцесс легкого (при отсутствии симптомов и небольших размерах) • очаговая пневмония • секвестрация легкого и другие пороки развития легких • артериовенозные аневризмы • очаговый пневмофиброз (после ТЭЛА, пневмонии, туберкулеза) Одно только перечисление далеко не всех заболеваний, проявлением которых могут быть периферические образования в легком, показывает, что традиционного подхода, когда диагностика ограничивается только лучевыми методами, явно недостаточно. Периферические образования в легких являются проявлением злокачественных опухолей в 40- 62% случаев (Lislington 1991) (из них более 90% составляют первичные, и лишь 10% - метастатические новообразования). В связи с этим цена ошибочной диагностики может быть очень велика, а стало быть, стремление к гистологической верификации диагноза должно стать основой диагностического алгоритма. Традиционные фибробронхоскопии (ФБС) со смывом из бронхов и браш-биопсией с последующим цитологическим исследованием полученного материала имеют небольшое значение. Чрезбронхиальная биопсия имеет высокую чувствительность, но, к сожалению, низкую специфичность. Роль этого исследования снижается по мере уменьшения размеров образования, а также при расположении периферических образований в субплевральных отделах легкого. Чувствительность трансторакальной биопсии для диагностики ПОЛ составляет 77-95%, а специфичность только 14% (Westcott et al. 1991). При этом отсутствие опухолевых клеток в биоптате, отнюдь, не исключает диагноз злокачественной опухоли. Эффективность чрезбронхиальной и трансторакальной биопсий в последние годы повысилась за счет использования для визуализации образований в ходе исследований компьютерной томографии, однако окончательно решить проблему верификации диагноза это нововведение не позволяет. Исходя из этого, значение видеоторакоскопической биопсии для гистологической верификации диагноза трудно переоценить. С этой целью выполняются краевые или клиновидные резекции легких с использованием эндоскопических сшивающих аппаратов, позволяющих прошивать и рассекать легочную ткань одновременно (Ethicon, Autosuture). Ошибки, опасности и осложнения, связанные с применением аппаратных резекций легочной ткани во время ВТС, соответствуют таковым при открытых трансторакальных операциях. Они, как правило, обусловлены прошиванием больших массивов легочной ткани, что приводит к несостоятельности швов и, как следствие, недостаточному аэрогемостазу или нарушениям вентиляции оставшихся участков легочной ткани. Так, Mack et al. (1993) в исследовании, включавшем 242 пациента, показали, что ВТС атипичная резекция участка легкого с патологическим образованием позволила установить окончательный гистологический диагноз в 100% наблюдений. В ходе ВТС необходимо использовать возможности инструментальной пальпации, кроме того, смещение легочной ткани к отверстиям в местах наложения портов в большинстве случаев позволяет произвести и пальцевую оценку размеров и консистенции патологического образования. Разумеется, что при достаточно центральном расположении патологического очага при ВТС не всегда удается выполнить необходимую ревизию и атипичную резекцию легочной ткани. В этих случаях можно рекомендовать игловую или щипковую биопсию образования под ВТС контролем с определением дальнейшей тактики по результатам срочного гистологического исследования. Иногда при доброкачественном характере процесса можно ограничиться пневмотомией и вылущиванием образования, например при гамартоме. Ложе удаленного образования в таких случаях обрабатывается расфокусированным лучом лазера или аргоново-плазменным коагулятором. При размерах образования менее 5 мм поиск его значительно затруднен. Не останавливаясь на деталях лучевой диагностики периферических образований, следует еще раз подчеркнуть, что определение показаний к ВТС требует всестороннего обследования пациента с использованием рентгенографии, современных модификаций КТ, а в зависимости от показаний магнитно-резонансной или позитронно-эмиссионной томографии. Наличие в арсенале торакальной клиники видеоторакоскопии не является поводом для отказа от традиционных методик верификации периферических образований в легких. Диссеминированные процессы в легких. Существует более 100 нозологических форм, рентгенологическая картина которых характеризуется диссеминированным процессом в легочной ткани. У большинства больных диагноз устанавливается в результате комплексного обследования, включающего данные современной лучевой диагностики, фибробронхоскопии и бронхоальвеолярного лаважа, чрезбронхиальной и трансторакальной биопсии. В начале 80-х годов только одна треть больных нуждалась в выполнении открытой биопсии легкого, т.к. другие методы не позволяли достоверно верифицировать диагноз (Gaensler et al. 1980). Противопоказаниями к выполнению открытой биопсии считались зависимость от кислорода и, следовательно, высокий риск проведения ИВЛ в условиях общей анестезии. В настоящее время можно с уверенностью сказать, что ВТС с широкими возможностями биопсии легочной ткани пришла на смену открытой биопсии легкого. Большим преимуществом ВТС является возможность ревизии всей плевральной полости, париетальной и висцеральной плевры, лимфоузлов средостения, что, в частности, особенно важно при саркоидозе, туберкулезе и лимфопролиферативных заболеваниях. Возможность записи хода операции в сложных случаях позволяет привлечь к обсуждению выявленных изменений патоморфологов, пульмонологов и других смежных специалистов. Стадирование рака легкого, молочной железы, пищевода. Возможности ВТС для оценки распространенности опухолевого процесса органов грудной полости и степени поражения медиастинальиых лимфатических узлов трудно переоценить. При раке легкого оценивается состояние висцеральной и париетальной плевры, перикарда. Для оценки поражения лимфатических узлов средостения необходимо широкое рассечение медиастинальной плевры паратрахеально кзади от полой вены до уровня впадения подключичных вен, спереди и сзади от корня легкого и в проекции пищевода после разделения нижней легочной связки. ВТС позволяет безопасно выполнить биопсию измененных лимфоузлов. Надежными анатомическими ориентирами при ревизии средостения являются полые и непарная вена, аорта и легочные сосуды, внутренняя грудная артерия, диафрагмальный и блуждающие нервы, Asamura et al. (1997) привели результаты стадирования при раке легкого у 116 пациентов, при этом оказалось, что в 6% наблюдений в результате ВТС была подтверждена неоперабельность вследствие карциноматозного плеврита, диссеминации опухолевого процесса и поражения лимфоузлов средостения с инвазией процесса в прилежащие ткани. Для стадирования рака пищевода во время ВТС оцениваются те же группы лимфоузлов, что и при раке легкого. Выбор стороны видеоторакоскопической операции определяется уровнем поражения пищевода. При раке молочной железы ВТС имеет большое значение для оценки состояния внутренних лимфатических узлов молочной железы, расположенных в эндоторакальной фасции и межреберных пространствах вдоль края грудины. В случае выполнения радикальной операции ВТС дает хорошие возможности лимфодиссекции из этой зоны без выполнения торако-или медиастинотомии. Перикардиты. Рецидивирующие экссудативные перикардиты, неподдающиеся консервативному лечению, также могут быть поводом для определения показаний к выполнению ВТС. Истинную причину развития рецидивирующего экссудативного перикардита установить сложно, однако следует помнить о таких факторах как вирусная инфекция, туберкулез, «холодовое» повреждение перикарда при проведении кардиоплегии в ходе операций на открытом сердце. Карциноматозный перикардит чаще возникает как осложнение основного онкологического заболевания и диагностика его не вызывает особых затруднений, однако случаи когда это заболевание диагностируется как первичное не так уж и редки. Основным методом лечения при экссудативных перикардитах является фенестрация перикарда. Предпочтительнее выполнение это
|
||||||||||||||||
|
Последнее изменение этой страницы: 2017-01-26; просмотров: 445; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.221.160.29 (0.022 с.) |

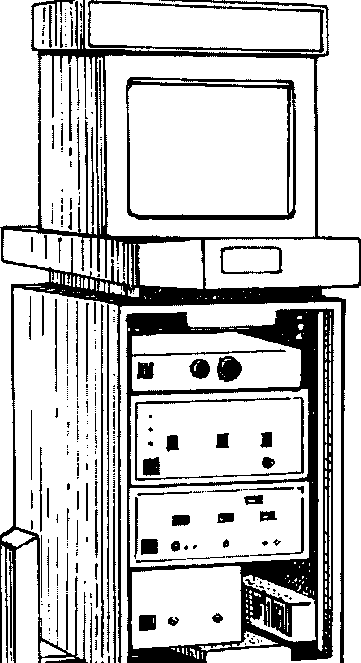
 Рис. 300. Использование двухпросветной интубаци- онной трубки для искусственной вентиляции легких при выполнении видеоторакоскопических оперативных вмешательств на органах грудной полости
Рис. 300. Использование двухпросветной интубаци- онной трубки для искусственной вентиляции легких при выполнении видеоторакоскопических оперативных вмешательств на органах грудной полости
 Рис. 301. Использование однопросветной интубационной трубки в сочетании с окклюзией главного бронха катетером Фогарти :для искусственной вентиляции легких при выполнении видеоторакоскопических оперативных вмешательств на органах грудной полости
Рис. 301. Использование однопросветной интубационной трубки в сочетании с окклюзией главного бронха катетером Фогарти :для искусственной вентиляции легких при выполнении видеоторакоскопических оперативных вмешательств на органах грудной полости
 тивных вмешательств на органах грудной полости (вид сверху).
тивных вмешательств на органах грудной полости (вид сверху).
 Рис. 303. Переднебоковое положение больного на операционном столе при выполнении видеоторакоскопических оперативных вмешательств на органах грудной полости (по Е.И.Сигалу)
Рис. 303. Переднебоковое положение больного на операционном столе при выполнении видеоторакоскопических оперативных вмешательств на органах грудной полости (по Е.И.Сигалу)
 Рис. 304. Места введения торакопортов (троакаров) для проведения оптического инструмента и устройств, обеспечивающих выполнение хирургических манипуляций на органах грудной полости
Рис. 304. Места введения торакопортов (троакаров) для проведения оптического инструмента и устройств, обеспечивающих выполнение хирургических манипуляций на органах грудной полости



