Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Клиническая физиология легких
Легкие, плевра - анатомические образования, находящиеся в составе одного органа или примыкающие к нему и определяющие его функционирование. Структурные особенности легких позволяют выделять в зтом органе три функциональые зоны. По одной из них, воздухопроводной зоне, осуществляется движения газов из окружающей человека газовой среды к дыхательной, альвеоло- капиллярной диффузионной (АКД) мембране легких и от нее. Эта зона составляет часть воздухопроводящих путей, начинающихся в носу (или во рту) и представлена в основном бронхиальным деревом с окружающей его стромой. В респираторной зоне легких происходит процесс газообмена через дыхательную мембрану. Она содержит как воздухоносные пути, так и АКД мембрану. Деление легких на две зоны во многом определяет особенности их органного обмена и патологии. Кроме того, следует отметить плевральную или плевропульмональную щель, состояние которой во многом определяет функционирование каждой из предыдущих зон за счет колебания так называемого внутриплеврального давления (Гриппи М.А., 2001) и других градиентов давления по отношению к респираторной зоне и внешней газовой среде (рис. 93). Газообменная функция легких. Легочный газообмен - важнейшая жизненно важная функция, через которую организм человека тесно связан с внешней средой. Выделяя газообмен как специфическую функцию легких, понимают, что она возможна благодаря процессам обновления газа над АКД мембраной, диффузии газов в кровь и перфузии легких кровью. АКД мембрана покрывает громадное число конечных структурно-функциональных элементов, воздухоносные пространства которых представляют первичную легочную дольку - ацинус. Это По аналогии с другими структурно- функциональными элементами паренхиматозных органов этому элементу было дано название "респирон" (Шанин Ю.Н., Костюченко AJL, 1969). Выделение респирона облегчает понимание физиологии легких и основано на следующих особенностях этого структурно-функционального элемента:
1) клеточное строение респирона резко отличается от выстилки бронхиального дерева и обладает рядом уникальных особенностей; 2) респирон имеет собственный значительный объем воздухоносного пространства (одни альвеолярные ходы занимают более 30% общего объема легких); 3) обмен газов над легочной АКД мембраной происходит не смешиванием и вытеснением (конвекцией), за счет диффузии из дыхательных бронхиол и альволярных ходов; 4) респирон снабжается кровью только из легочной артерии, а соединение между большим и малым кругом кровообращения находится за пределами респираторной зоны легких; 5) респирон практически лишен иннервации, так как эффекторные нервные окончания простираются не далее дыхательной бронхиолы и сопутствующей ей артериолы. Функция респиронов заключается в артериализации крови капилляров малого круга кровообращения, т.е. в насыщении ее кислородом и освобождении от двуокисо углерода. Для этого необходимы несколько условий, среди котрых следует выделить: - вентиляцию легких газовой смесью с достаточно высоким содержанием 02 и малым парциальным давлением С02; - возможность облегченной диффузии через АКД мембрану; - достаточное кровонаполнение и эффективный кровоток через капилляры малого круга кровообращения. В легочном газообмене выделяют внешнее дыхание, или собственно вентиляцию легких, и обмен газов через АКД мембрану. Вентиляция легких обеспечивается системой внешнего дыхания, включающую регуляторный элемент (от корковых нейронов до генома и многих гуморальных факторов), воздухопроводящие пути и альвеоло-капиллярный комплекс, костно-хрящевой каркас грудной клетки с выстилающей его плеврой, дыхательную мускулатуру, малый круг кровообращения. Взаимодействие элементов системы внешнего дыхания приводит к ритмичным изменениям в объеме грудной клетки, что вызывает перемещение дыхательной газовой смеси до уровня респиронов и обратно: - "вдох - дыхательная пауза - выдох". Полезный приспособительный результат системы внешнего дыхания трехзначный: Ра02= 94-96мм.рт.ст., РаС02=39-41 мм.рт.ст., рНа=7,39-7,41.
Действие дыхательных мышц. В физиологических условиях система внешнего дыхания выводится из равновесия в фазе вдоха сокращением дыхательной мускулатуры, побуждаемой регуляторным элементом. Объем грудной клетки увеличивается вследствие опускания диафрагмы и подъема ребер. На изменение объема грудной клетки оказывают влияние изгиб позвоночника и Главной дыхательной мышцей является диафрагма. Сокращаясь, она смещается в сторону брюшной полости, что увеличивает объем грудной клетки в вертикальном направлении и расширяет ее нижнюю апертуру. Расширение нижней апертуры объясняется куполообразной формой диафрагмы; мышечные волокна, которой начинаются от ее сухожильного центра и прикрепляются к нижним ребрам. Именно поэтому сокращение диафрагмы, смещая сухожильный центр книзу, одновременно поднимает нижние ребра. В биомеханике дыхательного акта в целом, кроме ритмичного сокращения диафрагмы, существенную роль играет постоянная тоническая активность ее мышечной части в течение выдоха. Если сокращение обеих куполов диафрагмы определяет величину нарастания отрицательного давления в замкнутой полости плевры (Ppl) и растяжение податливого легкого, то ее тоническая активность противодействует силам выдоха, в результате чего чередование колебаний Ppl происходит плавно. Увеличение объема грудной клетки за счет сокращения диафрагмы обеспечивает более 2/3 жизненной емкости легких (ЖЕЛ). Поэтому уменьшение экскурсий диафрагмы, вследствие повреждения или пареза диафрагмального нерва, возрастание внутрибрюшного давления (при метеоризме, асците и др.) резко сказывается на вентиляции легких, которая в подобной ситуации обеспечивается напряженной работой преимущественно межреберных мышц.. И, наоборот, при выраженной эмфиземе легких, но сохраненной дееспособности диафрагмы наложение пневмоперитонеума восстанавливает ее куполообразную форму и за счет этого улучшает вентиляцию легких. Функцональная роль диафрагмы не ограничивается ее участием в вентиляции легких. Кашель, чихание, рвота, возврат крови из органов живота - вот далеко не полный перечень физиологических актов, в большей или меньшей степени зависящих от сократительной способности диафрагмы. Благодаря ее иннервации из СЗ - С5 дыхательные движения грудной клетки охраняются даже при высоком повреждении спинного мозга. Активность межреберных мышц во время вдоха определяется величиной дыхательного объема (ДО). При возрастании ДО до 80% ЖЕЛ активны все межреберные мышцы. Включение их на вдохе происходит в нисходящем порядке от I до XI (что увеличивает выраженность эффекта диафрагмы), как и выключение к моменту пассивного выдоха. В то же время активный выдох происходит с участием всех межреберных мышц, а выключение происходит в восходящем порядке от XI до I. Нижний отдел грудной клетки сужается раньше верхнего, чему способствует не только тяга тонически активной диафрагмы, но и возрастание напряжения мышц передней стенки живота. Этот же механизм обеспечивает и кашель (Зильбер А.П., 1987).
Кроме основных дыхательных мышц, выделяют вспомогательные дыхательные мышцы вдоха, к которым относят: большую и малую грудные, лестничные, грудинно-ключично-сосковые мышцы. Усиленный выдох формируется за счет работы мышц живота. Вспомогательные дыхательные мышцы принимают участие в дыхании лишь при необходимости значительной гипервентиляции и существенном повышении сопротивления дыханию у больных с патологией легких или грудной клетки. В дыхательной паузе мышцы вдоха практически расслаблены. Возникает состояние равновесия, при котором проявляется действие эластичности системы "грудная клетка - легкие". Эластичные структуры легочной паренхимы стремятся уменьшить объем легких и содержащегося в них воздуха, а эластичные структуры грудной клетки - увеличить их. Эти силы противоположно направлены и в потенциальной полости плевры создают результирующее отрицательное давление РР1, которое притягивает легкое к париетальной плевре и расправляет его. Расправлению легкого способствуют и силы сцепления жидкости в плевральной щели грудной полости, которые исчезают, как только нарушается ее герметичность и в нее попадает воздух. При сокращении основных дыхательных мышц грудной клетки действие сил, растягивающих легкие, соответственно увеличивается. Давление в воздухоносных путях падает, и воздух из атмосферы поступает в легкие по воздухоносным путям, увеличивая объем газа в них (рис. 93). Основное изменение объема внутрилегочной газовой среды зависит от колебания воздухоносных пространств респиронов. Доказано, что при спокойном дыхании объем легочных альвеол не изменяется, однако расширяется вход в них и изменяется их форма (Storey J., Staub Н., 1962). Расправленное состояние альвеол определяется главным образом внутренними факторами, действие которых зависит от состояния АКД мембраны. Однако следует учитывать и состояние воздухопроводящей зоны легких. Во время вдоха трахея удлиняется, увеличивается длина и диаметр бронхов, причем наибольшее удлинение происходит в дистальной части бронхиального дерева. Во время спокойного выдоха объем воздухоносных пространств респиронов уменьшается, размер бронхов возвращаетсящается к исходному. Уменьшению объема бронхиального дерева, составляющего воздухопроводящую зону легкого, при выдохе способствует и укорочение бронхов за счет сокращения их собственных мышц, согласованного с дыханием.
В процессе спонтанной вентиляции, силы, вызывающие изменение объема грудной клетки и легких, преодолевают неэластическое и эластическое сопротивления дыханию, величина которых в конкретной клинической ситуации определяет механику дыхательного акта и особенности вентиляции легких. Общее неэластическое сопротивление дыханию складывается из аэродинамического сопротивления газотоку в дыхательных путях, динамического сопротивления трения всех перемещаемых во время дыхания тканей легких и грудной клетки (именуемое деформационным, вязкостным или фрикционным), а также инерционного сопротивления перемещаемой тканевой массы. Учитывая незначительную величину инерционного сопротивления (обычно не более 5% общего неэластического сопротивления), обычно под незластическим сопротивлением подразумевают сумму азродинамического и фрикционного сопротивлений. Аэродинамическое сопротивление является важнейшей составляющей общего респираторного сопротивления. Оно определяетется как величиной трения между молекулами газовой смеси, движущейся по бронхиальному дереву, так и между молекулами газа и стенкой воздухоносных путей. Оно выявляется как во время вдоха, так и во время выдоха. Фрикционное сопротивление дыханию наибольшего значения достигает при максимальной вентиляции. В конце вдоха и выдоха оно, как и аэродинамическое, равно нулю. Аэродинамическое сопротивление создается главным образом в зоне дыхательных бронхиол, общее сечение которых в 400 раз превышает сечение трахеи. На фоне спокойного дыхания сопротивление воздухоносных путей слегка уменьшается во время вдоха (возможно за счет расширения бронхиол под влиянием тракции легочной паренхимы) и слегка возрастает к концу выдоха. При максимальном форсированном выдохе этот компонент неэластического сопротивления дыханию возрастает значительно. Кроме того, имеет значение состояние мышц бронхов, в регуляции которого в последнее время особое значение придают оксиду азота., вырабатываему эпителием дыхательных путей (Мотавкин П.А., Гельцер Б. И., 1998). Физиологический эффект оксида азота проявляется понижением тонуса гладко мышечных клеток, что приводит к расширению бронхов. Больше всего N0 продуцируется в верхних отделах дыхательных путей, при этом в полости носа образуется до 90% этого газа. Более половины N0, аутоингалируясь расслабляет бронхи на вдохе, регулируя прохождение воздуха в респироны, остальная часть вырабатывается в бронхиальном эпителии. Таким образом, главным регулятором проходимости бронхов являются сами эпителиальные клетки, а их физиологическим раздражителем - сила воздушного потока (Мотавкин П.А., Зуга М.В., 1997). При интубации трахеи, трахеостомии, повреждении зпителия дефицит оксида азота на фоне действия гистамина приводит к усилению тонуса миоцитов, что суженает просвет бронхов (Schendin U. et al., 1995).
Неэластическое сопротивление возрастает при распространенном поражении стромы легких (диффузном легочном фиброзе, перибронхиальном интерстициальном отеке и др.)- Однако больше всего повышает неэластическое сопротивление нарушение бронхиальной проходимости различного генеза, приводящие к сужению просвета бронха, изменению его конфигурации, что увеличивает турбулентность тока дыхательной смеси газов. В крайних случаях обструкции воздухопроводящих путей возникает дистелекатаз, ателектаз, нарушающие легочный этап газообмена. Эластическое сопротивление дыханию. Достаточная эластичность легких и грудной клетки - непременное условие легочного газообмена как при спонтанной, так и при искусственной вентиляции. Эластичность- способность сохранять и восстанавливать прежние форму и размеры системы внешнего дыхания вопреки деформации, которая возникает под воздействием любой внешней силы (сокращение дыхательных мышц, воздействие аппарата ИВЛ, работающего по принципу вдувания, и др.)- Знание динамики вышеописанных сил позволяет врачу понимать положение грудной клетки при различных патологических состояниях: (эмфизема, фиброз легких, ожирение, пневмоторакс, ателектаз) и оценить влияние различных факторов на структуру отдельных элементов системы внешнего дыхания. Эластические свойства этих структур системы детерминирует их эластическое сопротивление к растяжению, что чаще всего определяется через соотношение между объемом и давлением газа в легких, когда обе эти величины сравниваются с состоянием внешнего покоя системы. Это соотношение можно обозначить как растяжимость или податливость грудной клетки и легких. Значение податливости грудной клетки в создании эластического сопротивления дыханию, хотя и меньше, чем значение податливости легких, но все же достаточно существенно, особенно при анормальном состоянии организма человека. Так, при ожирении податливость грудной клетки уменьшается в 2-3 раза. У таких людей существенное значение имеет и значительная инерционность грудной клетки, которую можно не принимать во внимание у худых пациентов. Кроме того, этот функциональный показатель может изменяться под влиянием других факторов, которые в той или иной степени воздействуют на эластичность грудной клетки, например, деформации костно-суставного аппрата грудной клетки, повышение внутрибрюшного давления и другие факторы, затрудняющие экскурсии диафрагмы. Следует подчеркнуть, что податливость легких феноменологически обратно пропорциональна их эластичности. Если легкое теряет свою эластичность (например, при эмфиземе легких), то оно становится более податливым при растяжении. И, наоборот, при хроническом или остром уплотнении легкого (фиброз, воспаление, острое повреждение паренхимы легких другого генеза) оно становится менее податливыми, и это даже определяет все проявления патологии. Понятно, что в силу разных причин величина податливости легких может изменяться и с возрастом. В известной мере она может зависить и от повышения неэластического сопротивления в грудной клетки и легких, что снижает податливость легких при форсированном дыхании у больных с обструктивными нарушениями вентиляции. Растяжимость, или податливость, легких определяется прежде всего состоянием эластических структур респиронов, также плевры, бронхов, кровеносных сосудов, тонусом гладкой мускулатуры бронхов и количеством и качеством бронхиальной слизи, даже при отсутствиии отчетливой бронхообтурации. В трахее и главных бронхах гладкомышечной ткани немного, она находится на задней стенке, замыкая хрящевые полукольца. Начиная с начальных разветвлений бронхиального дерева количество гладких миоцитов увеличивается. В мелких бронхах они образуют сплошной мышечный слой. Мышечные волокна идут в косопоперечном направлении: одни по часовой стрелке, другие - против часовой стрелки, что способствует растяжению бронхов при вдохе. Рефлекторное напряжение бронхиальных мышц при самостоятельном дыхании пропускает столько воздуха, сколько могут вместить легкие при максимальной вентиляции без угрозы их повреждения. Эластичность АКД мембраны только на 1/3 обусловлена эластичными волокнами, оплетающими эту мембрану снаружи от клеточного слоя, образованного альвеолоцитами двух типов. Третий клеточный элемент АКД мембраны - это легочный макрофаг, или "пылевая клетка". Более чем наполовину эластичность паренхимы легких обусловлена стремлением к спадению диффузионной мембраны под действием силы поверхностного натяжения. Стремлению к спадению противодействуют поверхностноактивные вещества легких - сурфактанты, которые постоянно вырабатываются альвеолоцитами II типа (Pattle R., Clement Y, 1957). Они снижают поверхностное натяжение влаги на АКД мембране более чем в 10 раз и поддерживают дыхательную поверхность легких расправленной даже в состоянии апноэ (Сыромятникова Н.В., 1983). Система сурфактантов обеспечивает не только антиателектатическое, но и противоотечное воздействие на легочную паренхиму, практически лишенную интерстициальной ткани, а также стабилизирует форму мелких воздухоносных путей вплоть до терминальных бронхиол (Луценко М.Т., 1994; MacLemP. et al.,1970). Сурфактантная система обуславливает 2/3 эластичности респирона. Остальную часть тяги создают эластические волокона. Толщина пленки поверхностно - активных веществ, покрывающих изнутри АКД мембрану 0,02 - 0,04 мкм. Структура пленки неоднородна и представлена тремя слоями (Scarpelli Е., 1977). Внутренний слой, находящийся на воздушно-гипофазной границе, состоит из слоя фосфолипидов, придающих всей мембране должное поверхностное натяжение. Гипофаза- второй слой - содержит все компоненты сурфактантной системы и служит источником восполнения потерь внутреннего слоя (рис. 94). Третий слой - гипофазно-клеточная граница - состоит из углеводов и является местом секреции иммуноглобулинов (IgA) и некоторых ферментов (фосфолипазы). Альвеолярный воздух В претерминальных и терминальных Воздушно-гипофазная бронхиолах находятся клетки Клара. Они Фосфолипиды___________________ граница являюхся как 5Ы антагонистами альвеолоцитов //Фосфолипиды, коллоиды П, так как выделяют ферменты, которые (альбумин, иммуноглобулин G), Гипофаза - х тг ^ углеводы ^гликоп^еинь!)// действуют на старый сурфактант. Кроме Углеводы, иммуноглобулин, Гипофазно- того, клетки Клара секретируют ферменты клеточная граница ЛИ1Юпротеиды для сурфактанта и ^Ч? Легочная пгюенхима°^? гликозоаминогликаны, определяющие сч ^ ^ г ь ^ - консистенцию и текучесть бронхиальной слизи. Рис. 94. Сурфактантная система легких „ л Дефицит поверхностно-активных веществ вследствие распространенного повреждения сурфактантной системы резко изменяет механические свойства легких, нарушая газообмен при спонтанном дыхании и даже при ИВЛ. Эти повреждения могут возникать вследствие прямого повреждения легкого (при травме, инфекции и пр.), а также в результате расстройств микроциркуляции и метаболизма в респираторной зоне. Гиповолемия и гипоциркуляция любого происхождения, эмболия легочной артерии, в том числе и трансфузионная, связанная с поступлением микросвертков иинородных частиц, отек легких замедляют репродукцию сурфактантов и способствовуют их разрушению. Этому же способствуют табакокурение, длительное вдыхание газовой смеси с высоким (>60об%) содержанием кислорода, а также воспалительные процессы в легочной паренхиме. Отрицательное влияние на продукцию и распад сурфактантов оказывают ряд факторов внутригрудной операции и анестезии. Прекращение кровоснабжения и вентиляции отдельных участков легких, травматизация паренхимы легкого при его выделении, чрезмерное растяжение легких при длительном раздувании снижают активность сурфактантов. В коллабированном легком их синтез падает, что может привести к усилению процессов атектазирования в послеоперационном периоде (Карнаухов И.Ф. и др., 1970). Жирорастворимые анестетики (фторотан, метоксифлуран) уменьшают активность легочных сурфактантов и увеличивают поверхностное натяжение не только на поверхности диффузионной мембраны, но и бронхиального секрета (Scarpelli Е., 1977). Даже небольшое количество жидкости, появляющееся по тем или иным причинам на поверхности АКД или в терминальных бронхиолах, блокирует сурфактантную систему, что быстро повышает поверхностное натяжение со спадением части респиронов, что опытный специалист сразу замечает по изменению податливости легких на мониторе современного аппарата ИВЛ или по тактильному ощущению при ручной ИВЛ. Статические и динамические легочные объемы. При спокойном вдохе поступившего в воздухоносные пути количество воздуха обычно не превышает объема, при котором эластические структуры грудной клетки полностью расслаблены. Объем максимального вдоха определяется взаимодействием между усилиями дыхательных мышц и противоположно направленной тягой легких и грудной клетки, где ведущим является эластическое сопротивление легких. Уровень максимального выдоха ограничивается все возрастающим (по мере уменьшения объема газа в легких) сопротивлением сжатию грудной клетки. Весь объем газа в положении максимально возможного вдоха, так называемую общую емкость легких (ОЕ), разделяют на ряд статических легочных объемов и емкостей, которые можно зафиксировать при проведении классической спирографии (рис. 95)
Дыхательный объем (ДО) - количество воздуха вдыхаемого или выдыхаемого при каждом дыхательном цикле на фоне обычного равномерного дыхания. Резервный объем вдоха (РОвд) - максимальное количество воздуха, которое можно вдохнуть после обычного вдоха. Резервный объем выдоха (РОвыд) - максимальный объем выдоха, который можно выдохнуть после обычного выдоха. Остаточный объем легких (ОО) — количество воздуха, остающееся в легких даже после максимального выдоха. РОвыд и ОО вместе составляют функциональную остаточную емкость (ФОЕ), а часть общей емкости легких, включающая ДО и РОвд принято определять как емкость вдоха (Евд). Наибольшее количество воздуха, которое может быть выдохнуто после максимального вдоха, достигаемого с помощью мышечного усилия, составляет жизненную емкость легких (ЖЕЛ). Важной характеристикой является часть ЖЕЛ, выдыхаемая в первую секунду, так называемая ЖЕЛ1. Величины объемов и емкостей, опредляемые в ходе спирографии, позволяют получить типичные варианты отклонений (паттерны) при функциональном тестировании легких, в частности выделять рестриктивные и обструктивные нарушения (табл. 12). Таблица 12. Типичные паттерны при функциональном тестировании легких.
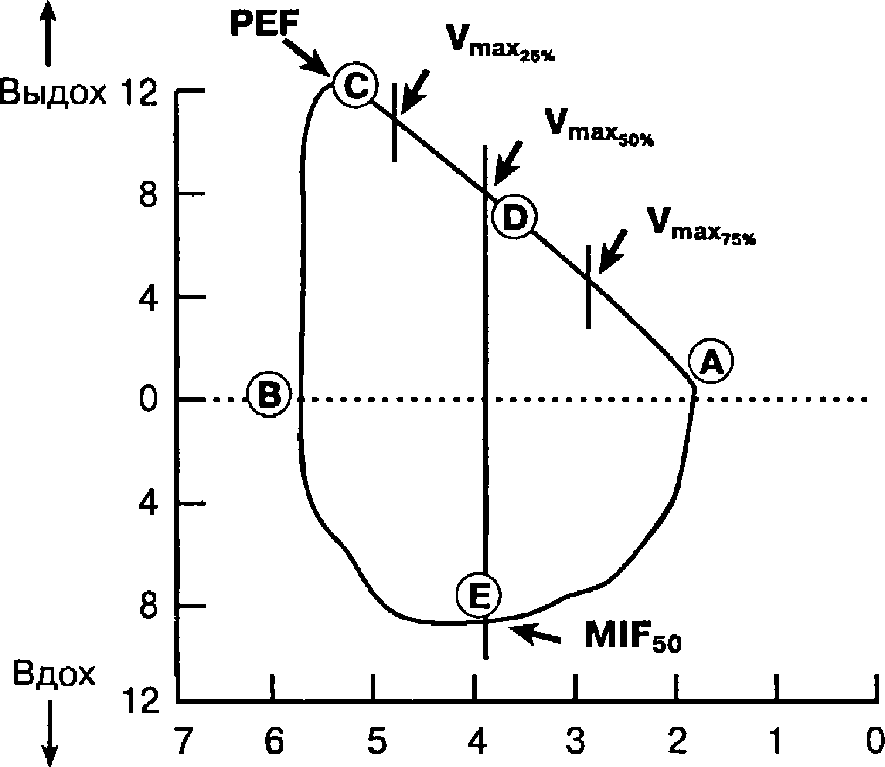
Представленные части объема газа в легких, определяют не только легочные объемы, но и соотношение величин так называемого транпульмонального (Р1) и трансторакального (Prs) давлении и создаваемой ими объемной скорости газотока в воздухопроводящих путях. Эти соотношения практически нелинейны, что прогрессивно увеличивается при возрастании воздушного потока. При форсированном полном вдохе после максимального выдоха транспульмональное давление плавно увеличивается и достигает максимума на высоте вдоха. В то же время поток воздуха, несмотря на продолжающееся увеличение усилия, после вдыхания половины ЖЕЛ начинает прогрессивно снижаться, останавливаясь на высоте полного вдоха. При форсированном выдохе максимальный газоток из легких достигается на уровне 70—80% ЖЕЛ на фоне прогрессирующего прироста давления. После достижения этого предела газеток снижается и падает до нуля гораздо резче, чем при вдохе. Уменьшение потока газа при одновременном нарастании давления указывает на увеличение сопротивления газотоку. В результате величина транспульмонального давления во время выдоха относительно больше, чем во время вдоха. Такое изменение объемной скорости газотока во время форсированного выдоха, несмотря на увеличение транспульмонального давления, свидельствует об изменении механических свойств легких на выдохе. На высоте форсированного вдоха в связи с падением внутриплеврального давления разивается градиент давления в воздухопроводящих путях по направлению от рта к респиронам. Поскольку наибольшее отрицательное давление создается в респираторной зоне легких, то в воздухоносной зоне трансторакальное давление будет тем больше, чем больше калибр бронха, в результате чего и происходит расширение воздухопроводящих путей, наиболее выраженное в их проксимальном отделе. Во время же форсированного выдоха внутриплевральное давление становится положительным, а давление в респираторной зоне - наибольшим. Трансторакальное давление по ходу воздухопроводящих путей снижается до уровня атмосферного давления в ротовой полости. Следовательно, на протяжении дыхательных путей легких должна быть точка, в которой транспульмопальное давление равно нулю: она называется точкой равных давлении (ТРД). Эта точка делит дыхательные пути на два сегмента, в периферическом сегменте трансторакальное давление положительное, в центральном сегменте В процессе форсированного выдоха ТРД смещается от трахеи к дистальным, периферическим отделам воздухопроводящих путей. Так, после выдоха, равного 50% ЖЕЛ, точка равных давлений находится сразу за долевыми бронхами; после выдоха 75% ЖЕЛ она располагается в бронхах с сечением менее 3 мм, которые легко спадаются на фоне отрицательного давления. Таковы соотношения, лежащие в основе феномена зксираторного закрытия дыхательных путей (ЭЗДП). Любая легочная или внелегочная патология, ведущая к потере эластичности дыхательных путей и ускорению газотока на выдохе, неизбежно усиливает ЭЗДП (Щелкунов B.C. и др., 1980). Существенное значение в возникновении этого феномена во время операции играет режим ИВЛ, характеризующийся укорочением выдоха или созданием активного выдоха. ЭЗДП считается одним из ведущих механизмов развития послеоперационной гипоксемии, резистентной к ингаляции кислорода, что требует специальных подходов при проведении респираторной терапии. В настоящее время классическая спирометрия вытесняется приборами, измеряющими газовый поток на вдохе и выдохе. Эти приборы позволяют проводить измерение объемной скорости дыхательных газов как функции объема легких. Соотношение между этими характеристиками газообмена выражается в виде петли "поток-объем" (рис.96). Хотя петля "поток-объем" содержит в основном ту же информацию, что и спирограмма, наглядность соотношения между потоком и объемом перемещаемого газа позволяет вникнуть в функциональные характеристики как верхних так и нижних воздухопроводящих путей. У пациентов с рестриктивными поражениями петля "объем - поток" выглядит как уменьшенный вариант нормальной, все ее величины снижены. Напротив, при преимущественно обструктивных поражениях изменена и форма петли "объем - поток": понижена пиковая объемная скорость газотока и заметно искажен ее контур, Такое исследование позволяет выявлять и так называемую фиксированную обструкцию и переменную обструкцию воздухопроводящих путей (рис. 97) в зависимости от локализации последней, когда воздухоносные пути и давление в них (Ptr) подвержены или влиянию атмосферного давления трахея (Patm) или преимущественно влиянию внутриплеврального давления - легкие (Ppl).
Многие современные аппараты ИВЛ оснащены устройствами, позволяющими контролировать --- TLS \
Фиксированная обструкция (внутри- или внегрудная)
а
Рис. 97. Петля «поток-объем» при фиксированной или переменной обструкции воздухопроводящих путей: а — фиксированная обструкция; б — переменная внутригрудная обструкция; в — переменная внегрудная обструкция форму петли "поток-объем" по ходу каждого дыхательного цикла, что дает возможность ориентироваться в локализации переменной обструкции. Работа дыхания. Величина этой составляющей легочного газообмена характеризует общее усилие дыхательной мускулатуры, для перемещения дыхательного газа к диффузионой мембране, которое зависит от минутного объема дыхания (МОД). Для понимания достаточности газообменной функции легких важно определение трех сторон работы дыхания: общей механической работы, выполняемой по ходу одного дыхательного акта или в единицу времени; отношения между общим количеством произведенной работы и той ее частью, которая затрачивается на вентиляцию воздухоносных пространств легких; и, наконец, величины потребления кислорода дыхательными мышцами. Общая механическая работа дыхания может расходоваться на преодоление ряда компонентов соответственно характеру имеющегося сопротивления: эластического или рестриктивного, неэластического или обструктивного и инерционного. На преодоление эластического сопротивления в норме приходится 2/3, неэластического сопротивления - 1/3 всей работы дыхания. В случаях ожирения, большой массы груди и живота существенное значение в расходовании энергии начинает играть инерционный компонент. Следует подчеркнуть, что многообразные механизмы регуляции внешнего дыхания обеспечивает оптимальный для конкретного пациента дыхательный объем и частоту дыхания при наименьшем расходовании энергии на вентиляцию. Расстройства регуляции дыхания могут привести к нарушению этого соответствия даже при нормальном состоянии аппарата дыхания. В тех случаях, когда податливость легких уменьшается (при легочном фиброзе, застойных явлениях в легких или при остром легочном повреждении) дыхание становится частым и поверхностным, так как при произвольном углублении вдоха работа по преодолению эластического сопротивления будет резко возрастать. Наоборот, при возрастании неэластического сопротивлений в случаях диффузной обструкции бронхиального дерева дыхание становится медленным и глубоким: учащение дыхания больным приводит к резкому возрастанию затрат энергии на преодоление неэластического сопротивления току воздуха. Соотношение МОД и его части используемой в газообмене (так называемой альвеолярной вентиляции), позволяет определять полезную работу дыхания, которая меняется в зависимости от величины конкретного кислородного запроса организма больного. По мере возрастания вентиляции в логарифмической зависимости возрастает и работа дыхания. Предельное значение общей работы дыхания при максимальном МОД равно 51,6+18 кгм умужчин и 32,2 + 13 кгм у женщин (Кадиев Н.Н., Кузнецова В.К., 1976). У больных с множественной патологией предельные значения работы дыхания У здоровых людей эффективный предел увеличения вентиляции не превышает 60 - 70% максимальновозможной вентиляции легких. Дальнейшее произвольное увеличение вентиляции не обеспечивает дополнительного прироста поступления кислорода в ткани вследствие того, что весь дополнительно поступивший в результате газообмена кислород потребляется только самими дыхательными мышцами, что лимитирует выполнение других физических нагрузок. О потреблении кислорода дыхательными мышцами судят по величине так называемой "кислородной цены дыхания", которая определяется по количеству 02, потребляемого дыхательными мышцами на вентиляцию 1 л МОД. При спокойном дыхании дыхательные мышцы здоровых людей используют лишь 5% общего потребления кислорода организмом, и только при значительной гипервентиляции (более 50 л/мин) потребление 02 дыхательными мышцами возрастает до 20%. Обтурационные нарушения легочного газообмена, ригидность грудной клетки и легких, ограничение подвижности диафрагмы при заболеваниях и повреждениях аппарата дыхания предрасполагают к значительному повышению кислородной цены дыхания: уже при объеме <15-20 л/ мин потребление 02 дыхательными мышцами составляет 25-40% кислородного дебита организма (Levinson Н., Cherniak R., 1968). Высокая кислородная цена дыхания крайне опасна для больного после резекции легкого или при уменьшении диффузионной способности кислорода в связи с послеоперационными легочными осложнениями, так как она ограничивает срочную адаптацию к меняющимся условиям жизнедеятельности, гомеостатическим колебаниям.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-01-26; просмотров: 588; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.17.6.75 (0.055 с.) |
 Рис. 93. Давления и градиенты давлений, создающие поток воздуха в легких
Рис. 93. Давления и градиенты давлений, создающие поток воздуха в легких
 Рис. 95. Изменение объемов легких в различные фазы дыхательного цикла:
ДО — дыхательный объем; РОвд — резервный объем вдоха; РОвьщ— резервный объем выдоха; ОО — остаточный объем; ОЕЛ — общая емкость легких; ЖЕЛ — жизненая емкость легких; Е — емкость вдоха; ФОЕ—функциональная остаточная емкость
ВД
Рис. 95. Изменение объемов легких в различные фазы дыхательного цикла:
ДО — дыхательный объем; РОвд — резервный объем вдоха; РОвьщ— резервный объем выдоха; ОО — остаточный объем; ОЕЛ — общая емкость легких; ЖЕЛ — жизненая емкость легких; Е — емкость вдоха; ФОЕ—функциональная остаточная емкость
ВД