Кинетика односторонних химических реакций второго порядка
Случай 1. Когда в элементарном акте реагируют две одинаковые частицы или когда концентрации исходных веществ А1 и А2 равны:
2А ®продукты или А1+А2 ®продукты.
Запишем выражение для скорости:
1) по закону действующих масс: v = k¢×C 2;
2) из определения скорости реакции: v =  . .
При выводе уравнения константы скорости химической реакции, приравняем полученные выражения, разделим переменные и проинтегрируем, учитывая что  : :
 , ,  , ,  , ,
 , (4.33) , (4.33)
Размерность константы скорости реакции второго порядка – «время -1×концентрация-1». Например: л/(моль×с).
Зависимость концентрации от времени выражается уравнением
 . (4.34) . (4.34)
Кинетическое уравнение для реакции второго порядка, согласно уравнению (1.19) имеет вид:
 (4.35) (4.35)
Откуда следует, что график в координатах  – есть уравнение прямой с тангенсом угла наклона – есть уравнение прямой с тангенсом угла наклона  . .
Период полупревращения для реакции второго порядка равен:
 . (4.36) . (4.36)
Как видно из этого уравнения, период полупревращения для реакции второго порядка обратно пропорционален начальной концентрации реагента.
Случай 2. Концентрации исходных веществ разные:
А1 + А2 ®продукты
Пусть начальные и текущие концентрации веществ  и и  равны соответственно: равны соответственно:
 , ,  , ,  и и  , где , где  - текущее изменение концентрации. - текущее изменение концентрации.
Запишем выражение для скорости:
1) по закону действующих масс
v = k× (с 01– x) (с 02 – x); (4.37)
2) из определения скорости реакции
v =  (4.38) (4.38)
Для нахождения константы скорости химической реакции прировняем уравнения (4.37 и 4.38) друг другу, разделим переменные и проинтегрируем:
 . (4.39) . (4.39)
Как видно из уравнения (4.39), размерность константы скорости реакции второго порядка – «время -1×концентрация-1».
Кинетика односторонних химических реакций третьего порядка
Такие реакции очень редки. Для элементарной реакции третьего порядка 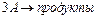 или или  , при одинаковой концентрации исходных веществ, уравнение для скорости на основе формальной кинетики имеет вид: , при одинаковой концентрации исходных веществ, уравнение для скорости на основе формальной кинетики имеет вид:
 . (4.40) . (4.40)
Для скорости реакции на основе общих представлений о скорости справедливо выражение:
 . (4.41) . (4.41)
Отсюда
 (4.42) (4.42)
где 
Разделив переменные в уравнении (4.42) и проинтегрировав его, получим выражение для константы скорости реакции третьего порядка:
 . (4.43) . (4.43)
Размерность константы скорости реакции третьего порядка –  . .
Например: л2/(моль2×с1).
Кинетическое уравнение для реакции третьего порядка, как следует из уравнения (4.43), имеет вид:
 . (4.44) . (4.44)
Подставив в уравнение (4.43) значение с = с 0/2, получим выражение для периода полупревращения
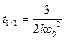 . (4.45) . (4.45)
Из уравнения (4.45) видно, что период полупревращения для реакций третьего порядка обратно пропорционален начальной концентрации реагента во второй степени.
|