
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Свойства гетерогенных катализаторовСодержание книги
Поиск на нашем сайте Скорость гетерогенной каталитической реакции пропорциональна величине поверхности катализатора и характеризуется количеством вещества, образующегося за единицу времени на 1г катализатора. Эта величина называется каталитической активностью катализатора (А): А = v к – v 0(1 – j), (5.61) где v к и v 0 – скорость реакции в присутствии катализатора и без него соответственно; j – доля поверхности катализатора, занятая реагирующими веществами. Часто v 0(1 – j) – мало и поэтому: А = v к. (5.62) Свойства различных катализаторов сравнивают по величине их удельной активности. Каталитическую активность гетерогенного катализатора характеризуют отношением константы скорости или скорости реакции к единице поверхности твердого катализатора:
где Sуд – удельная поверхность катализатора, которая определяется как отношение площади поверхности раздела фаз к одному грамму или единице объема катализатора. Приемы повышения каталитической активности катализаторов Использование в катализе носителей Для борьбы со спеканием катализатора и для экономии дорогостоящих материалов (Pt, Rh и др.) используются носители. Катализатор наносят в виде отдельных, изолированных друг от друга кристаллов, на поверхность пористого или волокнистого материала (носителя). В качестве носителей применяют активированный уголь, силикагель, алюмогель, оксиды металлов и др. пористые материалы. Носитель пропитывают растворами солей металлов (Pt, Ni, Pd), высушивают и обрабатывают водородом при 250-500 0С. При этом металл восстанавливается и в виде коллоидных частиц размером 10-9 м осаждается на поверхности и в порах носителя. Иногда катализатор синтезируют прямо на поверхности носителя, пропитав носитель растворами реагентов, с последующей термической обработкой. Так получают катализаторы с металлфталоцианинами, нанесенными на сажу, графит и др. Использование в катализе промоторов Промоторы – это вещества, которые сами не являются катализаторами, но добавление их к катализатору увеличивает его каталитическую активность. Если промоторы препятствуют рекристаллизации катализатора, то их называют структурирующими промоторами, а процесс их введения в катализатор – промотированием. Количество промотора, вводимое в катализатор, определяют экспериментально, изучая зависимость каталитической активности катализатора от процента промотора, введенного в катализатор. Согласно мультиплетной теории Баландина (см. ниже), промоторы формируют структуру активных центров катализатора. Каталитические яды Каталитическая активность катализатора может резко снижаться, а иногда влияние катализатора полностью подавляется, в присутствии ничтожно малых количеств некоторых веществ, которые называются каталитическими ядами. Типичными ядами некоторых катализаторов гидрирования являются соединения серы (H2S, CS2, тиофен, меркаптаны), сильные кислоты и их соли, соединения фосфора, мышьяка, свинца и др. Примечательно, что практически все они являются ядами и для большинства живых организмов. Характерно, что они обладают кумулятивным действием. Считается, что в большинстве случаев отравление катализатора происходит в результате адсорбции яда на поверхности и блокировки активных центров катализатора. Так как адсорбция может быть как обратимой, так и необратимой, то и отравление может быть соответствующим. Так, платиновый катализатор отравляется СО и СS2, однако, при внесении его в чистую смесь исходных веществ, его активность восстанавливается, при отравлении же H2S и РН3 – платина дезактивируется необратимо. Железный катализатор при пропускании влажного газа теряет свою активность в 5 – 6 раз, но при омывании сухой смесью азота с водородом восстанавливает ее полностью. Количество яда, достаточное для полного прекращения каталитической активности, чаще всего много меньше, чем его необходимо для полного покрытия поверхности монослоем. Это говорит о том, что каталитическая реакция протекает не на всей поверхности катализатора, а только на отдельных ее участках, так называемых «активных центрах». Понятие о роли активных центров общепринято, и основной задачей считается выяснение их природы, а так же механизма элементарной стадии каталитического процесса. Иногда в реакционную смесь специально вводят яды, для того чтобы замедлить процесс протекания побочных процессов. Смешанные катализаторы Эффективность катализаторов на практике часто удается повысить, используя многокомпонентные смеси или смешанные катализаторы. При этом активность смесей может быть значительно выше, чем активность ее отдельных компонентов. Это наблюдается, когда каталитически деятельный компонент проявляет поверхностно-активные свойства в составе смеси. Примером эффективности смешанных катализаторов может служить реакция разложения гипохлорида натрия на хлорид и хлорат натрия в вязком растворе, которая катализируется гидроксидами никеля, меди и железа. Скорость такой реакции в условных единицах составляет 70, 100 и 100 соответственно. При применении смешанного катализатора (70% гидроксида Ni и по 15% гидроксидов Cu и Fe) скорость реакции повышается до 1200 единиц.
|
||
|
Последнее изменение этой страницы: 2016-12-10; просмотров: 823; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.108 (0.006 с.) |

 @
@ 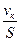 , (5.63)
, (5.63)


