
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Атомно-эмиссионный метод анализаСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Лабораторная работа № 4.1 Определение калия и натрия в минеральных водах методом пламенно-эмиссионной спектрометрии Цель работы:1. Определить массовую долю щелочных металлов в минеральной воде. 2. Получить практические навыки анализа с использованием пламенного анализатора жидкостей. 1. Общие сведения Свойством, что измеряют в методе пламенной спектрометрии, является интенсивность излучения света в атомизированных химических элементах, возбужденных в пламени. Анализируемый раствор сжатым воздухом через распылитель подается как аэрозоль в пламя горелки. В зависимости от состава горючей смеси температура пламени достигает 1800-3100°С. При такой температуре молекулы термически диссоциирует на свободные атомы, возбуждаются и излучают свет. Излучения выделяют оптическим фильтром или монохроматором и направляют на фотоэлемент или фотоэлектронный умножитель, что превращает световой сигнал в электрический. Фототок усиливают и измеряют гальванометром или регистрируют самописцем. Величина фототока пропорциональна интенсивности излучения исследуемого элемента, а следовательно, его концентрации в растворе. 2. Стандартные растворы Их готовят из препаратов квалификации «химически чистый» (хч) или «чистый для анализа» (чда). Раствор А (с массовой концентрацией калия 0,5 г/л): навеска хлорида калия массой (0,93355 ±0,0002) г растворяют в мерной колбе емкостью 1 л, доводят дистиллированной водой до метки и перемешивают. Раствор А (с массовой концентрацией натрия 0,5 г / л): неф-ЖКУ хлорида натрия массой (1,2708 ± 0,0002) г растворяют в ми-рний колбе емкостью 1 л, доводят дистиллированной водой до миф десятки и перемешивают. Спектроскопический буфер для определения калия: готовят насыщенный раствор, добавляя в указанном порядке CaCl2, NaCl и МgCl2. Спектроскопический буфер для определения натрия. Готовят насыщенный раствор смеси солей, растворяя их в таком последовательности: CaCl2, KCl, MgCl2. 3. Подготовка пламенного фотометра к работе 3.1 Подготовить комплект стандартных и рабочих растворов для выполнения данной работы. 3.2 Включить компрессор и установить давление 0,6-0,8 атм. Затем включить горючий газ и отрегулировать давление воздуха, определяется высотой четкого внутреннего конуса пламени сине-зеленого цвета.
3.3 Установить светофильтр, выделяющий излучение ис-джуваного элемента (Na или K). 3.4 Прогреть прибор в течение 30 мин. 3.5 Распиливая дистиллированную воду, установить стрелку амперметра на ноль шкалы. 3.6 Распиливая стандартный раствор с максимальной концент-рации элемента, установить стрелку прибора ручкой «чу-можность» на деление «100». Второй раз проверить нулевое по-жение и максимальный отсчет прибора и, если надо, откоректировать регистрирующее устройство. Растворы для градуировки прибора: в мерные колбы емкостью 100 мл вводят пипеткой 1,0; 2,0; 3,0; 4,0 5 мл соответствующего раствора А, доводят до метки дистиллированной водой и тщательно перемешивают. Полученные растворы содержат 0,5.10-2; 1,0.10-2; 1,5.10-2; 2,0.10-2; 2,5.10-2 г /л соответственно калия или натрия.К 100 мл каждого раствора добавляют по 5 мл спектроскопического буфера для калия или натрия. Измеряют интенсивность излучения для этих растворов, 3-5 раз. Перед каждым измерением промывают распылитель водой. По данным строят градуировачный график в координатах: абсцисса - значения концентраций стандартных растворов (С) ординат- соответствующие показания прибора (А). Масштаб выбираем так, чтобы график проходил через начало координат под углом, близким к 45°. 4. Анализ образца воды Пробы для определения калия и натрия готовят отдельно. Отбирают 100 мл пробы и добавляют 5 мл спектроскопического буфера для калия или натрия, а затем измеряют интенсивность излучения исследуемого раствора. По соответствующему градуировочным графиком, используя данные измерений (А х), находят концентрацию элемента (c х).
4.1.2 Атомно-абсорбционная спектрометрия Метод атомно-абсорбционной спектрометрии основан на поглощении света свободными атомами исследуемого элемента, которые возникают при попадании раствора анализируют, в пламени польника, при резонансной длине волны. Суть метода: свет от спектральной лампы проходит атомизатор спектрофотометра, где частично поглощается свободными атомами и попадает в монохроматор, что выделяет излу-нювання резонансной длины волны. Это излучение преобразуют в электрический сигнал, усиливающие и регистрируют прибор. Метод позволяет определить более 75 элементов с высокой селективностью и низким пределом определения: 10-10-10-12 г. В оптимальной области относительная погрешность составляет 0,5-3%. Зависимость между концентрацией атомов элемента, вы-определяется, и сигналом описывает закон Бугера-Ламберта-Бера:
A = lg (I0 / I) = K0 c l, где А - атомное светопоглощения; I0 - интенсивность аналитической линии в свете, падающем; I - интенсивность аналитической линии в исходном свете; К0 - коэффициент, характеризующий поглощения аналитической линии; c - концентрация элемента анализирующие; l - длина поглощающего слоя в атомизаторе. Удобным и стабильным средством атомизации жидкостных проб является пламени. Используют пламя, температура которого кколеается от 2000 до 3000 К. Распространенной является смесь ацетилен-воздух, с стехиометрическим соотношением топлива и окислителя. Определяя некоторые элементы, используют обогащенное пламя. Например, определить хром возможно только в сильно обогащенном, желтом пламени ацетилен-воздух. Анализируя другие элементы, можно использовать скудное пламя как более высокотемпературный. Пламя динитроксид-ацетилен используют, определяя элементы, образующие термостойкие соединения, например, алюминий, бор, вольфрам, барий и др. Атомно-абсорбционный метод является высокоселективным. Это означает, что исследуемый элемент можно открыть в присутствии других элементов в любых материалах.
Лабораторная работа № 4.2 Атомно-абсорбционные определения Атомно-абсорбционные определения меди, цинка и марганца в соках и водах. Цель работы:1. Ознакомиться с основными составляющими частями метода атомно-абсорбционные спектроскопии. 2. Проанализировать фруктовые соки, или столовые и минеральные воды на примеси тяжелых металлов.
1.Общие сведения Метод основан на измерении абсорбции света свободными атомами меди (цинка, марганца), которые образуются при введениииследованного раствора в пламя смеси ацетилена с воздухом или пропана с воздухом при длине волны 324,7 нм (213,9 нм; 279,5 нм). 2. Аппаратура, реактивы, растворы Атомно-абсорбционной спектрофотометр; Лампа с полым медным (цинковым, марганцевым) като-дом; Ацетилен по ГОСТ 5457-75; Компрессор воздушный; Медь металлическая; Цинк металлический; Марганец; Кислота азотная, хч, по ГОСТ 4461-77; Стандартные растворы с содержанием меди, цинка, марганца 1 г/л; Кислота азотная с массовой долей 1,5%; Пипетки на 1,0; 5,0; 10,0 мл; Мерные колбы на 100 мл; Стеклянные стаканчики. Стандартные растворы для атомно-абсорбционных определений готовят, растворяя металлы или их соли известного состава в кислотах или воде. Из концентрированных стандартных растворов (1 г/л) готовят менее концентрированные, разводя аликвоты азотной кислотой с массовой долей 1,5%. Этим сохраняем стандартные растворы долгое время, потому что подкисление к рН =1 предотвращает гидролиза ионов металлов.
Градуировачные растворы Раствор А: 10 мл раствора, содержащего 1 г/л меди (или цинка или марганца), переносят в мерную колбу на 100 мл, доводят до метки дистиллированной водой с массовой долей HNO3 1,5%, тщательно перемешивая. Массовая концентрация раствора А - 0,1 мг/мл меди (или цинка или марганца). Раствор Б: 1 мл раствора, содержащего 1 г/л меди (или цинка или марганца), переносят в мерную колбу на 100 мл, доводят до метки дистиллированной водой с массовой долей HNO3 1,5%, тщательно перемешивая. Массовая концентрация раствора Б - 0,01 мг/мл меди (или цинка или марганца).
Чтобы построить градуированый график, в 5 мерных колб вместимостью 100 мл вносят соответственно 1,3; 3,0; 5,0; 7,0; 10,0 мл раствора Б, доводят до метки раствором HNO3 с массовой долей 1,5%, тщательно перемешивают. Массовые концентрации этих растворов соответственно 1∙10 -4; 3∙10-4; 5∙10-4; 7∙10-4; 10∙.10-4 г/л меди (или цинка или марганца). Чтобы приготовить раствор с массовой концентрацией ионов металла 30.10-4 г/л, 3 мл раствора А переносят в мерную колбу обьемом 100 мл, доводят до метки раствором HNO3 с массовой долей 1,5%, тщательно перемешивают. Включив лампу с полым медным (или цинковым или марганцевым) катодом на монохроматор атомно-абсорбционной спектрометра выводят аналитическую линию меди (цинка, марганца) 324,7 нм (213,9 нм; 279,5 нм). Измеряют светопоглощения стандартных растворов. Исследование растворы упаривают с 100 мл до 10 мл.
Метод градуировочного графика Считают, что прибор градуированный, если для него установлено функциональная связь между концентрацией анализов ного элемента в стандартных растворах и показаниями прибора. Прибор градуируют после прогрева спектрофотометра течение 30 мин. Стандартные растворы употребляют в порядке роста концентраций, вводят их в огонь и фиксируют показания прибора. Эти операции выполняют со всеми приготовленными растворами, по три раза с каждым, и вычисляют среднее арифметическое трех измерений. Рекомендуем градуировачные измерения осуществлять в начале, в середине и в конце анализа. По полученным данным строят градуировачный график: по оси абсцисс откладывают концентрации стандартных растворов, с i, а по оси ординат - отвечает щие показания прибора, А i. Чтобы определить неизвестную концентрацию, сх, раствор вводят в атомизатор и после 10-15 с регистрируют показания прибора А х. Его откладывают на оси ординат ґрадуювального ґрафика, и на оси абсцисс находят соответствующее значение концентрации, сх, которую определяют. Градуировачный график должен проходить через начало координат и, чтобы отсчет по ним был точнее, под углом, близким к 45°. Конечно, определяя концентрации исследуемого элемента, учитываем, что раствор упаривали, концентрируя его в 10 раз. СПЕКТРОФОТОМЕТРИЯ Спектрофотометрические методы анализа основаны на законе Бугера, который выражают уравнением
где I 0,l, и I 0,l - интенсивность регулярного светового потока, падающего на образец и проходит насквозь соответственно; [ I 0,l] = [ I l] = лм;
Al - светопоглощения, сигнал, измеряют косвенным способом через отношение фотопотоков, пропорциональных в соответствии интенсивности световых потоков (безразмерная величина); с - концентрация вещества, поглощающего свет, [ с ]=моль/л, г/л; l - толщина слоя, поглощающего свет (внутренний размер кюветы в направлении распространения света), [ l ] =см; el - коэффициент поглощения, градуировочная характеристика, которая зависит от природы вещества, поглощающего свет и меняет значение при изменении длины волны излучения, изменении среды (растворителя, агрегатного состояния и т.п.). Если единица измерения [ c ] = моль/л, то el - молярный коэффициент поглощения (МКП) и единица измерения [el]=л/(моль•см). Применяют и удельный коэффициент погл-ния k, с единицей измерения [ k ] = л / (г • см). Закон Бугера оправдывается, если: - Луч монохроматический и плоско параллельный; - Частицы, поглощающие свет, не взаимодействуют между собой и с другими веществами, которые присутствуют в системе. Нарушение этих условий, а также различные виды взаимодействия света с объектами обусловливают разнообразие причин отклонения от закона Бугера. Их разделяют на две группы: инструментальные и физико-химические. В спектрофотометрических анализе сигнал измеряют в условиях, когда инструментальные влияния на светопоглощения постоянные и их можно учесть или исключить, а физико-химические - малые и ими можно пренебречь. Лабораторная работа № 4.3
|
||||||||
|
Последнее изменение этой страницы: 2016-08-01; просмотров: 755; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.135.205.102 (0.014 с.) |

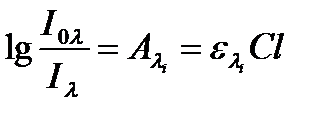 (1)
(1)


