
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Порядок взвешивания на весах типа ВЛР-200.Содержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Внимание! Включать весы следует при закрытых боковых шторках. Ставить объект взвешивания на левую чашу, а гири - на правую. Изменять нагрузку можно только при отключенных весах. Гири следует брать только пинцетом. 1. Включают весы. Через 20-25 сек проверяют положение нулевой отметки. Если отметка «0» не совпадает с отсчетной позицией, то ее корректируют ручкой установки нуля. Выключают весы, поворачивая ручку вверх. 2. Устанавливают взвешивания объект, на левую чашу весов. Пинцетом на правую чашу устанавливают гирю из набора, масса которой ориентировочно близка к массе объекта. 3. Весы включают, постепенно поворачивая ручку так, чтобы только выяснить, какая из чаш перевешивает. Запрещено резко опускать вниз ручку, которая включает весы. 4. Подбирают совокупность гирь, масса которых равна массе объекта или меньше ее на величину, не превышающую 1 г. Для этого гири добавляют (если перевешивает чаша с объектом) или снимают (если перевешивает чаша с гирями). Примечание: в комплекте гирь имеются гири с одинаковой (номинальной) массой, например, 2 г. (их фактические массы несколько отличаются от номинала и друг от друга); чтобы различать такие гири, над числом - массой второго образца гири ставят точку; чтобы при повторном взвешивании воспроизвести предыдущий набор гирь, договариваемся не ставить на чашу гирю «с точкой», если на чаше еще стоит соответствующая гиря «без точки».. 5. Когда масса объекта не превышает массу гири на 1 г, подбирают гири с встроенного гиревого механизма. 6. Если при полном обороте ручки вниз отсчетная отметка находится в пределах оцифрованной шкалы, то с помощью диска делительного устройства доводят ближайшую верхнюю черту шкалы до отсчетной позиции. 7. Регистрируют результат взвешивания и выключают весы. Лабораторная работа № 1.1. ГРАВИМЕТРИЧЕСКОЕ ОПРЕДЕЛЕНИЕ ВОДЫ В (для самостоятельного ознакомления) Цель: 1. Определить массовую долю воды в кристаллогидрате косвенным методом. 2. Получить навыки обоснования условий обезвоживания кристаллогидратов и практические навыки гравиметрических измерений. 1. Общие сведения Методы определения воды разделяют на прямые и косвенные. Прямые методы основаны на соответствующих стехиометрических реакциях, с высокой воспроизводимостью и титровании продуктов или избытка реагента или на измерении массы воды, выделившееся при нагревании и конденсированная или абсорбированная. Большинство реакций, пригодных для определения воды, - это гидролиз реагента с образованием удобного для титрования продукта. Как реагенты пригодны хлорангидриды и ангидрида кислот, альдегиды, кетоны, эфиры, нитрилы, оксиды, карбиды, гидриды металлов. Например: RCOCl + H2O Þ RCOOH + HCl, SO3 + H2O Þ H2SO4 , MO + 2 H2O Þ M(OH)2, MC2 + 2 H2O Þ C2H2 + M(OH)2, MH2 + 2 H2O Þ 2 H2 + M(OH)2. Косвенные методы основаны на потере массы образца при высушивании. Правильность методов зависит от таких условий: — Потеря массы обусловлена только потерей воды; — При определенных условиях выделяется практически вся вода и масса образца становится постоянной. Выбирая условия дегидратации используют термограммы - зависимости потери массы образца от температуры и времени. В качестве примеров, на рис. 4 приведены термограммы кристаллогидратов. Кроме температуры, принимают во внимание возможность химических реакций при нагревании между компонентами анализируемого материала, материалом фильтра и компонентами воздуха (см. рис. 5, примеры термограмм; рост массы соли при нагревании обусловлено следующими реакциями). 2. Подготовка к работе Объектом, в котором определяют кристаллизационную воду, может быть соль неорганических и органических кислот. Исполнитель должен обосновать условия обезвоживания кристаллогидрата, указанный преподавателем, и выбрать осушитель для эксикатора, используя таблицу. 3. Оборудование Бюксы; Ексикатор с осушителем; Шкаф сушильный; Печ муфельная; Щипцы муфельные; Шпателя Весы аналитические (типа ВЛР-200) 4. Ход работы Регулируют температуру сушильного шкафа (или муфельной печи). Если кристалогидрт теряет воду при t > 250 oC, то используют фарфоровые тигли. В чистые, доведенные до постоянной массы (m0), пронумерованы бюксы берут навески кристаллогидрата массой ~ 0,4- 0,6 г на аналитических весах. Записывают массу бюксу с навеской кристаллогидрата m1. Открытый бюкс с навеской кристаллогидрата высушивают в шкафу. Через 1 час. закрытый бюкс (или тигель) охлаждают в эксикаторе в течение 30 мин. в весовой комнате. Взвешивают бюкс с высушенной навеской, масса m2. Повторяют нагрева, охлаждения и взвешивания, достигая того, чтобы два последовательных взвешивания совпали в пределах 0,5 мг. 5. Обработка результатов Результаты взвешивания заносятся в таблицу:
Массовую долю рассчитывают по формуле w(H2O) = 100 % · (m 2 – m 1) / (m 1 – m 0). Результаты, получены несколькими исполнителями в одинаковых условиях, обрабатывают статистически.
Рис. 4. термограммы кристаллогидратов CuSO4.5H2O [2] СaC2O4.H2O [3], Na2HPO4.12H2O [2]
1‑Фильтровальная бумага, 2‑асбест, 3‑оксалат кальция, 4‑сульфат кальция, 5‑хромат серебра, 6‑гидрооксид хрома, осажденный аммиаком, 7‑гидрооксид хрома, осажденный тиосемикарбазидом, 8‑кобальттринитрат цезия, 9‑хромат ртути, 10‑неокупферонат железа, 11‑арсенат серебра, 12‑сульфид сурьмы, 13‑хромат свинца, 14‑сульфид меди, 15‑оксинат магния, 16‑оксалат магния, 17‑вольфрамат оксина, 18‑йодат тория, 19‑фосфат титана, 20‑сульфат бензидина. Таблица 1
|
||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-08-01; просмотров: 1738; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.133.126.241 (0.006 с.) |

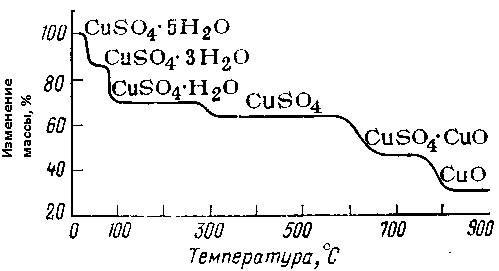

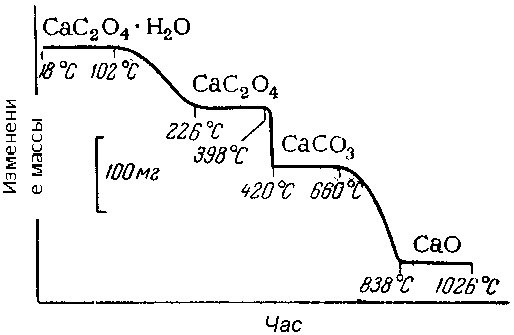
 Рис. 5. Кривые термолиза [4].
Рис. 5. Кривые термолиза [4].


