
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Органические реагенты в неорганическом анализеСодержание книги
Поиск на нашем сайте
Современное развитие аналитической химии обусловлен созданием новых приборов для инструментальных методов. Однако существенной составляющей методов отделения, выявления, определения и концентрировании (осаждением, экстракцией, сорбцией) остаются реакции с соответствующими реагентами. Ведущую роль в качественном анализе (в частности, в капельных методах), в гравиметрии, титриметрии (как индикаторы и титранты), в спектрофотометрии и т.д. играют органические реагенты. Их перспективность связана с яркой окраской многих комплексных соединений, их способностью к флуоресценции, существованием твердых соединений с большой молярной массой, комплексных соединений с преобладанием их растворимости в неводных растворителях над их растворимости в воде. Применение органично аналитических реагентов основали Н. А. Ильинский (1856-1941), применившего a-нитрозо-b-нафтол как реагент для определения кобальта, и Л. А. Чугаев (1873-1922), что в 1905 открыл диметилглиоксим, реагент для обнаружения и определения никеля. Важными для анализа продуктами могут быть как комплексы между аналитом и реагентом, так и новые органично соединения (например, продукты окислительно-восстановительных превращений) или другие формы реагента (для кислотно-основных индикаторов). Органично реагенты содержат определенные функциональные группы, определяющие разнообразие взаимодействия этих реагентов с компонентами, анализируют. Продукты - простые и комплексные соли, внутрикомплексные соединения, продукты окислительно-восстановительных превращений, адсорбции и др. Свойства комплексных соединений (устойчивость, окраска, растворимость и т.д.) Является источником информации о качественном и количественном составе объекта. В состав комплексов входит комплексообразователь (обычно ион или атом металла) и лиганды (ионы или молекулы). Эти составляющие части способны к самостоятельному существованию (правда, ионы металлов в растворе также комплексами с молекулами растворителя как лиганды. Лиганды могут быть анионами или полярными молекулами. Наиболее распространенными неорганическими лигандами есть молекулы H2O и NH3; ионы F‑, Cl‑, Br‑, I‑, CN‑, NO3‑, NO2‑, OH‑, SO42‑, CO32‑, H n PO4(3 n)‑ (n = 0, 1, 2). Органические лиганды - это в основном соединения, имеющие хотя бы на одном из атомов (донорные атоме) неразделенной пару электронов. Донорными зачастую являются атомы неметаллов (в скобках приведены значения электронегативности по Полингу): O (3,5), N (3,0), S(2,5), Se(2,4), Te (2,1), P (2,1), As (2,0), Sb (1,9). Донорные атомы входят в состав функциональных групп, таких как – ОН,
Устойчивость комплексов ионов металлов зависит от их электронной структуры. Ее связывают с ионным потенциалом - отношением заряда иона к его радиуса. Строение электронной оболочки и радиус иона влияют и на стереохимии комплекса. Реакционная способность органично реагента зависит не только от наличия функциональных групп, но и от его структуры. Так, группы без донорных атомов (такие как - СН3) могут помешать, чтобы функциональная группа подошла к комплексообразователю и образовала устойчивую координационную связь. Если у реагента есть несколько функциональных групп, они могут образовывать несколько координационных связей с компонентом,который анализируют. Комплексы, в которых образовалось несколько координационных связей полидентатных лиґанда (то есть способного к координации со многими группами, от латинского dens - зуб, родительный падеж - dentis), называют хелатными (от греческого chele, клешня), или внутрикомплексными. Лиганды с одной функциональной группой является монодентатно («однозубый»). Устойчивость хелатных комплексов гораздо выше, чем простых комплексных соединений с несколькими лигандамы, содержащие по одной соответствующей группе. Такое свойство комплексов с полидентатных лиґандом называют хелатным эффектом.
Устойчивость комплекса с полидентатных лигандом зависит от геометрии цикла, образованного комплексообразователем, одной из функциональных групп, фрагмент лиганды между функциональными группами, второй группой, затем замыкается на том же комплексообразователи. Согласно правилу циклов Чугаева, устойчивым комплексам соответствуют пяти или Шестиатомные цикла. Например, среди диоксипохидних бензола только орто-изомер может образовывать устойчивый пятиатомный цикл, геометрия же мета- и пара-изомеров неблагоприятная для хелатных циклов. Заметим, что и мета-изомер не образует шестиатомного хелатного цикла, так, чтобы образовать Селективность органично реагентов зависит от: 1) компонентов, анализирующие - их положение в периодической системе, строения электронной оболочки и ее размера; 2) скелета его молекулы, различных заместителей; 3) продуктов взаимодействия - их однородности, состав, устойчивости; 4) среды - величины рН, природы растворителя, температуры.
Таблица 2
|
||||||
|
Последнее изменение этой страницы: 2016-08-01; просмотров: 276; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.129.210.35 (0.01 с.) |

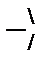 С‑ОН, ‑ СООН, = С = О,
С‑ОН, ‑ СООН, = С = О,  ‑, ‑ NH2, = NH,
‑, ‑ NH2, = NH, 


