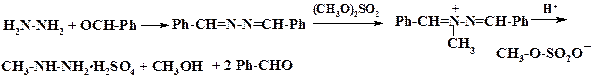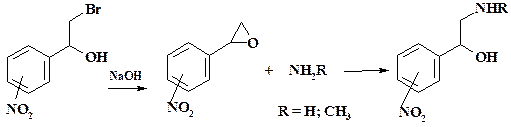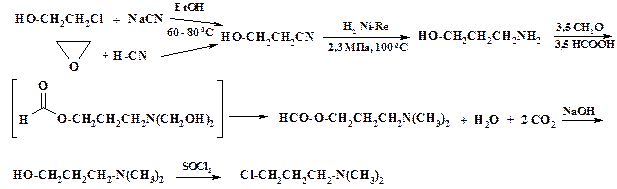Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Селективные методы синтеза вторичных аминовСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Самым простым способом синтеза вторичных аминов является взаимодействие большого избытка амина с алкилирующим агентом, амин в этом случае служит и кислотосвязывающим средством. При этом получают практически индивидуальный продукт. Следует отметить, что алкилирующий агент необходимо прибавлять к амину, чтобы всегда имелся избыток амина. Применение данного метода ограничивается только теми аминами, которые относительно дешевы, или непрореагировавший амин может быть регенерирован. Однако в синтезе лекарственных средств чаще всего для получения вторичных аминов используют селективные методы алкилирования. Первым методом является алкилирование N- алкил(арил)сульфаниламида с последующим гидролизом, который дает индивидуальный вторичный амин:
Для проведения реакции необходима активация NH-группы, которая достигается образованием соли со щелочами. При этом на атоме азота возникает целочисленный отрицательный заряд и его нуклеофильность существенно повышается. Без ионизации NH-группы алкилирование не идет. Способ используют в синтезе анальгина (метамизола натрия), который будет подробно рассмотрен в этом разделе. Вторым методом является алкилирование азометинов или гидразонов. Азометины восстанавливают до вторичных аминов. Восстановление азометинов боргидридом натрия, как это показано на схеме, дает с хорошим выходом вторичные амины. При алкилировании азометинов образуется четвертичная соль:
Четвертичную соль подвергают кислому гидролизу, альдегид экстрагируют и вновь используют. Так получают метилгидразин. При взаимодействии гидразин гидрата с бензальдегидом образуется азин. Его алкилирование в бензоле диметилсульфатом при кипении дает четвертичную соль, которую отфильтровывают. Метилирование второго атома азота исключается, т. к. электронная плотность на нем при образовании четвертичной соли резко уменьшается. Гидролиз соли уксусной кислотой в небольшом количестве воды при кипении дает сульфат метилгидразина. Бензальдегид экстрагируют бензолом и вновь используют. Сульфат метилгидразина выпадает в осадок, и его отфильтровывают.
Данный способ практически не дает отходов, т. к. бензальдегид возвращают на первую стадию. Реакция оксиранов с аммиаком приводит к получению первичного амина, а с первичным амином – вторичных аминов.
В синтезе фенилэфрина оксид м -нитростирола в изопропаноле при температуре 40 – 45 оС с метиламином дает 1-(м -нитрофенил)-2-метиламиноэтанол. В одном из способов синтеза хлорамфеникола (левомицетина) из оксида п -нит-ростирола в метаноле при взаимодействии с аммиаком в аналогичных условиях получают 1-(п -нитрофенил)-2-аминоэтанол (см. раздел 2.1.1). Наглядно видно использование реакций нуклеофильного замещения в синтезе анальгина и хлорпромазина (аминазина). Полный синтез анальгина приведен на схеме. Конденсация ацетоуксусного эфира с фенилгидразином дает антипирин. В его молекуле содержится NH-группа, имеющая кислый характер. Метилированием антипирина в водной щелочи диметилсульфатом получают метилантипирин. Нитрозирование этого продукта рассмотрено в разделе 2.1.2. Восстановление нитрозогруппы смесью сульфита и бисульфита натрия дает производное сульфаминовой кислоты. Наличие в молекуле сильфаниламидной группы позволяет провести монометилирование с помощью диметилсульфата. Однако прямое метилирование невозможно, т. к. электронная плотность на атоме азота низка. Необходима активация иминогруппы. Аналогично метилированию антипирина, производное сульфаминовой кислоты антипирина растворяют в щелочи, на атоме азота сульфаниламидной группы возникает целочисленный отрицательный заряд, его нуклеофильность значительно повышается и метилирование идет уже в мягких условиях. Для удаления защитной группы используют гидролиз в разбавленной серной кислоте. На последней стадии проводят N- сульфометилирование формалином с бисульфитом натрия.
Анальгин является основным болеутоляющим препаратом в РФ и Европе. На его основе выпускается большое количество лекарственных средств, например: пенталгин, седальгин и беналгин. При получении хлорпромазина (аминазин) на последней стадии натриевую соль 2-хлорфенотиазина алкилируют g-хлорпропилдиметиламином:
Однако последний продукт не выпускается промышленностью. Его синтезируют исходя из этиленхлоргидрина или оксида этилена. При взаимодействии первого с цианидом натрия, а также этиленоксида с синильной кислотой образуется этиленциангидрин, его восстановление водородом на никеле Ренея при температуре 100 оС и давлении 2,3 МПа дает g-пропаноламин. В молекуле этого соединения имеются амино- и гидроксигруппа. При алкилировании диметилсульфатом возможно образование O- и N- метильных производных или их смеси. Для селективного синтеза N,N- диметильного производного используют оригинальную методику. Взаимодействие первичного амина с муравьиной кислотой и затем с формалином приводит после обработки щелочью к получению g-пропанолдиметиламина. Формалин является гидроксиметилирующим средством. Муравьиная кислота формилирует гидроксигруппу и восстанавливает гидроксиметильные группы до метильных. При обработке щелочью происходит гидролиз эфира. Пропаноламин отделяют от водно-щелочного раствора и перегоняют.
Конечный продукт синтеза получают кипячением g-диметиламинопропанола в хлористом тиониле.
|
||||
|
Последнее изменение этой страницы: 2016-04-08; просмотров: 1049; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.191.192.250 (0.007 с.) |