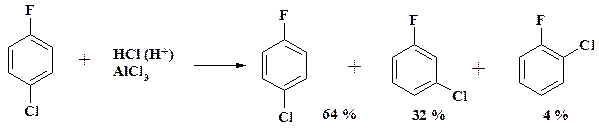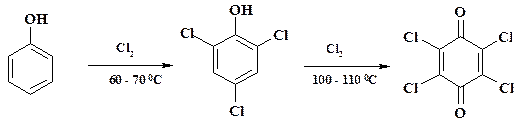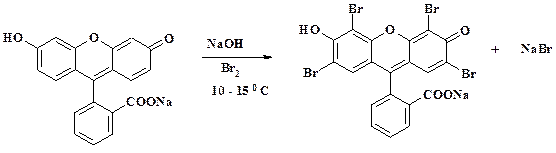Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Хлорирование ароматических соединенийСодержание книги
Поиск на нашем сайте
При хлорировании бензола избытком хлора наряду с хлорбензолом образуются дихлор- и полихлорбензолы. Изомерный состав полихлорбензолов, как видно из приведенной схемы, весьма разнообразен.
При действии активных кислот Льюиса изомеризация облегчается. Для получения индивидуальных соединений очень важен подбор катализатора. Полихлорбензолы служат исходным сырьем в синтезе поли- и перфторпроизводных, которые являются интермедиатами при получении антибиотиков фторхинолонового ряда. Глубокое хлорирование смеси три- и тетрахлорбензолов при температуре 100 оС дает пента- и гексахлорбензол. При обработке п- хлорфторбензола хлороводородом в присутствии хлорида алюминия образуется смесь изомерных продуктов:
В приведенном примере наблюдается смещение только атома хлора, но не фтора, т. к. энергия связи C-F существенно выше, чем связи C-Cl.
В тех случаях, когда необходимо предотвратить образование полихлорпроизводных, применяют такой технологический прием, как обрыв реакции на начальных стадиях процесса. Кинетические кривые приведены на рис. 2.2.
Рис. 2.2. Кинетические кривые реакции хлорирования бензола: 1-кривая расхода бензола во времени от 100 % до 0 %; 2 - кривая образования хлорбензола; 3 - кривая получения дихлорбензолов; 4 – обрыв реакции
Из рис. 2.2 видно, что с увеличением массы хлорбензола начинается образование дихлорбензолов, концентрация хлорбензола снижается. Для того чтобы уменьшить вероятность образования ди- и полихлорбензолов, необходимо оборвать реакцию на начальной стадии. Бензол остается неизрасходованным, примесь дихлорбензолов минимальна. При хлорировании толуола образуется смесь приблизительно равных количеств о- и п- хлортолуолов с примесью дихлорпроизводных. При этом до 70 % толуола не хлорируется и остается в неизмененном виде. Изомеры разделяют дробной кристаллизацией. Исходным продуктом в синтезе мефенаминовой кислоты служит о- хлорбензойная кислота, которую синтезируют из о- хлортолуола. Для синтеза лекарственных препаратов необходимо использовать индивидуальные соединения высокой чистоты. Поэтому 2,4-дихлортолуол, являющийся промежуточным продуктом в производстве аминазина, получают диазотированием 2,4-толуилендиамина и заменой диазониевых групп на хлор (см. раздел 2.4). Конечно, это соединение, синтезированное прямым хлорированием толуола, намного дешевле, однако содержит незначительные примеси других изомеров.
При наличии в ароматическом ядре электроноакцепторного заместителя региоселективность процесса увеличивается, т. к. общая скорость реакции хлорирования уменьшается. В производстве гипотиазида используют м- хлоранилин, который получают из м- нитрохлорбензола. При хлорировании нитробензола образуется в основном м- нитрохлорбензол. Небольшая примесь м- дихлорбензола возникает в результате ипсо -замещения нитрогруппы.
Хлорирование нитробензола одним из наиболее активных хлорирующих реагентов, каким является фторсульфонилгипохлорит, уже при 20 оС приводит к пентахлорнитробензолу. Тетрахлорфталевый ангидрид получают при пропускании хлора в раствор фталевого ангидрида в хлорсульфоновой кислоте при температуре 120 оС в течение 50 ч. В качестве катализатора в этом процессе используют иод.
В производстве гипотензивного препарата клонидин (клофелин) промежуточным продуктом является 2,6-дихлоранилин. При прямом хлорировании анилина образуется сложная смесь соединений. Поэтому для синтеза индивидуального 2,6-дихлоранилина блокируют п -положение анилина введением сульфогруппы, которая выполняет функцию защитной группировки. При хлорировании сульфаниловой кислоты образуется только один продукт – 4-амино-3,5-дихлорбензолсульфокислота, 2,6-дихлоранилин получают с помощью десульфирования.
Вместо сульфаниловой кислоты в качестве исходного продукта может быть использован стрептоцид. Хлорирование в этом случае ведут в соляной кислоте с пероксидом водорода и также удаляют сульфогруппу. В производстве гербицида 2,4-Д (2,4-дихлорфеноксиуксусной кислоты) хлорирование фенола проводят в присутствии воды. Процесс идет при низкой температуре без катализатора, в результате реакции образуется в основном 2,4-дихлорфенол с примесью 2,6-дихлор-, 2,4,6- и 2,4,5-трихлорфенолов.
Целевой продукт отделяют ректификацией, кубовый остаток не находит квалифицированного применения. Однако в конечном продукте – 2,4-Д, содержится незначительное количество трихлорфеноксиуксусных кислот. При использовании этого гербицида на полях под действием ультрафиолета наблюдается его разложение. Из примесей, а также и при утилизации кубового остатка образуется диоксин:
Диоксин чрезвычайно токсичен, вызывает генетические мутации и злокачественные новообразования. Разлив полихлорфенолов может привести к экологической катастрофе. В настоящее время производство данного гербицида запрещено. Применение во время войны во Вьетнаме для борьбы с партизанами agent orange (гербицид сплошного действия, трихлорфеноксиуксусная кислота) привело к гибели джунглей на большой площади. Кроме того, среди военнослужащих США и мирного населения отмечена высокая смертность от онкологических заболеваний и рождение детей с наследственными уродствами. Целенаправленный синтез 2,4,5-трихлорфенола осуществляют с помощью щелочного гидролиза 1,2,4,5-тетрахлорбензола, который очищают от непрореагировавшего тетрахлорбензола, 2,3,5-трихлорфенола и других примесей с помощью перекристаллизации из органических растворителей. Исчерпывающее хлорирование фенола проводят вначале при температуре 60 – 70 оС в расплаве. При этом образуется 2,4,6-трихлорфенол. При дальнейшем хлорировании в смеси хлорсульфоновой и серной кислот образуется мягкий окислитель – хлоранил:
Хлорирование фенола в присутствии хлорного железа при 160 – 180 оС приводит к пентахлорфенолу. В настоящее время его производство из-за экологических последствий применения ограничено. Для получения монохлорфенолов используют другие, более селективные реагенты. Хлорирование ведут хлористым сульфурилом с добавкой хлорного железа. Образуется смесь п- и о- хлорфенолов с преимущественным содержанием п -изомера. Индивидуальные продукты получают разгонкой. Промышленностью в большом объеме выпускается хлорбензол, из которого получают 2-нитро-, 4-нитро- и 2,4-динитрохлорбензолы. Также выпускаются о- и п- хлортолуолы, использующиеся в синтезе соответствующих бензойных кислот и альдегидов. Производство хлорфенолов снижается. В меньшем объеме производят 2,6-дихлоранилин и 3-нитрохлорбензол.
В качестве растворителей и промежуточных продуктов в ряде производств находят применение о- и п- дихлорбензолы, которые образуются наряду с хлорбензолом. Таким образом, для получения лекарственных соединений, где требуется высокая чистота продуктов, использование хлорирования на конечных стадиях производства нерационально в связи с низкой региоселективностью процесса.
Бромирование, иодирование
Если хлорирование широко применяется в промышленности, то бромирование используют только в тех случаях, когда в препарате необходимо иметь атом брома. Это еще в большей степени относится к иодированию. Бром и иод очень дороги, дефицитны и не только в России, но и во всем мире. Основные закономерности бромирования те же, что и хлорирования. Следует учитывать то, что бром менее сильный электрофил, чем хлор. Реакция более селективна (r = - 12), что позволяет использовать ее в производстве 4-бром- о -ксилола, который является промежуточным продуктом в синтезе 4-амино- о -ксилола в одном из методов получения рибофлавина.
Из-за стоимости брома метод дороже, чем производство 3 - и 4-ксилидинов из нитроксилолов при их комплексном использовании для получения рибофлавина и мефенаминовой кислоты. В отсутствие комплексного использования сырья бромирование дает лучшие результаты. Казалось бы, вместо бромирования можно использовать хлорирование, однако при этом образуется сложная смесь соединений, т. к. хлорирующие агенты не обеспечивают селективность процесса. Бромирование о- ксилола ведут при температуре от минус 5 до 0 оС, количество брома составляет 75 % от расчета. Повышение температуры больше 5 оС приводит к образованию примесей дибромксилолов, очистка от которых затруднительна, кроме того, это ведет к перерасходу дорогого брома. Реакционную массу промывают водой, щелочью и водой, бромксилол очищают с помощью вакуумной разгонки. Оригинальный отечественный противовирусный препарат теброфен содержит в своей молекуле четыре атома брома:
При непосредственном контакте теброфена с вирусом наблюдается вирулицидное действие. Препарат применяют в виде мазей для лечения аденовирусного кератита, герпеса и других кожных заболеваний предполагаемой вирусной природы (опоясывающий лишай, простой пузырьковый и рецидивирующий герпес и др.). Бромирование резорцина дает 2,2΄,4,4΄,6-пентабром-1,3-бензохинон. Его нагревание в бромбензоле при 140 – 145 оС приводит к дебромированию и образованию двойной С-С связи между ядрами хинона. При восстановлении последнего соединения дитионитом натрия получают целевой продукт. Синтез красителя эозин, использующегося в гистологии, осуществляют по представленной схеме:
При синтезе препаратов наиболее рационально использовать в качестве исходных полупродуктов бромбензол и бромтолуол. Молекулярный иод является очень слабым электрофилом, поэтому иодируют только высокоактивные субстраты – амины и фенолы. В отсутствие электронодонорных заместителей реакция иодирования не идет, т. к. кислоты Льюиса не активируют молекулу иода, в отличие от хлора и брома. В этом случае иодпроизводные получают через соли диазония. В качестве примера можно рассмотреть препараты тироксин и трииодтиронин. Тироксин – природный гормон щитовидной железы, его применение приводит к повышению потребления кислорода, усиливает энергетические процессы, стимулирует рост и дифференцировку тканей, улучшает функционирование нервной и сосудистой системы, усиливает всасывание глюкозы и ее утилизацию. В больших дозах понижает функцию щитовидной железы. Тироксин получают из высушенных, обезжиренных щитовидных желез убойного скота. Трииодтиронин в 3 – 5 раз более эффективен, его дешевле получать одиннадцатистадийным синтезом. На последней стадии проводят иодирование иодом в слабой соляной кислоте или в уксусной кислоте:
Исходный 3,5-дииодтиронин синтезируют из соответствующего диаминопроизводного (см. раздел 2.4). Производные иода задерживают прохождение рентгеновских лучей, потому при введении препаратов в кровь на рентгеновском снимке получают четкую картину состояния сосудов. Таким образом, иодпроизводные являются рентгеноконтрастными средствами. Синтез одного из препаратов, триомбраста, представлен на схеме. Иодирование 3,5-диаминобензойной кислоты ведут в слабой соляной кислоте иодистым хлором. В отличие от реакции с иодом, использование этого реагента дает максимальную экономию дефицитного и дорогого иода.
Трииоддиаминобензойную кислоту затем ацилируют уксусным ангидридом в обычных условиях.
|
|||||||
|
Последнее изменение этой страницы: 2016-04-08; просмотров: 2869; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.98.43 (0.012 с.) |