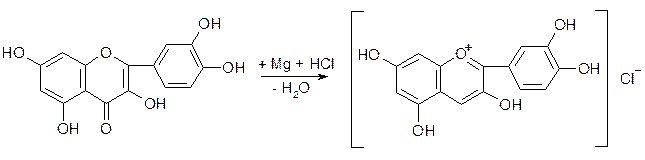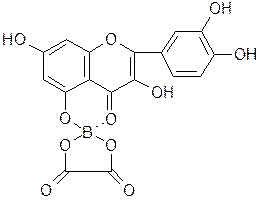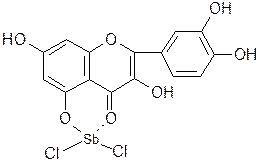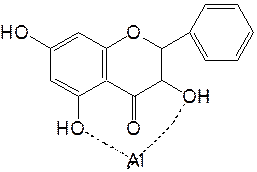Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Методы выделения флавоноидов из лрсСодержание книги
Поиск на нашем сайте
Для флавоноидов не существует универсального метода выделения из растительного сырья. В каждом конкретном случае учитываются свойства выделяемых веществ, сопутствующие вещества и особенности растительного сырья. Для выделения флавоноидов проводят экстрацию ЛРС одним из подходящих растворителей: этанолом, метанолом, горячей водой или спирто-водной смесью. Для очистки и разделения используют: 1) избирательную экстракцию; 2) осаждение солями тяжелых металлов; 3) хроматографические методы. Выделение флавоноидов из ЛРС 1. Экстракция суммы флавоноидов из ЛРС (70%,80% этанолом или метанолом). 2. Отгонка спирта под вакуумом до водного остатка. 3. Очистка полученной суммы флавоноидов СCl4от липофильных веществ. 4. Разделение флавоноидов на фракции растворителями с возрастающей полярностью: 1) экстракция агликонов этиловым эфиром; 2) экстракция моногликозидов этилацетатом; 3) экстракция биозидов, триозидов и др. полярных флавоноидов н-бутанолом. 5. Разделяют полученные фракции с помощью колоночной хроматографии на полиамидном сорбенте, силикагеле или целлюлозе. Элюирование веществ проводят смесью хлороформа с этанолом или спирто-водными смесями с возрастающей концентрацией спирта. Контроль за ходом разделения флавоноидов проводят методом хроматографии: используют ТСХ, БХ или высокоэффективную газожидкостную хроматографию. Наиболее подходящими системами для БХ флавоноидов являются: 15%, 60% РАСТВОРЫ УКСУСНОЙ КИСЛОТЫ; БУТАНОЛ - УКСУСНАЯ КИСЛОТА - ВОДА (4:1:5). Для ТСХ: ХЛОРОФОРМ-МЕТАНОЛ (8:2). 6. Установление структуры выделенных соединений проводят с помощью физико-химических методов: · определение температуры плавления; · определение удельного вращения (гликозидов); · сравнение УФ-, ИК-, масс-, ПМР-спектров со спектрами известных образцов. Схема 9 Качественное определение Для обнаружения флавоноидов в ЛРС используют химические реакции и хроматографию. Химические реакции подразделяются на цветные и реакции осаждения. I. Цветные реакции 1. Специфической реакцией на флавоноиды является цианидиновая проба (проба Шинода), основанная на восстановлении карбонильной группы атомарным водородом в кислой среде в присутствии металлического магния и образовании антоцианидинов. Продукты восстановления флавонов имеют окраску оранжевую, флаванолов, флаванонов - красно-фиолетовую. При использовании цинка положительную реакцию дают флаванолы и флаванол-3-гликозиды, а флаваноны не дают её. Цианидиновую реакцию не дают также изофлавоны, неофлавоноиды, халконы и ауроны. Халконы и ауроны образуют красное окрашивание при добавлении концентрированной хлористоводородной кислоты за счет образования оксониевых солей.
ЦИАНИДИН ХЛОРИД
Цианидиновая реакция по Брианту позволяет определить агликоновую или гликозидную природу исследуемого вещества. К окрашенному раствору продукта цианидиновой реакции прибавляют равный объём н-октанола(или бутанола), разбавляют водой до разделения слоёв и встряхивают. Гликозиды остаются в воде, а агликоны переходят в слой органического растворителя. 2. Реакция со щелочами (аммиаком) - флавоноиды дают различную окраску от желтой до коричневой; халконы и ауроны со щелочами дают красное окрашивание или ярко-желтое; антоцианидины - синее окрашивание. 3. Флавоноиды, благодаря карбонильным и фенольным оксигруппам, способны образовывать комплексы с солями металлов: · с хлоридом окисного железа (III) флавоноиды образуют комплексы, окрашенные в различные цвета в зависимости от структуры (от зеленого до коричневого цвета); · борно-лимонная реакция - 5-оксифлавоны и 5-оксифлавонолы взаимодействуют с борной кислотой в присутствии лимонной (или щавелевой), образуя комплекс ярко-желтого окрашивания с желто-зеленой флуоресценцией в УФ-свете. Если флавонол или флавон не содержит гидроксил в 5 положении, то реакция протекает за счет гидроксила 3 положения;
· реакция с треххлористой сурьмой - 5-оксифлавоны и 5-оксифлавонолы, взаимодействуя с треххлористой сурьмой, образуют комплексные соединения, окрашенные в желтый или красный цвет;
· многие флавоноиды дают окрашенные комплексы желтого цвета с 5% спиртовым раствором алюминия хлорида, с 2% спиртовым раствором циркония хлорида. Флавоноиды, имеющие две оксигруппы у С3 и С5, дают хелаты жёлтого цвета за
счёт образования водородных связей между карбонильной и гидроксильными группами: 4. Флавоноиды со свободной 7-оксигруппой вступают в реакцию с солями диазония, образуя оранжевые или красные продукты азосочетания. II. Реакции осаждения Все флавоноиды с основным ацетатом свинца образуют осадки, окрашенные в ярко-желтый или красный цвет. Средним ацетатом свинца осаждаются лишь флавоноиды, содержащие свободные орто-гидроксильные группы в 3', 4' -положениях кольца В. III. Хроматография Для обнаружения флавоноидов в растительном материале широко используется бумажная и тонкослойная хроматография. Обнаружение флавоноидов на хроматограммах проводят: · по окраске пятен в видимом свете (антоцианы); · по характеру свечения в УФ-свете: флавоны, флавонол-3-О-гликозиды, флаваноны и халконы обнаруживаются в виде темно-коричневых пятен, флавонолы и их 7-О-гликозиды - в виде желтых или желто-зеленых; · по характеру свечения в УФ-свете после проявления 5%-ным спиртовым раствором хлорида алюминия и последующего прогревания хроматограммы при 105°С в течение 2-3 мин: наблюдают пятна флавоноидов с интенсивной желтой и желто-зеленой флуоресценцией. Количественное определение Для количественного определения флавоноидов в растительном сырье наибольшее распространение получили физико- химические методы, прежде всего фотоколориметрия и спектрофотометрия. 1. Фотоколориметрический метод основан: · на цветных реакциях комплексообразования с солями различных металлов (алюминия, циркония, хрома, сурьмы); · на реакции с лимонно-борным реактивом; · на реакции восстановления атомарным водородом в кислой среде в присутствии металлического магния или цинка. 2. Спектрофотометрический метод, основанный на способности флавоноидов поглощать свет в УФ-области спектра. 3. Хромато-спектрофотометрический метод - более совершенный метод количественного определения флавоноидов, используется в сочетании с хроматографией, что позволяет произвести очистку и разделение суммы веществ на отдельные компоненты. Реже используют: 4. Флюориметрический метод. 5. Полярографический метод. 6. Наличие фенольных гидроксилов, обуславливающих слабокислые свойства флавоноидов, позволяет использовать метод кислотно-основного титрования в неводных растворителях: диметилформамиде, диметилсульфоксиде, ацетоне.
|
||||
|
Последнее изменение этой страницы: 2017-02-08; просмотров: 2167; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.135.220.208 (0.008 с.) |