
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Работа 5. Осаждение белков концентрированнойСодержание книги
Поиск на нашем сайте
азотной кислотой (проба Геллера).
Выпадение белка в осадок при действии некоторых минеральных кислот связано с дегидратацией белковых частиц и образованием комплексных солей белка с кислотами. В избытке всех минеральных кислот, за исключением азотной, выпавший осадок белка растворяется. Поэтому реакция осаждения белков азотной кислотой распространена при клинических исследованиях мочи (проба Геллера). Ход работы К 1 мл концентрированной азотной кислоты осторожно по стенке пробирки, наклонив ее под углом 450 так, чтобы обе жидкости сразу не смешивались, наслоить равный объем раствора белка. На границе двух жидкостей образуется осадок в виде белого кольца.
Работа 6. Количественное определение белка в моче по методу Робертса-Стольникова-Брандберга.
В основе метода лежит проба Геллера – денатурация белка азотной кислотой. Экспериментально установлено, что при наслаивании на азотную кислоту, растворы, содержащие 0,0033% белка, дают белое колечко в промежутке между второй и третьей минутами после наслаивания. Если колечко появляется непосредственно после наслаивания раствора белка на азотную кислоту, то путем последовательного разведения исследуемого материала достигают такого максимального разведения, при котором появляется кольцо между второй и третьей минутами. Умножая разведение на 0,0033%, получается процентное содержание белка в моче. Ход работы Заготовить 2 ряда пробирок (по 8 в каждом). Во все пробирки первого ряда прилить по 1 мл концентрированной азотной кислоты. В пробирках второго ряда развести исследуемую мочу методом кратных разведений. Для этого в первую пробирку этого ряда налить по 1 мл исследуемой мочи, во вторую и все последующие - по 1 мл дистиллированной мочи. После перемешивания из второй пробирки перенести 1мл жидкости в третью, затем после перемешивания такой же объем из третей пробирки перенести в четвертую и т.д. до конца ряда. Из последней пробирки 1мл жидкости вылить. Таким образом, получается следующий ряд разведений исследуемой мочи: в первой пробирке моча исходной концентрации, во 2-ой – разведена в 2 раза, в 3-ей – в 4 раза, в 4-ой – в 8 раз, в 5-ой - в 16, в 6-ой - в 32, в 7-ой – в 64, в 8-ой – в 128. После разведения мочи произвести поочередное наслаивание содержимого каждой пробирки на концентрированную азотную кислоту. По секундомеру отметить, в какой пробирке белое кольцо образовалось через 2-3 минуты после начала опыта.
Примерный расчет: Между 2-ой и 3-ей минутами белое кольцо образовалось в 5-ой пробирке, где разведение мочи 1:16. Следовательно, концентрация белка в исходной порции мочи равна: 0,0033% × 16 = 0,05% Эталоны ответов к тестовым заданиям
1.1. – А. – б; Б. – а 1.2.– г (включение пролина вызывает изгиб полипептидной цепи, делая невозможным вращение вокруг связи между a-углеродным атомом и азотом иминогруппы) 2.1. – 1-а, 2-б, 3-в, 4-г; 5-е, 6-ж, 7-д 2.2. – 1-г, 2-в, 3-б, 4-а 3.1. – 4 3.2. – 4 4.1. – Д (- + -) 4.2. – Е (- - -) Эталоны ответов на ситуационные задачи Задача 1. Аминокислотный состав пептида отличается высоким содержанием диаминомонокарбоновых кислот – лизина и аргинина, в то же время, в структуре пептида отсутствуют ароматические и гетероциклические аминокислоты - фенилаланин, тирозин, гистидин и триптофан, дающие положительную ксантопротеиновую реакцию. В частности, тирозин с концентрированной азотной кислотой реагирует по следующей схеме:
Задача 2. В живой клетке процесс укладки синтезируемой полипептидной цепи – фолдинг регулируется особыми белками шаперонами, называемыми также белками теплового шока. Эти белки контролируют формирование стабильной и биологически активной конформации, предотвращая образование из полипептидной цепи неспецифических клубков и агрегатов, а также участвуют в доставке белков к субклеточным мишеням.
|
|||||
|
Последнее изменение этой страницы: 2017-01-24; просмотров: 945; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.6.254 (0.007 с.) |


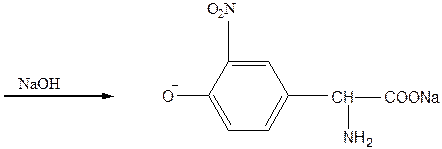 Оранжевая окраска
Оранжевая окраска


