Определение концентрации вещества в растворе.
Содержание книги
- Аналитический сиглан рефрактометрии, прибор на котором его измеряют.
- Аналитический сигнал кондуктометрии.
- Аналитический сигнал нефелометриии и прибор, на котором его снимают.
- Аналитический сигнал полиметрии и прибор на котором его измеряют.
- Аналитический сигнал фотометрии. Приборы фотометрии
- Аналитический сигнал фотометриии.
- В чем Различия между аморфными и кристалическими осадками.
- Вольтамперометрия (индикаторы метода и амперометрическое титрование).
- Монохроматический свет, монохроматизация , монохроматизаторы фотометрии
- Определение концентрации вещества в растворе.
- Декантация- понятие, сущность и пратическое применение
- Естественный и поляризованный луч-их различие, плоскость поляризации и плоскость колебаний.
- Закон Бугера — Ламберта — Бера
- Индикаторы - интервал перехода окраски и РТ-индикатора.
- Индикаторы метода кислотно-основного титрования (интервал перехода окраски и рТ).
- Классификация хроматографического анализа.
- Коэффициент рефракции – смысл ,формула и фактор влияющие на величину рефракции
- Кривые кондуктометрического титрования и их различия.
- Определение точки эквивалентности
- Кривые титрования, их назначение и координаты.
- Методы редоксиметрии. Координаты кривых титрования
- Монохроматический свет, монохроматизация , монохроматизаторы фотометрия
- Направление реакции редоксиметрии
- Основное условие амперометрического титрирования
- Основные операции гравиметрии (методы осождения)
- Относительный показатель преломления, формула и понятие
- Перманганатометрия, рабочий раствор, установленные вещества, индикаторы.
- Переносчик электричества в кондуктометрии
- Полярогррафия.индикаторный электрод.электрод сравнения.полярограмма
- Посуда и аппаратура их назначение в практике гравиметрии
- Прибор для снятия сигнала нефелометрии.
- Рабочие растворы и способы их приготовления.
- Рассчитать T(HCl/CaO);KMnO/Fe
- Редокс-потенциал-понятие, еденица измерения.
- С чем связанна оптическая активность вещества.
- Созревание осадков- понятие и для каких осадков характерно
- Спектр поглощения( определение), графическая зависимость.
- Способы определений концентрации вещества в методах прямых измерений (метод градуировочного графика, молярного вещества, добавок)
- Способы расчета концентрации в рефракции.
- Способы расчета концентрации в фотометрии.
- Стандартный редокс-потенциал.
- Сущность кислотно-основного титрования: реакции, рабочие растворы, установленные вещества, индикаторы и тд.
- Классификация видов хроматографии
- Сущность методы окисления-восстановления.
- Фильтрование и промывание осадка
- Уравнения Ленгмюра. Изотерм адсорбции.
- Условия осаждения амфотерных осадков.
- Формула расчета концентрации в поляриметрии.
- Фотоэлемент – определение (понятие)э
- Фототок — это электрический ток, возникающий в фотоэлементе при воздействии света.
В рефрактометрии используют два способа расчета концентрации вещества в растворе по измеренному показателю преломления.
1. Расчет концентрации по формуле:

Значение фактора показателя преломления берется из рефрактометрических таблиц.
Расчет концентрации по рефрактометрическим таблицам. Измерив показатель преломления, в таблице находят соответствующее ему значение концентрации. Если измеренный показатель преломления в таблице не приведен, проводится интерполирование.
Рефрактометрический метод используется для количественного определения концентрированных растворов.
Концентрированные растворы - это рабочие растворы ЛВ определенной, более высокой концентрации, чем эти растворы прописываются в аптеках.
При приготовлении концентрированных растворов следует избегать концентраций близких к насыщенным, т.к. при понижении температуры раствора возможна кристаллизация растворенного вещества.
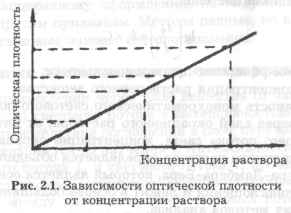
. Графическая зависимость оптической плотности от концентрации
Связь между концентрацией поглощающего раствора и его оптической плотностью lg (I0/I) выражается законом Бера, согласно которому оптическая плотность раствора прямо пропорциональна концентрации растворенного вещества при постоянной толщине слоя:

где к1 — коэффициент пропорциональности;
С — концентрация растворенного вещества.
Зависимость монохроматического светового потока, прошедшего через слой окрашенного раствора, от интенсивности падающего потока света, концентрации окрашенного вещества и толщины раствора определяется объединенным законом Бугера-Ламбера-Бера, который является основным законом светопоглощения и лежит в основе большинства фотометрических методов анализа.

где к — коэффициент светопоглощения, зависящий от природы растворенного вещества, температуры, растворителя и длины волны света.
Если концентрация С выражена в молях на литр, a l — в сантиметрах, то к представляет собой молярный коэффициент светопоглощения и обозначается Ел. Основной закон светопоглощения в этом случае будет иметь следующий вид:

При соблюдении основного закона светопоглощения оптическая плотность раствора прямо пропорциональна молярному коэффициенту светопоглощения, концентрации поглощающего вещества и толщине слоя раствора:

При графическом изображении зависимость оптической плотности от концентрации (при постоянном значении д ) С получается прямая линия. Эта прямая проходит через начало координат при отсутствии поглощения света растворителем и систематических погрешностей (рис. 2.1).
|