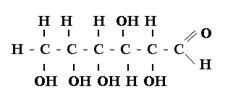Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
В состав лекарственного препарата «Ингалипт» входят эфирные масла.Содержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте Задача №1 1.Какой лекарственный препарат можно изготовить в аптеке при отсутствии в продаже аэрозоля «Ингалипт» (его состав: стрептоцида 0,75; норсульфазола 0,75; тимола 0,015; масла эвкалипта 0,015;формообразующие в-ва до30,0)? · В каких лекарственных формах экстемпоральноro изготовления используются поверхностно активные вещества (ПАВ)? Стрептоцида 0,75 Норсульфазола 0,75 Тимола 0,015 Масла эвкалипта 0,015 Масла мяты 0,015 Этанола 1,8 Сахара 1,5 Глицерина 2,1 Твина-80 0,9 Воды очищенной до 30,0 Азота газообразного 0,3 – 0,42
Поверхностно-активные вещества применяются при изготовлении суспензий, эмульсий, т.е. в гетерогенных лекарственных формах с неустойчивой системой. При отсутствии аэрозоля «Ингалипт», в аптеке можно изготовить суспензию вышеуказанного состава без включения в его состав азота. Суспензию изготавливают по массе, т.к. содержание твердой фазы составляет 10%. Расчеты: Mобщ. = 30,0 m стрептоцида = 0,75 m норсульфазола = 0,75 m тимола = 0,015 m сахара = 1,5 m масла эвкалипта = 0,015 m масла мяты = 0,015 m глицерина = 2,1 m твина-80 = 0,9 V этанола 90% = 1,8: 0,829 = 2,17 V воды очищенной = 30,0 - 0,75 - 0,75 - 0,015 - 1,5 - 0,015 - 0,015 - 2,1 - 0,9 - 1,8 = 22,15 Технология: в ступке измельчают 0,75 стрептоцида с 0,75 норсульфазола. К полученной порошковой смеси добавляют 0,9 твина-80 для получения пульпы. В подставку отмеривают 22,15 мл воды очищенной и растворяют 1,5 сахара. Водным раствором сахара смывают пульпу во флакон для отпуска. Во флакон отвешивают 2,1 глицерина и перемешивают содержимое флакона. В подставку отмеривают 2,17 мл 90% спирта этилового, растворяют 0,015 тимола, 0,015 масла эвкалипта и 0,015 масла мяты, полученный спиртовой раствор переливают во флакон для отпуска и перемешивают содержимое. Приготовленную суспензию оформляют к отпуску. ППК Streptocidi 0,75 Norsulfazoli 0,75 Twini-80 0,9 Aq. purificatae 22,15 ml Sacchari 1,5 Glycerini 2,1 Sp.aethylici 90% 2,17 ml Thymoli 0,015 Ol. Eucalypti 0,015 Ol. Menthae piperitae 0,015 M общ. = 30,0
2.При оценке качества норсульфазола и стрептоцида в образцах нескольких серий внешний вид не не отвечал требованиям по разделу «Описание» - порошки были влажными и желтого цвета. · Дайте обоснование причинам изменения их качества по данному признаку в соответствии с условиями хранения и свойствами. · Приведите комплекс испытаний по характеристике качества норсульфазола и стрептоцида.
StreptocidumSulfanilamidum Sulfanilamide NorsulfazolumSulfathiazolum Sulfathiazole n-аминобензолсульфамид 2-(n-аминобензолсульфамидо)-тиазол
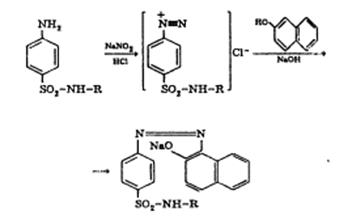
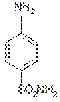
Представляют собой белые или белые со слегка желтоватым оттенком кристаллические порошки без запаха, стрептоцид – мало, норсульфазол – очень мало растворимы в воде, растворимы в спирте, растворимы в растворах минеральных кислот, растворах едких и углекислых щелочей. Tпл.стр.=164-167° Tпл.норс.=198-203° (с разлож) Хранение: в хорошо укупоренной таре. Образцы нескольких серий не отвечали требованиям НД по разделу «Описание» порошки были влажными и жёлтого цвета, т.к. не соблюдались условия хранения – во влажном воздухе отсырели и, обладая восстановительными свойствами за счёт ароматической аминогруппы, окислились до хинонимида и пожелтели. Подлинность: Основана на качественных реакциях на функциональные группы. 1)Реакция, обусловленная ароматической аминогруппой (общие) 1.1 ГФ X реакция образования азокрасителя
азокраситель (вишнёво-красного цвета) 1.2 Реакция конденсации
1.3 Реакция окисления
2)Реакция пиролиза (термического разложения) ГФ X Стрептоцид образует плав фиолетового цвета и выделяется аммиак
Норсульфазол образует плав темно-бурого цвета и ощущается резкий запах сероводорода
Pb(CH3COO)2 + H2S PbS ↓ + 2CH3COOH черный 3)Реакия, обусловленная сульфамидной группой (кислотные свойства, образование комплексных солей). По ГФ X для норсульфазола – реакция отличия: образуется с СuSO4 осадок грязно-фиолетового цвета
Грязно-филетовый осадок
Задача №2 1. Для производства препарата «Адонизид» закуплено лекарственное растительное сырье – горицвета весеннего трава. Результаты полного фармакопейного анализа: внешние признаки и микроскопия соответствуют стандарту, биологическая активность – 60 ЛЕД, влажность – 12%, общая зола – 10%, побуревших частей – 1%, стеблей с бурыми чешуйчатыми листьями – 0,5%, органической примеси – 2%, минеральной – 0,2%. · Сделайте заключение о качестве и возможности дальнейшего использования в производстве полученного ЛРС. Поясните свое решение. · С использованием какой методики была определена биологическая активность сырья? · Приведите кратко методику и поясните все действия. Данное растительное сырьё является качественным и пригодным к дальнейшему использованию для приготовления ЛП, так как в ГФ XI издания приведена статья «Трава горицвета весеннего», в которой указанно: Числовые показатели. Цельное сырье. Биологическая активность 1 г травы должна быть 50-66 ЛЕД или 6,3-8 КЕД; влажность не более 13%; золы общей не более 12%; побуревших частей растения не более 3%; растений со стеблями, имеющими бурые чешуйчатые листья, не более 2%; органической примеси не более 2%; минеральной примеси не более 0,5%. Измельченное сырье. Биологическая активность 1 г сырья должна быть 50-66 ЛЕД или 6,3-8 КЕД; влажность не более 13%; золы общей не более 12%; частиц, не проходящих сквозь сито с отверстиями диаметром 7 мм, не более 10%; частиц, проходящих сквозь сито с отверстиями размером 0,25 мм, не более 10%; органической примеси не более 2%; минеральной примеси не более 0,5%. Активность травы горицвета определяют биологическим методом на лягушках или кошках по сравнению с Государственным стандартным образцом (ГСО) цимарина. Испытание на лягушках. Испытание проводят на травяных лягушках, вводя растворы в лимфатические бедренные мешки (под кожу) или в сердце (в полость желудочка), либо на водяных, вводя растворы в сердце (в полость желудочка) или в вену. Аналитическую пробу сырья измельчают до размера частиц, проходящих сквозь сито с отверстиями диаметром 7 мм, и сушат в сушильном шкафу в течение 2 ч при температуре 40-60°С. Извлечение из травы горицвета готовят в зависимости от способа введения. Для подкожного введения 5 г измельченного и высушенного сырья экстрагируют 110 мл 95% спирта в аппарате Сокслета в течение 6-8 ч. Извлечение собирают в цилиндр вместимостью 100 мл и доводят объем 95% спиртом до метки (1:20).
Для внутрисердечного и внутривенного введения 5 г измельченного и высушенного сырья помещают в колбу с притертой пробкой вместимостью 500 мл, прибавляют 110 мл 75% спирта (по объему) и оставляют на сутки. Затем к колбе присоединяют обратный холодильник, помещают колбу на кипящую водяную баню и экстрагируют в течение 1 ч. Извлечение охлаждают, фильтруют в цилиндр вместимостью 100 мл через четырехслойный фильтр из марли и доводят объем 75% спиртом до метки (1:20). Извлечение пригодно в течение 2 сут со дня приготовления. Стандартный и испытуемый образцы готовят в день опыта. К 2 мл раствора ГСО цимарина 1:3333 прибавляют 6 мл воды (1:4). 20 мл спиртового извлечения (1:20) травы горицвета выпаривают на кипящей водяной бане до 2 мл и доводят объем водой до 20 мл. Образующуюся при этом муть или осадок не отфильтровывают, а прибавляют 1-2 капли 5% раствора натрия гидрокарбоната. Полученное таким путем спиртоводное извлечение (1:20) испытывают на лягушках. Определив наименьшие дозы стандартного и испытуемого образцов, вызывающие систолическую остановку сердца у большинства лягушек (в миллилитрах на массу травяной лягушки или в миллилитрах на 1 г массы водяной лягушки), вычисляют содержание ЛЕД в 1 г травы горицвета. Испытание на кошках. Из измельченной и высушенной травы горицвета готовят настой в соотношении 1,5:200. Для этого 1,5 г травы горицвета помещают в инфундирный аппарат, обливают 200 мл кипящей воды и настаивают в течение 25 мин на водяной бане при 90°С и частом взбалтывании. Затем настой охлаждают, фильтруют, к фильтрату прибавляют 1,8 г натрия хлорида и доводят объем настоя водой до 200 мл. ГСО цимарина разводят в день опыта 0,9% раствором натрия хлорида в соотношении 1:100 000. Устанавливают смертельную дозу настоя в миллилитрах на 1 кг массы кошки (для каждого животного в отдельности) и рассчитывают активность травы горицвета в сравнении с ГСО цимарина или вычисляют содержание КЕД в 1 г травы.(1)
Задача №3 1.При проведении оценки качества калия йодида в образцах одной серии внешний вид не отвечал требованиям НД по разделу «Описание» - порошок был влажным, желтого цвета. · Объясните причины изменения качества по данному показателю в соответствии с условиями хранения и свойствами. · Приведите другие испытания, характеризующие его качество. · Приведите русское, латинское и рациональное название препарата. Охарактеризуйте его физико-химические свойства и их использование для оценки качества. · Предложите реакции идентификации и методы количественного определения. · Напишите уравнения.
Описание: Бесцветные или белые кубические кристаллы или белый мелкокристаллический порошок горько-соленого вкуса, без запаха. Хорошо поглощает воду из влажного воздуха. Легко растворим в воде (1:0,75), спирте (1:12), глицерине (1:2,5). Порошок был влажным, желтого цвета т. к. не соблюдались правила хранения калия йодида. Его хранят в защищенном от света месте, в хорошо укупоренной таре из светонепроницаемого стекла. Реакции идентификации 1. Субстанция дает характерные реакции на ион К+ и I-
2. Реакция с ферумом (III) хлоридом в присутствие хлороформа:
Количественное определение: 1.
2.Йодатометрия, прямое титрование. Титруют раствором калия йодата в присутствие кислоты хлористоводородной до перехода красного окрашивания в желтое. Добавляют хлороформ и титруют до обесцвечивания хлороформного слоя, пересчет ведут на сухое вещество; (S=2):
Задача №4 1.В аналитическую лабораторию фармацевтического предприятия поступили ампулы и флаконы с раствором глюкозы, которые не отвечали требованиям НД по разделу «Описание» - наблюдалось пожелтение раствора. · Как можно объяснить появление этого брака при приготовлении лекарственной формы? · Приведите русское, латинское и рациональное название препарата, охарактеризуйте физико-химические свойства и их использование для оценки качества. · Напишите химическую формулу этого вещества · Предложите методы химической идентификации и количественного определения, напишите уравнения реакций.
На стадии термической стерилизации без добавления стабилизатора происходит деструкция глюкозы, раскрытие цикла и образование ациклической молекулы. Далее идет дегидратация, окисление, изомеризация. Раствор глюкозы приобретает желтую или даже бурую окраску. Поэтому используют стабилизатор Вейбеля, в состав которого входят: натрия хлорид (прокаленный) 0,26 г; 0,1М раствор кислоты хлористоводородной (5 мл на 1 л раствора глюкозы независимо от концентрации). Удобнее пользоваться свежеприготовленным, проанализированным раствором Вейбеля:
натрия хлорид (прокаленный), г…………………………5,2 раствор кислоты хлористоводородной (8,3 %), мл.........4,4 вода для инъекций, л ……………………………………До 1
Добавляют раствора стабилизатора 5 % объема раствора глюкозы независимо от концентрации. Срок годности стабилизатора 1 сут. Предполагают, что натрия хлорид стабилизатора Вейбеля способствует циклизации глюкозы, блокирует альдегидную группу в ациклической активной форме, что препятствует окислению глюкозы. В кислой среде, поддерживаемой хлористоводородной кислотой, замедляются процессы окисления глюкозы. Установлено, что при значении рН раствора глюкозы 3,0 — 4,1 количество 5-окси-метилфурфурола (5-ОМФ) минимально. Важно также уменьшить содержание кислорода в растворителе, заранее прокипятив воду для инъекций.
· Какие другие каналы товародвижения могут быть использованы при доведения товаров от производителей до потребителя? · Из каких элементов складывается отпускная цена производителя? · Как в аптеке будет сформирована розничная цена на данные лекарственные средства? Это косвенный канал, первого уровня. Если есть посредники между производителем и потребителем это косвенные каналы, сколько посредников между производителем и потребителем такого уровня и канал. Чаще используется косвенный канал второго уровня, так как производителям не выгодно работать напрямую с аптеками, из-за небольшого объема закупок. Отпускная цена производителя состоит из себестоимости и прибыли, а прибыль рассчитывается из себестоимости умноженной на рентабельность.
В себестоимость включаются все издержки обращения. • заработную плату персонала, • расходы на сырье и вспомогательные материалы, • расходы на энергию, используемую на технологические цели, • налоги с продаж. • амортизация основных средств, • арендовые и страховые платежи, • коммунальные расходы, • налог на имущество, • ремонтно-эксплутационные расходы.
Розничная цена на лекарственное средство формируется исходя из величины торговых наценок установленных в регионе. Розничная цена на ЛС складывается из оптовой цены посредника и торговой надбавки розничного звена к отпускной цене производителя.
3 .При получении антибиотиков в процессе ферментации в питательной среде возможно избыточное или недостаточное содержание глюкозы · Как в этом случае можно оптимизировать условия ферментации для получения максимального количества целевого продукта? Антибиотики – вторичные вещества, т.е. они не всегда выделяются микробной клеткой. Задача биотехнолога состоит в подборе концентрации питательных веществ в среде таким образом, чтобы не было слишком большого роста биомассы, но антибиотик бы продуцировался в достаточных количествах. Предпочтительным источником углерода является глюкоза. Глюкоза обеспечивает рост гриба, однако подавляет продукцию ферментов, необходимых для синтеза пенициллина. Поэтому обычно стимулируют быстрый рост гриба в первые 30—40 ч, а затем добавляют глюкозу в низкой концентрации либо контролируемыми дозами, либо постоянно (т. е. это периодическое культивирование с добавлением субстрата). Задача №5 1.Обоснуйте требования к глазным лекарственным формам в условиях промышленного производства. · Обоснуйте последовательность и содержание технологических стадий получения глазных капель. · Как обеспечивается стерильность и контролируется этот показатель в сооветствии с требованиями нормативных документов (принципы анализа)? Глазные ЛФ промышленного производства: капли, мази, пленки. Самой распространенной глазной ЛФ являются капли. Основные требования, которым должны соответствовать глазные капли: - стерильность; - отсутствие механических включений; - комфортность (изотоничность, оптимальное значение рН); - химическая стабильность; - пролонгирование действия. Стерильность –это одно из главных требований. Особенно опасна загрязненность глазных капель синегнойной палочкой и золотистым стафилококком. Микробная контаминация обуславливает также нестойкость глазных капель при хранении. Через несколько дней после изготовления в нестерильных глазных каплях обнаруживаются видимые признаки микробной контаминации – муть, плесень, осадок. Стерильность глазных капель достигается такими же методами, как и стерильность растворов для инъекций – приготовлением в асептических условиях и использованием того или иного способа стерилизации. Способ стерилизации глазных капель зависит от устойчивости ЛВ в растворах к температурному воздействию. В связи с этим глазные капли можно разделить на три группы. В 1-ю группу входят глазные капли, которые могут быть простерилизованы паром под давлением в течение 8 – 12 мин без добавления стабилизаторов. Это растворы амидопирина, атропина сульфата, кислоты борной, дикоина, калия йодида, кальция хлорида, натрия хлорида, кислоты никотиновой, пилокарпина гидрохлорида, прозерина, рибофлавина, сульфопиридазин – натрия, фурацилина, цинка сульфата, эфедрина гидрохлорида, а также глазные капли, содержащие рибофлавин в комбинации с кислотой аскорбиновой и глюкозой и др. Во 2-ю группу входят глазные капли с добавлением стабилизаторов, которые могут быть простерилизованы паром под давлением или текучим паром. 3-я группа включает глазные капли, содержащие термолабильные вещества, которые не могут стерилизоваться термическими методами (бензилпенициллин, стрептомицина сульфат, колларгол, протаргол, резорцин и др.). Для стерилизации таких лазных капель может быть использовано фильтрование через микропористые стерильные фильтры. Используются следующие консерванты: хлорбутанола гидрат (0,5%), спирт бензиловый (0,9%), сложные эфиры параоксибензойной кислоты (нипагин и нипазол, 0»%), соли четвертичных аммониевых оснований (бензалкония хлорид, 0)1%), кислота сорбиновая (0,05 – 0,2%). Технология глазных капель. Глазные капли представляют собой водные или масляные растворы, тончайшие суспензии и эмульсии для инстилляции в конъюктивальный мешок. Растворителями служит вода для инъекций, стерильные жирные масла – персиковое, миндальное и парафин жидкий. Особенностями промышленного их производства является применение, кроме антиоксидантов, газовой защиты для легкоокисляющихся веществ (морфина гидрохлорида, натрия сульфацила, кислоты аскорбиновой), совершенствование упаковки (тюбик – капель – капельницы). Растворы в тюбик- капельницах готовятся в помещениях 2–го класса чистоты в условиях асептики. Растворение проводят в реакторах с мешалками, раствор освобождают от механических включений, подвергают стерильному фильтрованию и собирают в стерилизованный аппарат для последующего наполнения тюбик - капельниц. Параллельно с этим изготавливают корпусы и колпачки тюбик – капельниц. Корпус вместимостью 1,5 мл получают на автомате в несколько стадий выдуванием и штамповкой из гранул полиэтилена высокого давления. Колпачки со штырем для прокалывания выливаются под давлением из расплавленных гранул ПЭ низкого давления. После изготовления их промывают водой очищенной, сушат и подвергают газовой стерилизации при 40 – 50ºС смесью этиленоксида и 10% СО2 в течение 2 часов. Этиленоксид удаляют из изделий выдерживанием их в течение 12 часов в стерильном помещении. Далее в асептических условиях в агрегате с избыточным давлением стерильного воздуха происходит навинчивание колпачков на корпус, наполнение его раствором ЛВ с помощью дозирующих насосов и запайка термосвариванием. Наполненные тюбик – капельницы контролируют визуально на отсутствие механических включений на черном и белом фоне освещении электро- лампой в 60 Вт.
2.При проведении оценки качества глазных капель «Р-р сульфацила натрия 20% 10 мл.» в образцах одной серии показатель «Прозрачность и цветность» не отвечал требованиям НД. · Обоснуйте изменение качества раствора по данному показателю. · Напишите формулу действующего вещества. · Приведите русское, латинское и рациональное название и рациональное название. · Охарактеризуйте физико-химические свойства и их использование для оценки качества. · Предложите реакции идентификации и методы количественного определения, напишите уравнения реакций.
На первичные ароматические амины:
Задача №6 Фармацевтическое предприятие для производства экстракта жидкого закупило ЛРС – корневище с корнями валерианы. Сырье представляет собой кусочки корней и корневищ различной формы, проходящие через сито с отверстиями размером 7 мм, светло-коричневого цвета с сильным ароматным запахом и пряным сладковато-горьковатым вкусом. Под микроскопом – клетки паренхимы с крахмальными зернами, эпидерма с каплями эфирного масла, обрывки спиральных и кольчатых сосудов. Числовые показатели соответствуют стандарту. · Сделайте заключение о качестве закупленного ЛРС, поясните. · Какой нормативной документацией руководствуются при проведении анализа? · Какую методику применяют при приготовлении микропрепарата? КОРНЕВИЩА С КОРНЯМИ ВАЛЕРИАНЫ - RHIZOMATA CUM RADICIBUS VALERIANAE Валериана лекарственная - Valeriana officinalis L. Сем. валериановые – Valerianaceae
По ГФ 11: Измельченное сырье. Кусочки корней и корневищ различной формы, светло-коричневого цвета, проходящие сквозь сито с отверстиями диаметром 7 мм. Запах сильный, ароматный. Вкус пряный, сладковато-горьковатый. Микроскопия. На поперечном срезе корня виден эпидермис, клетки которого часто вытянуты в длинные волоски или сосочки. Клетки гиподермы более крупные, часто с каплями эфирного масла. Кора широкая, состоит из однородных округлых паренхимных клеток, заполненных крахмальными зернами, простыми и 2-5-сложными, размером 3-9 (реже до 20) мкм. Эндодерма состоит из клеток с утолщенными радиальными стенками. Молодые корни имеют первичное строение. Старые корни в базальной части имеют вторичное строение с лучистой древесиной.
Кофеин-бензоат натрия
Задача №7 Для производства «Горькой настойки» предприятием закуплена партия ЛРС «Лист вахты трехлистной» массой 2160 кг (нетто), упакованные в тюки из ткани массой 40 кг (нетто). На трех тюках обнаружены следы подтеков. Для подтверждения качества сырья были отобраны пробы и проведен их анализ. · Какой нормативной документацией руководствуются при проведении приемки и испытании проб? · Рассчитайте объем выборки. · Как определяются массы средней и аналитической проб? Что такое метод квартования? ЛИСТЬЯ ВАХТЫ ТРЕХЛИСТНОЙ - FOLIA MENYANTHIDIS TRIFOLIATAE Вахта трехлистная - Menyanthestrifoliata Семейство вахтовые – Menyanthaceae
Заключение о качестве сырья: По ГФ XI– числовые показатели для цельного сырья: суммы флавоноидов в пересчете на рутин не менее 1%; влажность не более 14%; золы общей не более 10%; пожелтевших, почерневших и побуревших листьев не более 5%. При проведении приемки и испытаний проб руководствуются ОФС 420013-03 «Правила приемки лекарственного растительного сырья и методы отбора проб», а анализ проб проводят согласно Государственной фармакопеи XIиздания. Объем выборки рассчитывают для неповрежденных единиц продукции, а три тюка со следами подтеков вскрывают, и отдельно анализируют. Объем выборки рассчитывают по таблице №1.
2160 / 40 = 54 (тюка) объем выборки составляет 10% от транспортных единиц партии, т.е. 6 тюков.
Из каждой вскрытой единицы продукции берут по 3 точечной пробы одинаковые по массе, смешивают их и получают объединенную пробу, из которой методом квартования берут среднюю пробу массой согласно таблице №2 (400,0), которые упаковывают и отправляют в центр по контролю и сертификации лекарств, там её методом квартования делят на 3 аналитические пробы:
по первой (массой 200,0) определяют подлинность, измельченность и содержание примесей;
по второй (массой 25,0) определяют влажность;
по третьей (массой 150,0) определяют зольность и действующие вещества.
Государственная Фармакопея требует определить в листьях трилистника сумму флавоноидов в пересчете на рутин (согласно Государственной фармакопеи XIиздания не менее 1%).
В ОТК фармацевтического предприятия для изготовления таблеток поступило для оценки качества субстанция «Рутин» нескольких серий. В одной серии показания оптической плотности при определении примеси кверцетина превысили регламентируемую норму. · Обоснуйте причины изменения содержания примеси. · Приведите химическую формулу этого вещества, его латинское и рациональное названия. · Перечислите его физико - химические свойства и нормативные показатели, обусловленные этими свойствами. · Предложите методы качественного и количественного определения рутина, напишите уравнения реакции. Rutinum – Рутин
З-Рутинозид кверцетина; 3-рамногликозил-3,5,7,3',4'-пентаоксифлавон
В составе рутина присутствуют химические группы: По химическому строению рутозид является гликозидом. Сахарная часть (дисахарид рутиноза) включаетD-глюкозу иL-рамнозу.Агликон — кверцетин,относится к флаваноидам, содержащимядро хромана (дигидробензпирана) кверцетин 1. фенольные гидроксилы. Описание. Зеленовато-желтый мелкокристаллический порошок без запаха и вкуса. Растворимость. Практически нерастворим в воде, мало растворим в 95% спирте, трудно растворим в кипящем спирте, практически нерастворим в растворах кислот, в эфире,
Анализ Рутина. 1. ИК-спектр должен полностью совпадать со спектром стандарта. 2. УФ-спектр 0,002% раствор препарата в абсолютном спирте имеет max при 259, и 362,5 нм. За счет ароматической системы кверцетина.
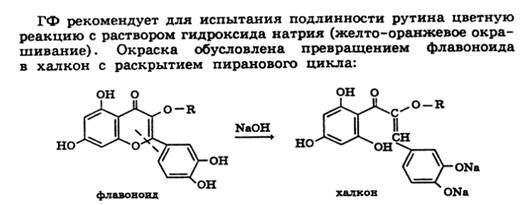
Химические реакции: 1)происходит годролиз гликозидной связи, а затем цветная реакция с раствором гидроксида натрия (желто-оранжевое окрашивание), окраска обусловлена превращением флавоноида в халкон с раскрытием пиранового цикла.
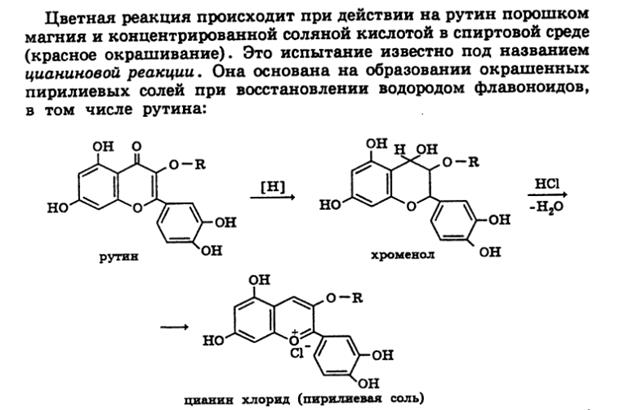
2) Цианиновая реакция происходит при действии на рутин порошком магния и конц. соляной кислоты в спиртовой среде. основана на образовании окрашенных пирилиевых солей при восстановлении водородом флавоноидов, в том числе рутина
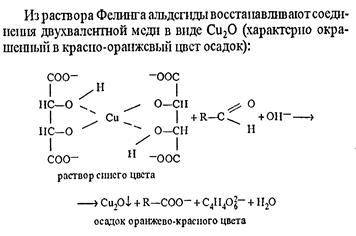
3) сахарная часть (глюкоза) опр-ся с реакт. Фелинга после гидролиза.
Количественное определение: Метод –УФ-спектрофотометрия.
Определяют оптическую плотность раствора на спектрофотометре при длинах волн 375 нм (D1) и 362,5 нм (D2) в кювете с толщиной слоя 1 см. Если отношение D1/D2 находится в пределах 0,875±0,004, то содержание рутина в процентах (X) вычисляют по формуле: где 325,5 - удельный показатель поглощения Е\%см чистого рутина (безводного) в абсолютном спирте при длине волны 362,5 нм; а - навеска в граммах. Если отношение D1/D2 превышает 0,879, то содержание рутина в процентах (X) вычисляют по формуле:
3.В условиях аптеки: · Обоснуйте правила введения спиртосодержащих лекарственных средств при изготовлении жидких лекарственных форм для внутреннего и наружного применения. При изготовлении ЖЛФ часто вводятся спиртосодержащие ЛФ (настойки, жидкие экстракты, эликсиры, новогаленовые (максимально очищенные препараты) спиртовые растворы). Следует руководствоваться положением приказа МЗ и соц. Развития России №308 от 21.10.97: - спиртовые растворы готовятся массо-объемным способом; - если в прописи рецепта без указания концентрации выписан раствор; предусмотренный в НД несколькими концентрациями ЛВ, отпускать следует раствор слабой концентрации (например, раствор борной кислоты 0,5%, 1%, 2%, 3%, 5% - отпускать 1% раствор, р-р йода 1%, бриллиантового зеленого 1% и т.д.) - норма отпуска спирта учетной концентрации в пересчете на массу составляет 50,0, в случае указания по специальному назначению – не более 100,0. - в сложные микстуры, спиртосодержащие жидкости следует добавлять по возрастанию крепости спирта во избежание образования осадка ДВ. - спиртосодержащие жидкости добавлять во флакон для отпуска после водных жидкостей без последующей фильтрации. - спирт при изготовлении экстемпоральных препаратов отмеривают по объему, а учитывают по массе в пересчете на 95 – 96%. - бланк рецепта №148, спирт находится на ПКУ.
4.Акцентируйте внимание на организационно-экономических аспектах: · Какой порядок ценообразования, отпуска из аптеки и учета этилового спирта, спиртосодержащих лекарственных форм и спиртовых настоек заводского изготовления? Задача №8 Задача №9 1.Фармацевт для изготовления лекарственной формы для новорожденного по прописи: Раствора глюкозы 10% 100 мл. Кислоты глютаминовой 1,0 Смешай. Выдай. Обозначь. По 1 чайной ложке 3 раза в день. взял раствора глюкозы 10% 100мл для инъекций после стерилизации, маркировки и контроля, вскрыл флакон и растворил в растворе глюкозы 1,0 кислоты глютаминовой, профильтровал, укупорил и оформил к отпуску. · Оцените действия фармацевта · Приведите оптимальный, на Ваш взгляд, вариант технологии данной лекарственной формы. Rp: Solutionis Glucosi 10% - 100 ml Acidi glutaminici 1,0 Misce. Da tales doses N 4. Signa: По 1 чайной ложке 3 раза в день (отделение новорождённых) Оптимальный вариант приготовления. Фармацевтическая экспертиза Выписан рецепт на сложную жидкую лекарственную форму для внутреннего применения для новорожденных. Форма бланка №107, в аптеке не хранится. Согласно приказу МЗ РФ № 309 от 1997г. Изменения № 2 от 14.08.01 к статье ГФ XI «методы микробиологического контроля лекарственных средств» растворы для новорождённых для внутреннего применения: • должны быть стерильными, готовиться в асептических условиях массо - объёмным способом на воде очищенной; • добавление стабилизаторов не допускается; • растворы глюкозы для внутреннего применения готовятся без стабилизатора; • в качестве растворителя используется вода очищенная; • глюкоза содержит 10 процентов влаги, следует делать пересчёт 10 * 100 Х= 100 -10 =11,11 КУО = 0,69 • объём растворов для внутреннего применения должен быть не более 100 мл; • режим стерилизации при t 120°С 8 минут в паровом стерилизаторе. • все лекарственные формы для новорожденных подвергаются полному химическому контролю; • флакон стерильный, не щелочного стекла КЗ – 100 К отпуску оформить этикеткой «Внутреннее» с зелёным сигнальным цветом с дополнительной надписью «Детское» «Для новорождённых» «Стерильно». Рабочая пропись: Объём микстуры 100 мл * 4 = 400 мл Воды очищенной 400 мл - (44,44 *0,69) = 369 мл или до 400 мл. Глюкозы (вл.10%) = 44,44 Кислоты глютаминовой 4,0 V = 400 мл Приготовление: Готовить в асептических условиях. В стерильную подставку отмерить стерильным цилиндром 369 мл воды очищенной. На ручных весах (протираются или обрабатываются спиртоэфирной смесью или 3% раствором Н202) отвесить 44,44 глюкозы с влажностью 10%, растворить в воде, добавить 1,0 кислоты глютаминовой, отвешенной на стерильных ручных весах 5,0, растворить, После полного растворения отдать на полный химический анализ. После положительного анализа раствор профильтровать через бумажный двойной стерильный фильтр, промытый водой очищенной, (при этом первую порцию фильтровать дважды) в 4 флакона, фасуя по 100 мл, Флаконы закрыть пробкой, проверить на чистоту, обкатать колпачком, на котором (или на бирке) написать «раствор глюкозы 10%, глютам. кислоты 1,0, дата, время», отдать на стерилизацию t = 120°- 8 мин., после чего снова проверить на целостность флакона и чистоту, оформить к отпуску. На этикетке: «в отдел новорождённых. Р-р глюкозы 10% с кислотой глютаминовой 1,0». № анализа, № серии, дата, кто готовил, проверил». Годность 30 суток до вскрытия «Детское» «Для новорождённых» «Стерильно». 2.Акцентируйте внимание на организационно-экономических аспектах: · Каков порядок организации изготовления и контроля качества в аптеках ЛС для новорожденных. · Как должен быть организован учет поступления и розничной реализации товаров в аптеке? · В каком документе материально-ответственного лица отражается движение товаров в аптеке? Лек средства для новорожденных: растворы для внутреннего и наружного применения, глазные капли, масла для обработки кожных покровов, инъекционные лекарственные формы - должны быть стерильны. Нормативные документы, регламентирующие требования: «Инструкция о санитарном режиме»; -приказ МЗРФ №309 от 1997г., в котором даны ссылки на приказ №1026 от 19.10.82г. -изменение №2 от 14.08.01 к статье ГФ 11 «Методы микробиологического контроля ЛС» -Методические указания по изготовлению стерильных растворов в аптеке от 1994г. На основании требований нормативной документации лек.средства для новорожденных и детей до года готовят в условиях асептики. Растворы лек.веществ, вспомогательные вещества и лекарственные вещества, выдерживающие стерилизацию, стерилизуют. В приказе МЗРФ №214 от 16.07.97 «О контроле качества лекарственных веществ, изготовленных в аптечных учреждениях» приведены условия приготовления, режимы стерилизации, условия и сроки хранения лек. форм для новорожденных и некоторых лек форм для детей более старшего возраста. Согласно приказу МЗРФ №214, лек. формы для новорожденных кроме обязательных видов внутриаптечного контроля: письменного
|
|||||
|
Последнее изменение этой страницы: 2016-04-23; просмотров: 1279; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.41 (0.013 с.) |



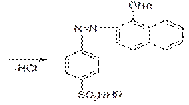








 2I- + 2Fe3+ I2 + 2Fe2+
2I- + 2Fe3+ I2 + 2Fe2+


 2KI + KIO3 + 6HCl 3ICl + 3KCl + 3H2O
2KI + KIO3 + 6HCl 3ICl + 3KCl + 3H2O


 2CuOH H2O + Cu2O
2CuOH H2O + Cu2O 2.Аптека получает лекарственные средства, содержащие глюкозу, напрямую от химико-фармацевтического предприятия. Какому уровню канала товародвижения это соответствует?
2.Аптека получает лекарственные средства, содержащие глюкозу, напрямую от химико-фармацевтического предприятия. Какому уровню канала товародвижения это соответствует?

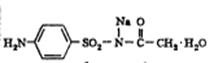
 + CuSO4 + Na2SO4
+ CuSO4 + Na2SO4