Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Пирогены, встречающиеся в медицинских препаратахСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Реферат Структура дипломной работы: Дипломная работа изложена на48страницах, состоит из введения, 3 глав (обзор литературы, материалы и методы тестирования на пирогенность и на бактериальные эндотоксины, результаты проведенных испытаний и их обсуждение), заключения и выводов, списка литературы из 71 названий, включает 7 таблицы, 3 рисунка. Ключевые слова: пирогенность, бактериальные эндотоксины, безопасность лекарственных средств, ЛАЛ-тест. Актуальность темы: За всю историю развития фармацевтики, было важно не только действие того или иного лекарственного препарата, а так же отсутствие опасности от применения. Дело в том, что доклинические испытания любого медицинского препарата и изделия дает выявить качество продукта и его дальнейшую судьбу. Одним из важных этих испытаний является тестирование на пирогенность. Одной из причин наличия пирогенности является присутствие в препарате бактериальных эндотоксинов. Все эти тестирования проводятся в целях безопасности и сохранности здоровья людей. Для проведения тестирования на пирогенность и на наличие бактериальных эндотоксинов в настоящее время используются два метода. Цель: сравнить результаты тестирования на пирогенность и на наличие бактериальных эндотоксинов при введении инфузионных лекарственных препаратов. Задачи: 1) Изучить и освоить принципы и методы фармакопейных тестирований на пирогенность и на наличие бактериальных эндотоксинов. 2) Провести испытания на наиболее широко применяемых инфузионных растворов. Объекты и методы: для тестирования пирогенности: половозрелые кролики весом от 2-х до 4-х килограмм, шприцы 10 мл, дистиллированная вода;для ЛАЛ-теста: термостат, стерилизованные пипетки и пробирки, апирогенная вода для ЛАЛ-теста, водяная баня.
Реферат Дипломдықжұмыс: 47беттен, 7 кестеден, 3 суреттентұрады, пайдаланғанәдебиеттертізімі – 71. Түйінсөздер: пирогенділік, бактериалдықэндотоксиндер, дәрі-дәрмектердіңкауіпсіздігі, ЛАЛ-тест. Жұмыстыңмақсаты: пирогенділіккежәнебактериалдықэндотоксингеөткізілгенсынақтардыңнәтижелерінсалыстыру. Жұмыстыңміндеттері: 1) Мемлекеттік фармакопея бойыншапирогентесті мен бактериалдыэндотоксингежасалатынсынақәдістеріноқыпбілу. 2) Жиіқолданылатынинфузиялықерітінділердіпирогендіккежәнеэндотоксиндергетексеру. Зерттеуобъектісіжәнеәдістері: пирогенділікке тест жасауүшін: жынысмүшелеріжетілген, салмағы 2 және 4килограммғадейінгіаралықтағықояндар, шприцтер 10мл, тазартылған су, ЛАЛ-тестіүшін: термостат, стерилдіпипеткалар мен пробиркалар, апирогенді су. Практикалықмаңыздылығы: Қазіргі уақытта халықтың денсаулығын сақтау үшін тек қана дәрі-дәрмек өндіру ғана емес, оған қоса өндірілген тауарды тексерістен өткізу маңызды орын алады. Себебі дәрі-дәрмектердің сапасыныңөндіріс барысында немесе тасымалдау кезінде төмендеуі ықтимал. Оған себеп – өндіріс кезінде бөгде заттардың немесе сұйықтықтардың енуі. Осы себепті жағымсыз салдарды алдын алу үшін дәрі-дәрмектерді пирогендікке және бактериалдық эндотоксинге арнайы тексериз жүргізіледі. Бұл әдістердің уақыт бойынша қайсысы тиімді екенін және дәл нәтиже көрсететінін салыстырмалы түрде көруге болады.
Abstract The structure of diploma work: volume of diploma work is 47 pages, diploma work consists of an introduction, three chapters (literature review, materials and methods), findings and conclusions, bibliography of 71 titles, including 7 tables, 3 figures. Keywords: pyrogenicity, bacterial endotoxins, safety of medicines, Limulus test. There are many ways to provide the safety of medicines imported from foreign countries and making in our government. Only two ways afford us to distinguish the pyrogens and bacterial endotoxins. They are pyrogen tests and LAL-tests (limulus amebocyte lysate). These approaches determine usefulness of medicines and medical products. Objective: a comparison of efficiency of pyrogen tests and LAL-tests in injection of infusion solutions. Task of study: 1) to study and learn principles and methods of pharmacopoeia tests for the presence of pyrogenicity and bacterial endotoxins. 2) to spend experience for the most common infusion solutions. Subjects and methods: for the pyrogen tests: sexually mature rabbits weighing from 2 kg until 4 kg, syringes 10 ml, distilling water; for LAL-test: thermostat, sterilized test tubes and pipettes, apyrogenic water for LAL-test, water bath. Practical importance: we can see what kind of these ways is faster and more effective.
СОДЕРЖАНИЕ ВВЕДЕНИЕ……………………………………………………………………….…7 ОСНОВНАЯ ЧАСТЬ 1. ЛИТЕРАТУРНЫЙ ОБЗОР.…………………………………………….……….9 1.1. Пирогенность. Пирогены, встречающиеся в медицинских препаратах…....9 1.2. Limulusamebocytelysate (ЛАЛ-тест)………………………………………...13 2.МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ………………………………31 2.1. Материалы исследования……………………………………………………..31 2.2. Методы исследования………………………………………………………....31 3.РЕЗУЛЬТАТЫ ИСПЫТАНИЙ И ИХ ОБСУЖДЕНИЕ …………………….....34 3.1. Исследование особенностей теста на пирогенность………………………...34 3.2. Изучение особенностей теста на наличие бактериальных эндотоксинов…38 ЗАКЛЮЧЕНИЕ…………………………………………………………………......41 СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ……………………………......42 СПИСОК СОКРАЩЕНИЙ………………………………………………………...48
ВВЕДЕНИЕ Одной из задач Системы организации производства и контроля качества (GMP) является гарантия безопасности применения выпускаемого продукта. В отличие от лекарственных препаратов, для которых четко регламентированы как параметры безопасности, так и методики их контроля, адекватный контроль безопасности медицинских изделий является более сложной задачей. Химическая стабильность медицинского изделия в условиях использования – один из параметров безопасности, определяемый на стадии лабораторных испытаний. Однако, человеческий организм не может оказаться более чувствительным к отдельным химическим веществам, чем используемые методы контроля. Поэтому в программу доклинических испытаний обязательно входит тестирование пирогенной реакции на кроликах и на наличие бактериальных эндотоксинов. Наиболее часто пирогенность медицинских изделий, так же как и лекарственных средств, обусловлена наличием бактериальных эндотоксинов. В настоящее время контроль на наличие бактериальных эндотоксинов проводится при помощи ЛАЛ-теста. Этот метод обладает высокой чувствительностью, достаточно прост в исполнении и может быть принят на вооружение практически любой лабораторией отдела контроля качества предприятия. Главным образом определения пирогенности долгое время был тест на кроликах. В этом тесте исследуется реакция кроликов на введение им в кровь испытуемого раствора. Повышение температуры тела животного выше допустимой нормы указывает на наличие пирогенных примесей. Этот тест был впервые узаконен Фармакопеей США XII издания в 1942 г. Этому в немалой степени способствовала высокая потребность в инъекционных лекарствах, в том числе в инфузионных растворах во время войны. Однако, сравнительно недавно появился тест, способный регистрировать наличие эндотоксинов. Речь идет о ЛАЛ-тесте или Limulus тесте, представляющим собой реакцию invitro между эндотоксинами и ЛАЛ-реагентом. В отличие от теста на кроликах, в данном случае речь идет не о пирогенах вообще, а именно об эндотоксинах грамотрицательных бактерий. Именно с эндотоксинами, и только с ними способен специфически реагировать лизат амебоцитов Limulus/ Впервые этот тест был включен в Фармакопею США ХХ издания в 1985 г. и получил название «Определение бактериальных эндотоксинов». ЛАЛ-тест для определения пирогенности лекарственных препаратов является активно развивающимся в настоящее время способом контроля качества лекарств, воды для инъекций и т.д. В основе этого теста лежит способность лизата амебоцитов мечехвоста специфически реагировать с эндотоксинами грамотрицательных бактерий. В результате реакции эндотоксина и лизата происходит помутнение прозрачной реакционной смеси или образование твердого геля, что и служит индикатором присутствия эндотоксина. Реакция просто и не требует много времени, ответ может быть получен через 30-60 мин. Тест высокоспецифичен по отношению к эндотоксинам грамотрицательных бактерий. Чувствительность его во много раз превышает чувствительность фармакопейного теста на кроликах. Сырьем для производства ЛАЛ-реагента служит кровь мечехвостов. – морских животных, обитающих у берегов Северной Америки, Японии, Китая, Индии, Вьетнама. В данной работе рассматриваются особенности фармакопейных методов тестирование на пирогенность и на наличие бактериальных эндотоксинов. Приводятся результаты, полученные при проверке на пирогенность и эндотоксины инфузионных растворов. Цель исследования. Сравнение обоих методов по эффективности, скорости, а так же по точности данных на примере инфузионных растворов. Задачи: 1) Изучить и освоить принципы и методы фармакопейных тестирований на пирогенность и на наличие бактериальных эндотоксинов. 2) Провести испытания на наиболее широко применяемых инфузионных растворов.
ОСНОВНАЯ ЧАСТЬ ЛИТЕРАТУРНЫЙ ОБЗОР Пирогенность Материалы исследования
Испытания проводились в национальном центре экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники «Дәрі-дәрмек» МЗ и СР РК. Материалами исследования служили: для тестирования пирогенности: половозрелые кролики весом от 2-х до 4-х килограмм, шприцы с объемом 10 мл, дистиллированная вода, термостат, стерилизованные пипетки и пробирки, апирогенная вода для ЛАЛ-теста, водяная баня, инфузионные растворы.
Методы исследования Испытание на бактериальные эндотоксины Данный раздел частично гармонизирован с соответствующими текстами Государственной Фармакопеей Республики Казахстан и Аналитическим нормативным документом Республики Казахстан. Испытание проводят с использованием ЛАЛ, полученного из экстракта амебоцитов мечехвоста, приготовленного и рекомендованного к применению в качестве ЛАЛ-реактива. Испытание проводят двумя методами: гель-тромб, который основан на образования геля, и фотометрический метод. В последствии были разработаны турбидиметрический метод, основанный на появлении мутности после расщепления эндогенного субстрата, а также хромогенный метод, который основан на развитии окраски после разложения синтетического пептидно-хромогенного комплекса. Испытание проводят любым из этих двух методов, если в частности фармакопейной статье не указано иное. В сомнительных случаях окончательное решение принимают на основании результатов, полученных методом гель-тромб теста, если в частной фармакопейной статье не указано иное. Объектами испытания являются растворы для инфузионной терапии: раствор глюкозы, раствор натрия хлорида и ацесоль. Приборы и стеклянная посуда. Используя валидированный процесс, депирогенизируют всю стеклянную посуду и другие термостабильные материалы в сухожаровом шкафу. Стерилизацию обычно проводят минимум в течение 30 минут при температуре 250 Приготовление основного раствора стандарта эндотоксина и его рабочих растворов. Стандартный образец эндотоксина Фармакопей США имеет установленную активность 10000 ЕЭ в одном флаконе. Содержимое одного флакона разводят в 5 мл воды для ЛАЛ-теста, периодически перемешивают в течение 30 минут с помощью вортекса. Этот концентрат используют для приготовления последующих разведений. Его хранят в холодильнике не более 14 сут. Перед использованием этот раствор тщательно перемешивают не менее трех минут с помощью вортекса. Каждое разведение перемешивают не менее 30 сперед приготовлением следующего разведения. Во избежание потери активности вследствие адсорбции эндотоксина разведения должны быть свежеприготовленными, если нет данных, указывающих обратное. Готовят растворы образца путем растворения или разбавления лекарственного препарата и промывки медицинской аппаратуры водой для ЛАЛ-теста. Некоторые субстанции или препараты могут быть разбавлены, растворены или экстрагированы с помощью других подходящих водных растворов. При необходимости доводят рН раствора (или его разведения) таким образом, чтобы рН смеси ЛАЛ-реактива и образца находился в диапазоне, установленным производителем ЛАЛ-тест реактива. В большинстве случаев диапазон рН составляет 6,0 до 8,0. рН можно изменить, используя кислоту, основание или соответствующий буфер, рекомендованный производителем ЛАЛ-реактива. Кислоту и основание готовят с помощью концентрированных растворов или твердых веществ и воды ЛАЛ-теста в емкостях, не содержащих эндотоксин. Буфер должен быть проверен на отсутствие эндотоксина и мешающих факторов. Максимально допустимое разведение(МДР) – максимально допустимое разведение образца, в котором может быть определено предельное содержание эндотоксинов. Это понятие применимо к инъекционным лекарственным средствам или растворам для парентерального введения в готовой или разведенной форме, или к количеству лекарственного средства по весу, если объем вводимой дозы различен. Основная формула для определения МДР выглядит следующим образом: МДР=(предельный уровень эндотоксина х концентрация раствора испытуемого образца)/λ, где концентрация раствора образца и λ, т.е. заявленную чувствительность (ЕЭ/мл) ЛАЛ-реактива, используемого в данном методе. Если в частной фармакопейной статье уровень содержания эндотоксина указан в весовых единицах или в единицах активности препарата (ЕЭ/мл или ЕЭ на единицу действия), то для вычисления МДР умножают предельную концентрацию препарата (мг/мл или МЕ/мл) в испытуемом растворе или субстанции, и делят полученный результат на λ. Полученное таким образом значение МДР – предельное значение разведения препарата, при котором испытание можно считать достоверным. Уровень бактериальных эндотоксинов, определенный на основании дозы препарата, равен: К/М3, где К – пороговая величина пирогенной дозы эндотоксина на килограмм массы тела человека; М – максимальная доза препарата на килограмм массы тела человека, вводимая в течение часа. Уровень эндотоксина для парентеральных препаратов установлен в частных фармакопейных статьях в ЕЭ/мл, ЕЭ/мг или ЕЭ/единицы биологической активности. Гель-тромб тест – метод обнаружения или определения количества эндотоксинов основанный на реакции гелеобразования ЛАЛ-реактива в присутствии эндотоксина. Чувствительность ЛАЛ-реактива, указанная на этикетке флакона, - концентрация эндотоксина, которая вызывает реакцию гелеобразования лизата при нормальных условиях опыта. Для того, чтобы обеспечить точность и достоверность результатов испытания, необходимо поверить и подтвердить заявленную чувствительность ЛАЛ-реактива и отсутствие мешающих факторов, согласно подразделу «Предварительные испытания при использовании метода гель-тромб теста». Реферат Структура дипломной работы: Дипломная работа изложена на48страницах, состоит из введения, 3 глав (обзор литературы, материалы и методы тестирования на пирогенность и на бактериальные эндотоксины, результаты проведенных испытаний и их обсуждение), заключения и выводов, списка литературы из 71 названий, включает 7 таблицы, 3 рисунка. Ключевые слова: пирогенность, бактериальные эндотоксины, безопасность лекарственных средств, ЛАЛ-тест. Актуальность темы: За всю историю развития фармацевтики, было важно не только действие того или иного лекарственного препарата, а так же отсутствие опасности от применения. Дело в том, что доклинические испытания любого медицинского препарата и изделия дает выявить качество продукта и его дальнейшую судьбу. Одним из важных этих испытаний является тестирование на пирогенность. Одной из причин наличия пирогенности является присутствие в препарате бактериальных эндотоксинов. Все эти тестирования проводятся в целях безопасности и сохранности здоровья людей. Для проведения тестирования на пирогенность и на наличие бактериальных эндотоксинов в настоящее время используются два метода. Цель: сравнить результаты тестирования на пирогенность и на наличие бактериальных эндотоксинов при введении инфузионных лекарственных препаратов. Задачи: 1) Изучить и освоить принципы и методы фармакопейных тестирований на пирогенность и на наличие бактериальных эндотоксинов. 2) Провести испытания на наиболее широко применяемых инфузионных растворов. Объекты и методы: для тестирования пирогенности: половозрелые кролики весом от 2-х до 4-х килограмм, шприцы 10 мл, дистиллированная вода;для ЛАЛ-теста: термостат, стерилизованные пипетки и пробирки, апирогенная вода для ЛАЛ-теста, водяная баня.
Реферат Дипломдықжұмыс: 47беттен, 7 кестеден, 3 суреттентұрады, пайдаланғанәдебиеттертізімі – 71. Түйінсөздер: пирогенділік, бактериалдықэндотоксиндер, дәрі-дәрмектердіңкауіпсіздігі, ЛАЛ-тест. Жұмыстыңмақсаты: пирогенділіккежәнебактериалдықэндотоксингеөткізілгенсынақтардыңнәтижелерінсалыстыру. Жұмыстыңміндеттері: 1) Мемлекеттік фармакопея бойыншапирогентесті мен бактериалдыэндотоксингежасалатынсынақәдістеріноқыпбілу. 2) Жиіқолданылатынинфузиялықерітінділердіпирогендіккежәнеэндотоксиндергетексеру. Зерттеуобъектісіжәнеәдістері: пирогенділікке тест жасауүшін: жынысмүшелеріжетілген, салмағы 2 және 4килограммғадейінгіаралықтағықояндар, шприцтер 10мл, тазартылған су, ЛАЛ-тестіүшін: термостат, стерилдіпипеткалар мен пробиркалар, апирогенді су. Практикалықмаңыздылығы: Қазіргі уақытта халықтың денсаулығын сақтау үшін тек қана дәрі-дәрмек өндіру ғана емес, оған қоса өндірілген тауарды тексерістен өткізу маңызды орын алады. Себебі дәрі-дәрмектердің сапасыныңөндіріс барысында немесе тасымалдау кезінде төмендеуі ықтимал. Оған себеп – өндіріс кезінде бөгде заттардың немесе сұйықтықтардың енуі. Осы себепті жағымсыз салдарды алдын алу үшін дәрі-дәрмектерді пирогендікке және бактериалдық эндотоксинге арнайы тексериз жүргізіледі. Бұл әдістердің уақыт бойынша қайсысы тиімді екенін және дәл нәтиже көрсететінін салыстырмалы түрде көруге болады.
Abstract The structure of diploma work: volume of diploma work is 47 pages, diploma work consists of an introduction, three chapters (literature review, materials and methods), findings and conclusions, bibliography of 71 titles, including 7 tables, 3 figures. Keywords: pyrogenicity, bacterial endotoxins, safety of medicines, Limulus test. There are many ways to provide the safety of medicines imported from foreign countries and making in our government. Only two ways afford us to distinguish the pyrogens and bacterial endotoxins. They are pyrogen tests and LAL-tests (limulus amebocyte lysate). These approaches determine usefulness of medicines and medical products. Objective: a comparison of efficiency of pyrogen tests and LAL-tests in injection of infusion solutions. Task of study: 1) to study and learn principles and methods of pharmacopoeia tests for the presence of pyrogenicity and bacterial endotoxins. 2) to spend experience for the most common infusion solutions. Subjects and methods: for the pyrogen tests: sexually mature rabbits weighing from 2 kg until 4 kg, syringes 10 ml, distilling water; for LAL-test: thermostat, sterilized test tubes and pipettes, apyrogenic water for LAL-test, water bath. Practical importance: we can see what kind of these ways is faster and more effective.
СОДЕРЖАНИЕ ВВЕДЕНИЕ……………………………………………………………………….…7 ОСНОВНАЯ ЧАСТЬ 1. ЛИТЕРАТУРНЫЙ ОБЗОР.…………………………………………….……….9 1.1. Пирогенность. Пирогены, встречающиеся в медицинских препаратах…....9 1.2. Limulusamebocytelysate (ЛАЛ-тест)………………………………………...13 2.МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ………………………………31 2.1. Материалы исследования……………………………………………………..31 2.2. Методы исследования………………………………………………………....31 3.РЕЗУЛЬТАТЫ ИСПЫТАНИЙ И ИХ ОБСУЖДЕНИЕ …………………….....34 3.1. Исследование особенностей теста на пирогенность………………………...34 3.2. Изучение особенностей теста на наличие бактериальных эндотоксинов…38 ЗАКЛЮЧЕНИЕ…………………………………………………………………......41 СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ……………………………......42 СПИСОК СОКРАЩЕНИЙ………………………………………………………...48
ВВЕДЕНИЕ Одной из задач Системы организации производства и контроля качества (GMP) является гарантия безопасности применения выпускаемого продукта. В отличие от лекарственных препаратов, для которых четко регламентированы как параметры безопасности, так и методики их контроля, адекватный контроль безопасности медицинских изделий является более сложной задачей. Химическая стабильность медицинского изделия в условиях использования – один из параметров безопасности, определяемый на стадии лабораторных испытаний. Однако, человеческий организм не может оказаться более чувствительным к отдельным химическим веществам, чем используемые методы контроля. Поэтому в программу доклинических испытаний обязательно входит тестирование пирогенной реакции на кроликах и на наличие бактериальных эндотоксинов. Наиболее часто пирогенность медицинских изделий, так же как и лекарственных средств, обусловлена наличием бактериальных эндотоксинов. В настоящее время контроль на наличие бактериальных эндотоксинов проводится при помощи ЛАЛ-теста. Этот метод обладает высокой чувствительностью, достаточно прост в исполнении и может быть принят на вооружение практически любой лабораторией отдела контроля качества предприятия. Главным образом определения пирогенности долгое время был тест на кроликах. В этом тесте исследуется реакция кроликов на введение им в кровь испытуемого раствора. Повышение температуры тела животного выше допустимой нормы указывает на наличие пирогенных примесей. Этот тест был впервые узаконен Фармакопеей США XII издания в 1942 г. Этому в немалой степени способствовала высокая потребность в инъекционных лекарствах, в том числе в инфузионных растворах во время войны. Однако, сравнительно недавно появился тест, способный регистрировать наличие эндотоксинов. Речь идет о ЛАЛ-тесте или Limulus тесте, представляющим собой реакцию invitro между эндотоксинами и ЛАЛ-реагентом. В отличие от теста на кроликах, в данном случае речь идет не о пирогенах вообще, а именно об эндотоксинах грамотрицательных бактерий. Именно с эндотоксинами, и только с ними способен специфически реагировать лизат амебоцитов Limulus/ Впервые этот тест был включен в Фармакопею США ХХ издания в 1985 г. и получил название «Определение бактериальных эндотоксинов». ЛАЛ-тест для определения пирогенности лекарственных препаратов является активно развивающимся в настоящее время способом контроля качества лекарств, воды для инъекций и т.д. В основе этого теста лежит способность лизата амебоцитов мечехвоста специфически реагировать с эндотоксинами грамотрицательных бактерий. В результате реакции эндотоксина и лизата происходит помутнение прозрачной реакционной смеси или образование твердого геля, что и служит индикатором присутствия эндотоксина. Реакция просто и не требует много времени, ответ может быть получен через 30-60 мин. Тест высокоспецифичен по отношению к эндотоксинам грамотрицательных бактерий. Чувствительность его во много раз превышает чувствительность фармакопейного теста на кроликах. Сырьем для производства ЛАЛ-реагента служит кровь мечехвостов. – морских животных, обитающих у берегов Северной Америки, Японии, Китая, Индии, Вьетнама. В данной работе рассматриваются особенности фармакопейных методов тестирование на пирогенность и на наличие бактериальных эндотоксинов. Приводятся результаты, полученные при проверке на пирогенность и эндотоксины инфузионных растворов. Цель исследования. Сравнение обоих методов по эффективности, скорости, а так же по точности данных на примере инфузионных растворов. Задачи: 1) Изучить и освоить принципы и методы фармакопейных тестирований на пирогенность и на наличие бактериальных эндотоксинов. 2) Провести испытания на наиболее широко применяемых инфузионных растворов.
ОСНОВНАЯ ЧАСТЬ ЛИТЕРАТУРНЫЙ ОБЗОР Пирогенность Пирогены, встречающиеся в медицинских препаратах Во многих словарях термин «пироген» объясняется таким образом: слово происходит от греческого “pyreto” – лихорадка. То есть, пирогенами называют те вещества, которые способны вызывать повышение температуры тела при попадании в кровь. Давайте разберем, какие вещества относятся к пирогенам: это – грамотрицательные бактерии и их токсины, вирусы и продукты их жизнедеятельности, лизированные микробные клетки и пр. По химическому составу пирогенные вещества представляют собой липополисахаридные или липополисахаридно-протеиновые комплексы наружных мембран грамотрицательных бактерий, так называемые – бактериальные эндотоксины. Пирогенные вещества – это высокомолекулярные соединения, они нелетучие и не перегоняются с водяным паром. Загрязнение жидкостей, в особенности, дистиллированной воды пирогенными веществами происходит чаще всего в результате переброса капельной фазы, содержащей пирогенные вещества, из испарителя в конденсатор и сборник аквадистиллятора. Пирогены– термостабильные вещества, они разрушаются только при нагревании в суховоздушных стерилизаторах при температуре 250°С в течение 30 минут. При воздействии пара под давлением (t 120°Савтоклавированием) в растворах пирогены разрушаются только через 5 часов. Следовательно, освободиться от пирогенных веществ в воде и инъекционных растворах при помощи термической стерилизации практически невозможно. Таким образом, каждый инъекционный раствор после его правильной стерилизации стерилен, но не каждый стерильный раствор – апирогенен.Стерильность и апирогенность – разные понятия и подменять одно другим – нельзя[1]. Пирогенами называют эндогенные или экзогенные вещества, вызывающие пирогенные эффекты (лихорадку). Эндогенные пирогены вырабатываются в организме в ответ на различные стимулы; чаще всего это инфекция или воспаление. Экзогенные пирогены представлены в основном микроорганизмами, их токсинами и продуктами жизнедеятельности. Типичный пример экзогенногопирогена - эндотоксин. Он представляет собой липополисахарид наружной мембраны грамотрицательных бактерий и состоит из липида А(рисунок 1), полисахаридного ядра и боковой цепи - O-полисахарида. Последовательность олигосахаридов в боковой цепи у всех бактерий разная. Липид А состоит из дисахарида, фосфата и жирных кислот.
Рисунок 1. Химическая структура О-специфической цепи Кор ЛипидаА[по 3]. Липид А состоит из дисахарида, фосфата и жирных кислот. Жирные кислоты, входящие в состав Липида А, могут быть насыщенными и ненасыщенными. Наиболее часто в состав Липида А входят кислоты: пальмитиновая, лауриновая, глутаминовая, меристиновая. Участок Липида А является наиболее константным участком молекулы ЛПС, и его строение схоже у многих бактерий. О-специфическая цепь липополисахаридов построена из повторяющихся олигосахаридов. Наиболее распространенными сахарами, входящими в состав О-специфической цепи, являются глюкоза, галактоза, рамноза. Этот участок молекулы придает ей гидрофильные свойства, благодаря которым ЛПС хорошо растворимы в воде. Полисахаридная часть является наиболее вариабельной частью молекулы ЛПC. Часто этот фрагмент молекулы называют О-антигеном, так как именно он отвечает за антигенную активность грамотрицательных бактерий. Кор - центральная часть молекулы, связывающая О-антиген с Липидом А. Формально структура кора подразделяется на внешнюю и внутреннюю части. В состав внутренней части кора обычно входят остатки L-глицеро-О-манногептозы и 2-кето-3-дезоксиоктоновой кислоты (КДО). КДО содержит 8 атомов углерода и в природе практически нигде больше не встречается. Жирные кислоты, входящие в состав Липида А, могут быть насыщенными и ненасыщенными. Наиболее часто в состав Липида А входят кислоты: пальмитиновая, лауриновая, глутаминовая, меристиновая. Участок Липида А является наиболее константным участком молекулы ЛПС, и его строение схоже у многих бактерий. Доза эндотоксина, способная вызвать у человека лихорадку, составляет 1 нг/кг. Большинство экзогенныхпирогенов вызывают лихорадку, стимулируя образование эндогенных пирогенов клетками макроорганизма (обычно это моноциты и макрофаги). Но из этого правила есть исключения. Так, эндотоксин вызывает лихорадку без участия эндогенныхпирогенов, воздействуя на эндотелиальные клетки в головном мозге[2]. Эндогенные пирогены включают иммунные комплексы, продукты распада комплемента, метаболиты стероидных гормонов, желчные кислоты и цитокины. Большинство эндогенныхпирогенов представляют собой полипептиды, которые вырабатываются многими клетками макроорганизма, особенно моноцитами и макрофагами. Они поступают в кровоток и вызывают лихорадку, воздействуя на терморегуляторный центр гипоталамуса [2]. Бактериальный эндотоксин является постоянным структурным компонентом наружной клеточной стенки грамотрицательных бактерий (рисунок 2). По структуре это липополисахарид (ЛПС), состоящий из липида А (базисной части или ядра) и О-специфичной цепи полисахарида, образованной повторяющимися идентичными полисахаридными последовательностями. Живые организмы находятся в постоянном контакте с эндотоксином, так как в кишечнике обитает довольно большое количество грамотрицательных бактерий [5-7]. У человека в 1 мл плазмы крови содержится примерно 3-10 пкг эндотоксина[6]. У здоровых организмов имеются резервы связывания эндотоксина лейкоцитами[8]. В зависимости от концентрации эндотоксин может вызывать активацию лейкоцитов и макрофагов, стимуляцию продукции эндогенногопирогена. Бактериальные эндотоксины являются исключительно сильными пирогенами: для развития лихорадочного приступа достаточно присутствия в инфузионном растворе бактериальных эндотоксинов в концентрации 1 нг/мл. Возможна ответная активация антагонистов глюкокортикоидов, интерферона, интерлейкинов, фактора некроза опухоли (кахексина) и других медиаторов, а также синтеза белков острой фазы (в том числе амилоидного), миелопоэза, системы комплемента. Происходит поликлональная активация В-клеток. Так же в связи с этим могут появляться индукция развития провирусов, митогенный эффект, подавление тканевого дыхания, гиперлипидемия, диссеминированное внутрисосудистое свертывание крови, эндотоксический шок и острая полиорганная недостаточность [10].
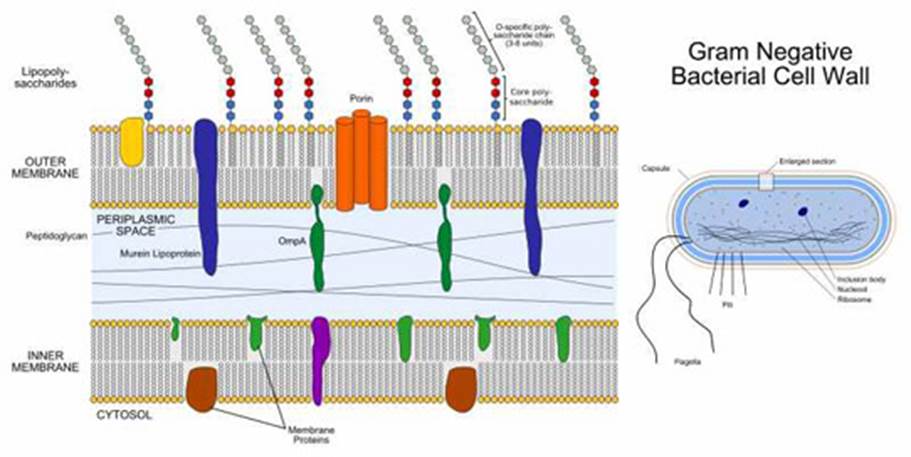
Рисунок 2. Строение клеточной стенки у грамположительных бактерий [по 4]. Несмотря на давние (начиная с 40-х годов ХХ в.) и разносторонние исследования, эндотоксин до сих пор остается объектом пристального внимания, в том числе и в связи со сложностью и многоликостью его физиологического воздействия на живой организм[12]. В настоящее время существует ряд иммунологических и биохимических методов, позволяющих определять содержание ЛПС в биологических жидкостях. Для определения содержания эндотоксина в лекарственных препаратах и изделиях медицинского назначения на протяжении более 30 лет успешно используется ЛАЛ-тест в различных модификациях[13]. Для сертификации фармацевтической и медицинской продукции на пирогенность ЛАЛ-тест включен в арсенал лабораторных методов многих стран. Этот метод основан на способности ЛПС вызывать коагуляцию белков, содержащихся в лизате амебоцитов мечехвоста. (Подробнее о ЛАЛ-тесте описано в разделе 1.2)[9-11]. Таким образом, значение эндотоксина велика в медицинской отрасли и, в общем, для ученых создается большой интерес в изучении природы эндотоксина, так как его динамичная эволюция не дает однозначных результатов в исследованиях. Наука и медицина, шагая вперед с новыми технологиями, дает возможность обезопасить применение лекарственных препаратов. Методы обнаружения бактериальных эндотоксинов будут описаны ниже.
|
||||
|
Последнее изменение этой страницы: 2016-08-06; просмотров: 872; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 13.59.205.182 (0.009 с.) |

 С. Если используют устройство из пласмассы, такие как микропланшеты и наконечники для автоматических пипеток, то они должны быть апирогенными и не влиять на результаты испытания.
С. Если используют устройство из пласмассы, такие как микропланшеты и наконечники для автоматических пипеток, то они должны быть апирогенными и не влиять на результаты испытания.