Тема 9. 4. Обмен аммиака: источники, превращение в тканях
Содержание книги
- Регуляция активности пируваткиназы в печени осуществляется путем фосфорилирования (дефосфорилирования) в зависимости от ритма питания
- Структурная организация межклеточного матрикса (суставной хрящ, базальные мембраны, субэпителиальные слои)
- Гликозилирование лизина под действием гликозилтрансфераз прекращается по мере формирования трехспиральной структуры.
- Патологий, связанных с уменьшением эластичности сосудов. При недостаточной активности металлопротеиназ развивается фиброз тканей и неадекватный иммунный ответ.
- Хондроитинсульфат; 2 - кератансульфат; 3 - коровый белок; гк - гиалуроновая кислота
- Тема 7. 5. Структурная организация межклеточного матрикса (суставной хрящ, базальные мембраны, субэпителиальные слои)
- Регуляция процесса. Амф, гмф, имф, ди- и трифосфаты адениловых и гуаниловых нуклеотидов ингибируют ключевые реакции своего синтезааллостерически по механизму отрицательной обратной связи.
- Частым нарушением катаболизма пуринов является гиперурикемия, которая возникает, когда в плазме крови Концентрация мочевой кислоты превышает норму.
- Синтез цтф из утф осуществляет цтф-синтетаза, используя амидную группу глн и энергию атф для аминирования пиримидинового кольца.
- Тема 10. 3. Биосинтез дезоксирибонуклеотидов.
- Тема 10. 4. Механизмы действия противовирусных и противоопухолевых препаратов на ферменты синтеза рибо- и дезоксирибонуклеотидов
- И рецепторов. Особенно много сфинголипидов в нервной ткани, где они формируют миелиновые оболочки нейронов.
- Тема 8. 3. Хиломикроны - транспортная форма экзогенных жиров
- Модульная единица 2 биосинтез высших жирных кислот и жиров
- Реакции восстановления обеспечивают синтез насыщенного алифатического радикала жирных кислот
- Запасание жиров в жировой ткани - так называемое депонирование жиров - происходит в абсорбтивный период, когда увеличивается соотношение инсулин - глюкагон.
- Первичное ожирение развивается в результате алиментарного дисбаланса - избыточной калорийности питания по сравнению с расходами энергии.
- Модульная единица 3 жиры, жирные кислоты и кетоновые тела как источники энергии. Эйкозаноиды, Строение, синтез и биологические функции
- Скелетные мышцы и почки используют кетоновые тела даже при их низкой концентрации в крови.
- Выведение кетоновых тел, в том числе и ацетона, с мочой (кетонурия), потом выдыхаемым воздухом является способом выведения избытка кетоновых тел из организма и уменьшения таким образом ацидоза.
- Ацетильный остаток переносится с молекулы аспирина на oh-группу фермента и необратимо ингибирует его
- Модульная единица 4 обмен холестерола, его регуляция и транспорт кровью. Дислипопротеинемии. Биосинтез и функции желчных кислот. Желчнокаменная болезнь
- В поддержании гомеостаза холестерола в организме. Биохимия желчнокаменной болезни
- Тема 8. 14. Роль липопротеинов в транспорте
- Атеросклероз представляет собой заболевание, при котором поражается внутренний слой артерий за счет отложения холестерола в интиме сосудов.
- Тема 9. 2. Переваривание белков в желудке и кишечнике, всасывание аминокислот
- Тема 9. 3. Трансаминирование и дезаминирование аминокислот
- Тема 9. 4. Обмен аммиака: источники, превращение в тканях
- Тема 9. 5. Орнитиновый цикл и его биологическая роль
- Тема 9. 6. Гипераммониемия и ее причины
- Тема 9. 8. Биосинтез заменимых аминокислот
- Тема 9. 10. Обмен метионина. Реакции трансметилирования
- Тема 9. 11. Обмен фенилаланина, тирозина и гистидина в разных тканях
- Тема 9. 12. Заболевания, связанные с нарушением обмена фенилаланина и тирозина
- Тема 9. 13. Биогенные амины: синтез, инактивация, биологическая роль
- Тема 11. 1. Роль гомонов в регуляции метаболизма
- Тема 11. 3. Строение и биосинтез гормонов
- Тема 11. 4. Регуляция обмена основных энергоносителей при нормальном ритме
- Тема 11. 5. Изменения метаболизма при гипо- и гиперсекреции гормонов
- Тема 11. 6. Изменения гормонального статуса и метаболизма при голодании и физической работе
- Тема 11. 7. Изменения гормонального статуса и метаболизма при сахарном диабете
- Тема 11. 8. Регуляция водно-солевого обмена
- Тема 11. 9. Регуляция обмена кальция и фосфатов. Строение, синтез и механизм действия паратгормона, кальцитриола и кальцитонина
- Модуль 12 обезвреживание токсических веществ в печени
- Тема 12. 2. Обезвреживание продуктов катаболизма аминокислот в кишечнике
- Тема 12. 3. Биотрансформация лекарств
- Тема 12. 5. Химический канцерогенез
- Тема 13. 1. Синтез гема и его регуляция
- Тема 14. 1. Метаболизм эритроцитов
- Тема 14. 2. Особенности метаболизма фагоцитирующих клеток
1. Основным источником аммиака является катаболизм аминокислот в
тканях. Небольшая часть аммиака образуется в клетках при распаде азотсодержащих соединений (биогенных аминов, нуклеотидов и др.) (рис. 9.7), а также при гниении белков в кишечнике в результате деятельности микрофлоры, откуда он частично всасывается и поступает в воротную вену. Концентрация аммиака в крови воротной вены существенно выше, чем в общем кровотоке.
Катаболизм аминокислот и образование аммиака происходит во всех тканях организма. Однако концентрация аммиака в крови очень мала, так как он быстро связывается в клетках с образованием нетоксичных продуктов. Содержание аммиака в крови в норме составляет всего 0,4-0,7 мг/л (25-40 мкмоль/л).
Из организма аммиак выводится почками в виде конечных продуктов азотистого обмена:
• мочевины - синтезируется в печени;
• аммонийных солей - образуются в почках.
 Рис. 9.7. Источники аммиака и пути его превращения в разных тканях Рис. 9.7. Источники аммиака и пути его превращения в разных тканях
2. В разных тканях существует несколько способов связывания и выведения аммиака (рис. 9.8).
Основной реакцией обезвреживания аммиака почти во всех тканях является синтез глутамина под действием глутаминсинтетазы:
 Глутаминсинтетаза обладает высоким сродством к аммиаку и благодаря этой реакции в крови и тканях поддерживается низкая концентрация NH3. Глутаминсинтетаза обладает высоким сродством к аммиаку и благодаря этой реакции в крови и тканях поддерживается низкая концентрация NH3.
Глутамин можно считать транспортной формой аммиака, он является нейтральной аминокислотой и способен легко проникать через клеточные мембраны путем облегченной диффузии (в отличие от глутамата, требующего механизмов активного транспорта). Глутамин поступает в кровь из многих органов, в наибольшем количестве - из мышц и мозга (см. рис. 9.8).
3. Из тканей глутамин транспортируется в почки и кишечник. В клетках кишечника под действием фермента глутаминазы происходит отщепление амидной группы в виде NH3 а образовавшийся глутамат с помощью АЛТ превращается в аланин.
 Таким образом, в энтероцитах амидная группа глутамина превращается в аммиак, а аминогруппа глутамина - включается в состав аланина. Таким образом, в энтероцитах амидная группа глутамина превращается в аммиак, а аминогруппа глутамина - включается в состав аланина.
4. В почках глутамин также подвергается действию фермента глутаминазы и
расщепляется на глутамат, который реабсорбируется и возвращается в клетки тканей, и аммиак (см. рис. 9.8, В).
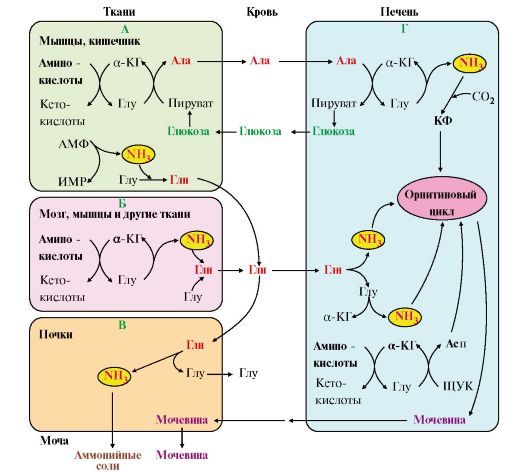 Рис. 9.8. Пути обмена азота аминокислот и аммиака: Рис. 9.8. Пути обмена азота аминокислот и аммиака:
А - выведение азота из мышц и кишечника в составе аланина и глутамина; Б - выведение азота из мозга и мышц в виде глутамина; В - экскреция аммиака из почек в виде аммонийных солей; Г - включение азота аминокислот в мочевину в печени
Глутаминаза почек активируется при ацидозе; образовавшийся аммиак используется для нейтрализации кислых продуктов и образования аммонийных солей [в основном, NH4Cl, (NH4)2SO4], которые экскретируются с мочой (рис. 9.9). Экскреция солей аммония в норме составляет -0,5 г/сут, при
ацидозе выведение аммонийных солей может увеличиться до 10 г/сут. Этот путь выведения аммиака:
• поддерживает кислотно-щелочной баланс в норме;
• защищает организм от потери с мочой ионов Na+ и К+, которые также могут использоваться для выведения избытка анионов.
 Рис. 9.9. Использование глутамина в почках для поддержания кислотно-щелочного баланса Рис. 9.9. Использование глутамина в почках для поддержания кислотно-щелочного баланса
5. В мозге и некоторых других органах для обезвреживания аммиака используется реакция восстановительного аминирования α-кетоглутарата под действием глутаматдегидрогеназы, которая катализирует реакцию, обратную окислительному дезаминированию глутамата. Однако этот путь в тканях используется слабо. Хотя, если учитывать возможность последующего образования глутамина, он является выгодным для клеток, так как способствует обезвреживанию сразу двух молекул NH3:
 6. Из мышц, клеток кишечника и некоторых других тканей избыток азота выводится в кровь в виде аланина (см. рис. 9.8, А, Г). Образование аланина в этих органах можно представить следующей схемой: 6. Из мышц, клеток кишечника и некоторых других тканей избыток азота выводится в кровь в виде аланина (см. рис. 9.8, А, Г). Образование аланина в этих органах можно представить следующей схемой:
 Аминогруппы разных аминокислот в ходе реакций трансаминирования переносятся на пируват, источником которого служат глюкоза и безазотистые остатки аминокислот. Особенно много аланина выделяют мышцы в силу их большой массы, а также потому, что работающие мышцы часть энергии получают за счет распада аминокислот. Аланин поступает в печень, Аминогруппы разных аминокислот в ходе реакций трансаминирования переносятся на пируват, источником которого служат глюкоза и безазотистые остатки аминокислот. Особенно много аланина выделяют мышцы в силу их большой массы, а также потому, что работающие мышцы часть энергии получают за счет распада аминокислот. Аланин поступает в печень,
где подвергается непрямому дезаминированию. Выделившийся аммиак обезвреживается в процессе синтеза мочевины, а пируват включается в глюконеогенез или ОПК. Глюкоза из печени поступает в ткани и в процессе гликолиза окисляется до пирувата. Образование аланина в мышцах, его перенос в печень и перенос глюкозы в обратном направлении составляют глюкозоаланиновый цикл (см. рис. 9.8, А, Г).
7. В печени аммиак обезвреживается путем связывания с СО2 и образования карбамоилфосфата (см. рис. 9.8, Г). Реакцию катализирует карбамоилфосфатсинтетаза I, которая использует 2 моль АТФ. Фермент локализован в митохондриях гепатоцитов. Продукт реакции - карбамоилфосфат - включается затем в орнитиновый цикл Кребса-Гензелейта для синтеза мочевины.
|