
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Производные бензолсульфокислотыСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте Бензолсульфокислота является весьма реакционноспособной и может образовывать различные производные и, соответственно, различные фармакологически активные вещества. В соответствии с этим будут рассмотрены несколько групп производных бензолсульфокислоты.
Производные n-аминобензолсульфокислоты Одной из первых групп бактериостатических средств синтетического происхождения были производные амида n-аминобензолсульфокислоты, которые в настоящее время объединяются одним названием – сульфаниламиды. Несмотря на то, что амид сульфаниловой кислоты был получен в 1908 г Гельмо исследование противомикробных свойств сульфаниламидов началось лишь в 30-е годы 20 столетия. Первый препарат пронтозил (красный стрептоцид, рубиазол) являлся азокрасителем и показал высокую противомикробную активность в отношении гемолитического стрептококка. Наибольший вклад в изучение сульфаниламидов внёс Домагк, который был удостоен Нобелевской премии в 1939 г. Одновременно, а именно в 30-е годы исследование сульфаниламидов началось в других странах в т.ч. в Германии и СССР. В СССР во ВНИХФИ под руководством М.В. Рубцова и О.Ю. Магидсона были синтезированы оригинальные препараты сульфидин, сульгин. В Свердловске над изучением сульфаниламидов работал И.Я. Постовский. В это время в Германии начались работы над промышленным выпуском сульфаниламидов. Со времени открытия сульфаниламидов было синтезировано более 10000 соединений. Хотя в медицинскую практику было введено около 2-х десятков эффективных соединений работы по изучению связи структуры и действия имели значение не только для этой группы, но и для фармацевтической химии вообще. Что же касается сульфаниламидов то выявлено следующее: 1. Аминогруппа и сульфамидная группа должны находиться только в n-положении. Если эти группы находятся в o- или м-положениях, то бактериостатическое действие практически исчезает. 2. Заместитель в аминогруппе должен легко отщепляться в организме, в противном случае действие сульфаниламида резко снижается. 3. Заместитель в сульфамидной группе должен метаболизироваться в организме, однако введение такого заместителя не только не снижает бактериостатического действия, но иногда повышает, а чаще всего пролонгирует действие сульфаниламида. Гипотеза о механизме действия сульфаниламидов была высказана в 40-е годы, когда рентгеноструктурным методом была изучена структура кислоты n-аминобензойной и n-аминобензолсульфамидов, а также электронная плотность вокруг отдельных атомов обеих структур. Приведенные ниже формулы показывают близость структурных характеристик n-аминобензой- ной кислоты и n-аминобензолсульфамидов
Сравнивая приведенные геометрические размеры, а также некоторые химические свойства было высказано, а затем доказано, что сульфаниламиды проявляют конкурентное действие в отношении n-аминобензойной кислоты при синтезе фолиевой кислоты. Фолиевая кислота с остатком n-аминобен-золсульфокислоты (псевдофолиевая) не может служить переносчиком формильной или гидроксиметильной групп при биосинтезе пуриновых и пиримидиновых оснований, что в конечном счёте приводит к блокированию биосинтеза нуклеиновых кислот в клетках патогенных микроорганизмов. Конкурентность n-аминобензойной кислоты и сульфаниламидов была доказана клинической практикой. При одновременном приёме производных n-аминобензойной кислоты и сульфаниламидов, активность последних снижается во много раз. Кроме того, применение кислоты фолиевой и производных пиримидина также снижает активность сульфаниламидов. Выясненные факты не могут полностью объяснить механизм действия сульфаниламидов. Всегда остаётся много вопросов. Например почему микроорганизмы не могут усваивать фолиевую кислоту человека и др. Поэтому наряду с высказанной гипотезой имеют право на существование и другие, например, влияние сульфаниламидов на проницаемость мембраны цитоплазмы бактерий. Остаётся сказать несколько слов о наличии радикала в сульфамидной группе. Несмотря на то, что основную роль играет амид n-аминобензойной кислоты радикал в амидной группе оказывает большое значение на проницаемость сульфаниламида через биологические барьера организма, сульфаниламида с белками плазмы, обратное всасывание сульфаниламида из первичной мочи и другие. Это всё оказывает влияние на длительность действия сульфаниламидов. В настоящее время значение сульфаниламидов в фармакотерапии несколько снизилось. Это связано с появлением более эффективных противомикробных средств – антибиотиков и появлением устойчивых к сульфаниламидам микроорганизмов.
Сульфаниламид Sulfanilamidum Стрептоцид
М.м.=172,2 n-аминобензолсульфамид амид сульфаниловой кислоты Для синтеза сульфаниламида как и большинства сульфаниламидных препаратов исходным продуктом служит анилин с защищённой аминогруппой. Его подвергают сульфохлорированию с помощью хлорсульфоновой кислоты. На последних стадиях вводят соответствующий амин (в данном случае аммиак) и проводят дезацетилирование
==========================????? Сульфаниламид - это белый с желтоватым оттенком порошок, мало растворим в воде и спирте, растворяется в минеральных кислотах и щелочах. Для установления подлинности сульфаниламида проводят реакции образования азокрасителя
оранжево-красное окрашивание Наличие серы устанавливают после нагревания сульфаниламида с азотной кислотой. Образовавшиеся сульфат-ионы обнаруживают по реакции с раствором бария хлорида
RSO2NH2 H2SO4; H2SO4 + BaCl2 → BaSO4↓ + 2HCl Сульфаниламид подвергается бромированию, нитрованию с образованием соответствующих производных. Сульфаниламид может вступать в реакцию с ароматическими альдегидами с образованием азометиновых красителей
жёлто-оранжевое окрашивание На этой реакции основана так называемая лигниновая проба. Так как лигнин содержит остаток ванилина, то на него наносят несколько кристалликов сульфаниламида и 1-2 мл раствора разведенной кислоты хлористоводородной - вокруг кристалликов появляется оранжевое пятно. Для количественного определения сульфаниламида описано несколько способов. Каждый из них имеет определённые преимущества. Однако наиболее приемлемыми оказались нитритометрический и броматометри- ческий. Нитритометрический метод проводят по общепринятой схеме: температура должна быть не выше +15 0С, среда кислая, индикатор–смесь тропеолина 00 и метиленового синего
Броматометрическое определение обычно проводят обратным методом
KBrO3 + 5KBr + 3H2 SO4 →3Br2 + 3K2SO4 + 3H2O Br2 + 2 KI → I2 + 2 KBr I2 + 2 Na2S2O3 → 2 NaI + Na2S4O6 Сульфаниламид оказывает противомикробное действие по отношению к стафилококкам, стрептококкам, менингококкам, кишечной палочке, возбудителям холеры, трахомы и др. Назначается внутрь в начальной дозе 1-2 г, а затем по 0,5 г 5-6 раз в день. В настоящее время применяется реже из-за выработки устойчивости микроорганизмов к сульфаниламид. Сохранил значение при поверхностных инфекциях кожи и слизистой оболочки и применяется в виде присыпки, мази и линимента. Выпускается сульфаниламид в пакетиках по 2 и 5г в виде порошка, в таблетках по 0,3 и 0,5, в виде мази 10%, линимента 5%.
М.м.=254,2 4-аминобензолсульфонилацетамид Сульфацетамид - натрий (альбуцид) - это белый или желтовато-белый кристаллический порошок, легко растворим в воде, мало растворим в спирте. Растворы препарата имеют слабо-щелочную реакцию (рН от8.0 до 9,5). Подлинность сульфацетамида-натрия подтверждают с помощью УФ- и ИК-спектроскопии. УФ-спектр сульфацетамида в фосфатном буферном растворе (рН=7) имеет полосу поглощения с максимумом при 255 нм. ИК–спектр должен совпадать с ИК-спектром стандартного образца сульфацетамида-натрия или с прилагаемым к НД. Препарат должен давать положительную реакцию на ионы натрия, на остаток уксусной кислоты. Сульфацетамид-натрий даёт другие реакции подобные реакциям на сульфаниламид. Для количественного определения сульфацетамида-натрия можно использовать нитритометрический метод, такой же как и для сульфаниламида. Другой метод заключается в нейтрализации сульфацетамида-натрия 0,1 М раствором кислоты хлористоводородной в среде метанола и ацетона в присутствии тимолового синего
Сульфацетамид-натрий является бактериостатическим средством. Применяется он в основном в глазной практике при гнойных язвах роговицы глаза, при коньюктивитах, гнойных заболеваниях глаз у новорожденных и взрослых. Выпускается сульфацетамид-натрий в основном в виде растворов 10%; 20% и 30% во флаконах.
Сульфадиметоксин Sulfadimethoxinum
М.м.=310,3 4-амино-N-(2,4-диметоксипиримидинил-6) – бензолсульфамид Стадии получения сульфадиметоксина такие же как и сульфаниламида.
Сульфадиметоксин - это белый или желтовато-белый кристаллический порошок, практически нерастворим в воде, мало растворим в спирте, хорошо растворим в минеральных кислотах и растворах щелочей. Для определения подлинности сульфадиметоксина используют реакции с сульфатом меди и хлоридом кобальта. При проведении этих реакций избыток щёлочи может исказить результаты реакций, поэтому при растворении препарата в растворе щёлочи всегда необходимо, чтобы сульфадиметоксин был в небольшом избытке
жёлтый осадок с зеленоватым оттенком С кобальта хлоридом образуется комплексное соединение такой же структуры, но ярко-розового цвета. Другие испытания на подлинность такие же как и у сульфаниламида. Количественное определение сульфадиметоксина проводят нитритометрическим методом. Применяется сульфадиметоксин как противомикробное средство. Показания к применению сульфадиметоксина такие же как и у других сульфаниламидных препаратов. Действие его более длительное. Это связано с его реабсорбцией в почеч ных канальцах. Сульфадиметоксин выпускается в таблетках по 0,2 и 0,5 г.
Сульфален
2-(n-аминобензолсульфамидо)-3-метоксипиразин Сульфален получают по такой же схеме как и другие сульфамидные препараты. Сульфален представляет собой белый или желтовато-белый порошок, практически нерастворимый в воде, легко растворим в растворах щелочей и минеральных кислот. Подлинность сульфалена определяют с помощью УФ- и ИК-спектроскопии. УФ-спектр сульфалена в 0,1 М растворе натрия гидроксида имеет полосу поглощения с максимумом при 325 нм, в 0,1 М растворе кислоты хлористоводородной – при 289 нм. ИК–спектр должен совпадать с ИК-спектром стандартного образца сульфалена или с прилагаемым к НД. Реакцию с раствором меди сульфата проводят так же как и с сульфадиметоксином – образуется осадок грязно-зелёного цвета, постепенно переходящий в голубовато-зелёный. Другие реакции проводят также как и на все сульфаниламидные препараты. Количественное определение сульфалена проводят нитритометрическим методом. Сульфален является бактериостатическим средством. Его назначают при заболеваниях вызванных чувствительными к препарату возбудителями: при пневмонии, трахоме, бронхите, холецистите, уретрите и др. Его отличительной особенностью является высокая степень реабсорбции из почечных канальцев. При острых инфекциях его назначают ежедневно, при хронических – один раз в 7-10 дней, в дозах от 0,2 до 1,0 г. Выпускается сульфален в таблетках по 0,2г.
Фталилсульфатиазол Рhthalylsulfathiazolum Фталазол Рhthalazolum
2 – (n – фталиламинобензолсульфамидо) – тиазол 4-(фтазолил-2-сульфамоил) фталевая кислота Получают фталилсульфатиазол путём ацилирования сульфатиазола с помощью фталевого ангидрида
Фталилсульфатиазол представляет собой белый или слегка желтоватый порошок, нерастворим в воде, легко растворим в растворах щелочей, мало растворим кислотах. Характерной реакцией для испытания на подлинность фталилсульфатиазола является реакция образования флюоресцеина. Её проводят путём сплавления фталилсульфатиазола с резорцином в присутствии нескольких капель кислоты серной концентрированной. После этого плав разбавляют значительным количеством воды с несколькими каплями раствора щёлочи – в результате появляется зелёная флюоресценция. Другие продукты реакции после сплавления с концентрированной серной кислотой не изучались
Реакция образования азокрасителя проводится после предварительного гидролиза в присутствии раствора натрия гидроксида. ИК–спектр фталилсульфатиазола должен быть идентичным с ИК-спектром стандартного образца. Количественное определение фталилсульфатиазола проводят в среде диметилформамида путём титрования 0,1 М раствором натрия гидроксида (индикатор – тимоловый синий)
Фармакологическое действие фталилсульфатиазола такое же как и у других сульфамидных препаратов. Однако он плохо растворяется в воде и кишечнике, поэтому практически не всасывается. Его применяют при кишечных инфекциях: дизентерии, колитах и для профилактики кишечных инфекций после операционных вмешательств. Обычно дозы фталилсульфатиазола находятся в пределах от 0,1 до 1,0 г. Выпускается фталилсульфатиазол в таблетках по 0,5 г.
Сульфасалазин Sulfasalazine
М.м.=398,4 2-(n-салицилазобензолсульфониламидо) пиридин или 5-[4-N-(2-пиридилсульфомоилфенил)-азо] салициловая кислота Сульфасалазин - это ярко-жёлтый кристаллический порошок практически нерастворим в воде, мало растворим в спирте, легко растворим в растворах щелочей Для испытания на подлинность используют УФ- и ИК-спектроскопию. УФ-спектр сульфасалазина в 0,1 М растворе натрия гидроксида имеет две полосы поглощения с максимумами при 238 и 359 нм. ИК–спектр сульфасалазина должен совпадать с ИК-спектром стандартного образца или со спектром, прилагаемым к НД.
оранжево-красное окрашивание Количественное определение сульфасалазина в субстанции можно провести методом нейтрализации в среде диметилформамида. Конец титрования обычно определяют потенциометрическим методом. Схема реакций такая же как у предыдущего препарата. В лекарственной форме определяют сульфасалазин спектрофотометрическим методом в 0,1 М растворе натрия гидроксида при длине волны 359 нм. Сульфасалазин плохо всасывается из кишечника. Поэтому его применяют в основном при язвенном колите. В кишечнике он медленно расщепляется микрофлорой до сульфанилпиридина и 5-аминосалициловой кислоты, которые оказывают противомикробное и противовоспалительное действие. Выпускается сульфасалазин в таблетках по 0,5г.
Ко-тримазол Co-trimazolum Бисептол Biseptol Ко-тримазол, который в РФ более известен как бисептол или бактрим, является комбинированным препаратом и содержит в своём составе два вещества: сульфаметоксазол и триметоприм в отношении 5:1
5-метил-3(n-аминобензолсульфамидо)- 2,4-диамино-5(3,4,5-три- -изооксазол метоксибензил) пиримидин Ко-тримазол оказывает противомикробное действие по отношению к микроорганизмам, устойчивым к другим сульфамидным препаратам. Подлинность бактрима устанавливают по реакциям, характерным для сульфамидов и триметоприма. Триметоприм отделяют с помощью хлороформа и регистрируют УФ-спектрпоглощения с максимумом при 246 нм. Количественное определение сульфаметоксазола проводят нитритометрическим методом (как и других сульфамидных препаратов). Триметоприм определяют путём титрования 0,1 М кислотой хлорной в безводной кислоте уксусной в смеси с уксусным ангидридом. Ко-тримазол применяют при инфекциях дыхательных путей, желудочно-кишечного тракта, мочевыводящих путей. Выпускается ко-тримазол в таблетках по 0,12 и 0,48 г.
|
|||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-08; просмотров: 3351; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.108 (0.008 с.) |


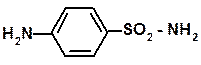 Streptocidum
Streptocidum





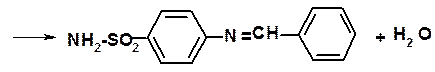
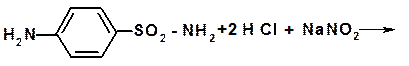

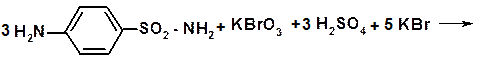
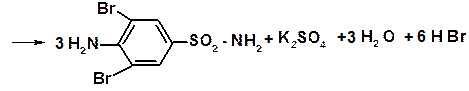
 Сульфацетамид - натрий
Сульфацетамид - натрий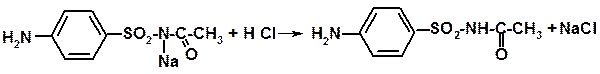

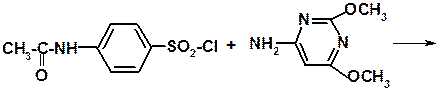 На последних стадиях вместо аммиака используют 6-амино,2,4-диметоксипиримидин
На последних стадиях вместо аммиака используют 6-амино,2,4-диметоксипиримидин


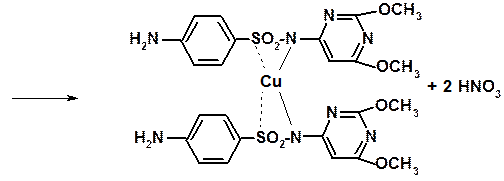
 Sulfalenum
Sulfalenum
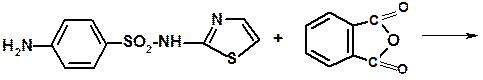

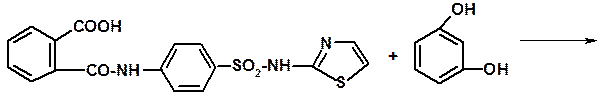


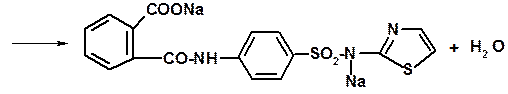

 Для идентификации сульфасалазина можно провести реакцию образования азокрасителя. Для этого вначале проводят восстановление сульфасалазина цинковой пылью в кислой среде (можно использовать гранулированный цинк) до ароматического амина, а затем проводят реакцию образования азокрасителя по обычной схеме
Для идентификации сульфасалазина можно провести реакцию образования азокрасителя. Для этого вначале проводят восстановление сульфасалазина цинковой пылью в кислой среде (можно использовать гранулированный цинк) до ароматического амина, а затем проводят реакцию образования азокрасителя по обычной схеме







