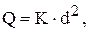Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Відбирання проби твердих речовинСодержание книги
Поиск на нашем сайте
Під час відбирання генеральної, лабораторної та досліджуваної проби твердих речовин виникає питання про розмір проби. Оптимальна маса проби обумовлена неоднорідністю досліджуваного об’єкту, розміром частинок, з яких починається неоднорідність та вимогами до точності аналізу, які звичайно, визначають за похибкою у відбиранні проби. Залежність маси представницької проби від розміру (діаметру, d) неоднорідних частинок проілюстрована нижче: d, мм 40-50 25 10 5 3 2 1 Q, кг 50-3×103 10-700 2-100 0,5-25 0,2-10 0,1-5 0,02-1 Для розрахунку оптимальної маси представницької проби існує декілька прийомів. Часто використовують формулу Річердса-Чеччота:
де Q - маса проби, яка забезпечує показність, кг; d - найбільший діаметр неоднорідних частинок, мм; К - емпіричний коефіцієнт пропорційності, що характеризує ступінь неоднорідності розподілу визначаємого компоненту в матеріалі, змінюється у межах 0,02 - 1. Способи відбору генеральної проби твердої речовини різні для речовин, які знаходяться у вигляді цілого чи подрібненого продукту. Після відбирання генеральної проби твердої речовини здійснюють процес гомогенізації, який включає операції подрібнення та просівання. Ці операції чередуюють до тих пір, доки не одержать достатньо розтерту однорідну пробу. Наступний етап відбирання проби ¾ усереднення, яке включає операції перемішування та скорочення проби. Перемішування може проводитись механічно, за методом конуса та кільця. Скорочення проби проводять різними способами. Цей процес, як правило, багатостадійний, включає повторне перемішування та розподіл.
Переведення проби у розчин Сучасні методи підготовки проби базуються на використанні високо активних реагентів, збільшених тиску та температури, каталізу, випромінювань різного типу. Вибір способу розкладання проби та переведення її компонентів у розчин залежать від деяких факторів, які необхідно враховувати під час обгрунтування схеми хімічного аналізу. Перед усім звертають увагу на неорганічну чи органічну природу основи об’єкту (матріца), хімічний склад зразку, хімічні властивості компонента, що визначають. Спосіб розкладання проби та переведення її у розчин залежить від мети аналізу. Так, різним чином проводять пробопідготовку під час елементного та функціонального аналізу органічних сполук; під час визначення загального вмісту будь-якого елементу (залізо, хром) та його форм у різному ступені окиснення (ферум(ІІ) та ферум(ІІІ), хром(ІІІ) та хром(VI)), а також основних компонентів зразку та домішок у ньому.
Спосіб розкладання та переведення проби в багатьом визначається вибраним аналітичним методом. Наприклад, пробопідготовка під час визначення органічних сполук у біологічних об’єктах хроматографічним та спектрофотометричними методами розрізняється. Після вибору способу розкладання проби необхідно оцінити усі можливі похибки на цій стадії аналізу. Найбільш типові похибки обумовлені втратами летучих компонентів під час використання високих температур; забрудненням із матеріалів посуду та пристріїв для розкладання проб; наявністю заважаючих проведенню аналізу домішок у реактивах та розчинниках, що використовують для розкладання зразків. Способи розкладання поділяють на “сухі” та “мокрі”: до перших відносять термічне розкладання, сплавлення та зпікання з різними речовинами (солі, оксиди, луги та їх суміші); до других ¾ розчинення досліджуваної проби у різних розчинниках, переважно у кислотах та сумішах. Розчинення У найкращому випадку розчинник повинен розчиняти пробу швидко, у достатньо м’яких умовах і не заважати на слідуючих стадіях аналізу. Найкращий розчинник ¾ вода. Багато неорганічних солей та деякі органічні сполуки (нижчі та багатоатомні спирти, амінокислоти, гідрохлориди амінів, солі лужних металів органічних кислот, сечовина) легко розчиняються у воді. Іноді у воду додають невелику кількість кислоти для запобігання гідролізу та часткового осадження деяких катіонів металів. У окремих випадках для розчинення органічних речовин використовують суміш води та органічного розчинника, що змішується з нею (наприклад, суміш води та етанолу). Для розчинення органічних сполук застосовують органічні розчинники. Як правило, це спирти, хлоровані вуглеводні, кетони. Так, для розчинення полімерних матеріалів різного типу використовують диметилформамід, диметил ацетамід, метилізобутилкетон, метанол. Під час “мокрого” способу розкладання проби часто застосовують різні кислоти та їх суміші за умов нагрівання. При цьому в пробу не вводять сторонні катіони; а самі кислоти порівняно легко видаляються з сфери реакції за умов нагрівання. Кислоти в залежності від їх природи та концентрації можуть проявляти окисні (конц. HNO3 та H2SO4) чи комплексоутворюючі властивості (HF та H3PO4). Кислоти та їх суміші, які найбільш часто використовують для розчинення представлені у таблиці 7.
Таблиця 7
|
||||||
|
Последнее изменение этой страницы: 2017-02-05; просмотров: 597; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.133.109.183 (0.01 с.) |