Химиялық заттардың энергетикасы
Жұмыстың мақсаты: Химиялық реакция энергетикасын калориметрия өлшеп және термодинамикалық есептеу арқылы анықтау.
Жұмысты жүргізу:
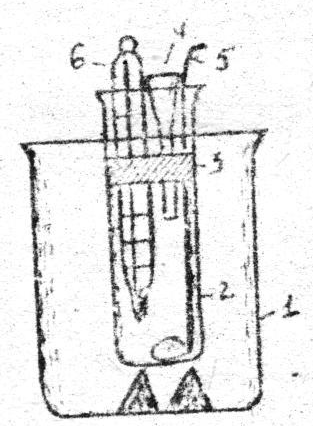 Химиялық реакцияның энтальпиясын калориметр деген құрал арқылы өлшейді. 1- сыртқы стакан, 2- реакция жүретін стакан, 3- қақпақ, 4- воронка, 5- ерітінді араластыратын құрал, 6-термометр. Химиялық реакцияның энтальпиясын калориметр деген құрал арқылы өлшейді. 1- сыртқы стакан, 2- реакция жүретін стакан, 3- қақпақ, 4- воронка, 5- ерітінді араластыратын құрал, 6-термометр.
Күшті қышқылды күшті негізбен нейтралдау реакциясының энтальпиясы және реакцияның Гиббс энергиясын есептеу. Электролиттік диссоциация теориясы бойынша күшті қышқыл мен күшті негіз арасында мынадай реакция жүреді:
NaOH + HCl = NaCl + H2O
NaOH + HNO3 = NaNO3 + H2O
№4 сурет Калориметр
Нейтралдау реакциясының термохимиялық теңдеуін былай жазуға болады:
Н+ + ОН- =Н2О: ΔН=-57 кДж
Нейтралдау реакциясы үшін бірдей көлемдер алу керек, мысалы: 100 мл қышқыл, 100 мл негіз.
Реакция жүретін стаканға (2) негіздің белгілі көлемін (20 мл концентрациясы 1 М) құйыңдар да температурасын 0,10К дәлдікке дейін өлшеңдер (Т1), оны зертханалық дәптерге жазыңдар. (Қышқылдыңда температурасын осындай дәлдікпен өлшеңдер, екі температура тең болуы керек). Сондай көлем (20 мл) қышқылды кұйып (1М) араластырып, ең жоғары температураны өлшеңдер (Т2). Тәжірибе нәтижесін кестеге жазыңдар:
Жүйе
Стакандағы жалпы көлем, V мл
Т1, К
Т1, К
Т = Т2- Т1
NaOH
HCl
NaOH
HNO3
Тәжірибе нәтижесінен мыналарды анықтаңдар:
1.Температуралар айырмашылығын ΔТ = Т2- Т1
2.Стакандағы ерітіндінің массасын (m) (ерітінді тығыздығын бірге тең деп алыңдар).
3.Реакция нәтижесінде бөлінген жылуды (q): q= C∙m∙ΔT
C- ерітіндінің жылу көлемі 4,18 кДж (кг∙К) m- ерітінді массасы
Тәжірибе нәтижесінде табылған жылу мөлшері 0,1 моль сілтіні нейтралдағандағы жылу мөлшері болып табылады.
4.1 моль үшін нейтралдау энтальпиясы (кДж/моль);
ΔНнейтралдау = -q/0,1 кДж/моль
5.Теория бойынша нейтралдау энтальпиясы ΔНнейтралдау = -57 кДж/моль болса, салыстырмалы қате %қате = ((ΔНтеор. – ΔНтәж.)/ ΔНтеор.)∙100
6.Энтропия мәндерін кестеден тауып, нейтралдау реакциясының энтропиясының өзгеруін табыңдар
7.Нейтралдау реакциясының Гиббс энергиясын есептеңдер.
ΔG = ΔH + TΔS
Күшті қышқыл мен күшті негіз әрекеттескенде неге энтропия азаяды, соны түсіндіріңдер.
Табылған ΔН, ΔS, ΔG мәндеріне сүйеніп, нейтралдау реакциясы өздігінен жүретіндігі туралы қорытынды жасаңдар.
Өзін өзі бақылауға және зертханалық жұмыстарды қорғауға арналған сұрақтар:
1.Термохимия нені зерттейді?
2.Экзотермиялық және эндотермиялық деп қандай реакцияларды айтады?
3.Гесс заңын және оның салдарын айтып беріңіз.
4.Ішкі энергия деген не?
5.Энтальпия деген не және оның физикалық мәні қандай?
6.Термодинамиканың бірінші заңын айтып беріңіз.
Энтропия деген не? Стандартты энтропия деген не? Энтропиялық бірлік деген не?
7.Изобаралы-изотермиялық потенциал деп немесе Гиббс энергиясы деп қандай шаманы айтады? ∆G қандай бірлікпен өлшенеді?
8.Жүйенің энтропиялық және энтальпиялық факторлары деген не?
9.ΔН пен ΔS байланысы қандай теңдеумен өрнектеледі?
№ 4 Зертханалық сабақ
|