
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Алкены, строение, гомологический ряд.Содержание книги
Поиск на нашем сайте
Углеводороды ряда этилена содержат одну двойную связь и отличаются от предельных на 2 атома Н. Алкены – по номенклатуре ИЮПАК. Общая формула
С2Н4 этилен этен С3Н6 пропилен пропен С4Н10 бутилен бутен С5Н10 амилен пентен
Н2С = СН2sp2- гибридизация
Вспоминаем sp2- гибридизацию образования π- связи. При sp2- гибридизации происходит смешение одной 2s и двух 2р- орбиталей. Образовавшиеся три гибридные орбитали расположены в одной плоскости под углом 1200. Третья 2р- орбиталь сохраняет свою форму, так как не участвует в гибридизации и располагается в плоскости перпендикулярной плоскости гибридных связей. В результате перекрывания р-орбиталей соседних углеродных атомов образуется π- связь. Площадь перекрывания 2р-электронных орбиталей при образовании π- связи меньше, чем sp2- гибридных при образовании σ-связей, и, следовательно, π- связь менее прочна и более реакционноспособна, чем σ-связь. Поэтому π- связи реагируют в первую очередь.
 




Два вида изомерии: изомерия углеродного скелета и изомерия положения двойной связи. СН2 = СН2 СН2 = СН- СН3
Пентен имеет пять изомеров. Физические и химические свойства алкенов. Физические свойства закономерно изменяются в гомологическом ряду. Температура кипения несколько ниже чем у соответствующих предельных углеводородов, а плотность выше. Первые три члена (С2- С4) – газы, С5 – С17 – жидкости, С18 – и выше твердые вещества. Этилен и пропилен без заметного запаха, а остальные гомологи обладают резким неприятным запахом. Температура кипения и температура плавления алкенов нормального строения возрастают по мере увеличения молекулярной массы. Углеводороды нормального строения кипят при более высокой температуре, чем углеводороды изостроения. Олефины мало растворимы в воде, хорошо растворяются в органических растворителях. Все они хорошо горят. Этилен и пропилен горят коптящим пламенем, с воздухом образуют взрывоопасную смесь. Химические свойства Химические свойства алкенов определяются наличием двойной связи. Электронная плотность σ-связи концентрируется по линии, соединяющей ядра атомов, а электронная плотность π- связи выходит за эти пределы, образуя более обширную область отрицательного заряда. π- электроны более подвижны, менее прочно удерживаются ядрами атомов, чем σ- электронов. Поэтому π- связь легче поляризуется. π- электроны легко вовлекаются в реакции электрофилами, которые возбуждая поляризацию π- связи, вызывают ее гетеролитический разрыв. Для алкенов в отличии от алканов характерны реакции присоединения, окисления, полимеризации. Реакции присоединения Большинство реакций присоединения к С = С идет по гетеролитическому типу, является реакциями электрофильного присоединения и приводит к образованию предельных соединений. а) гидрирование (присоединение водорода)
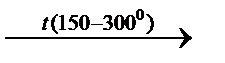 СnH2n + 2 СnH2n + 2
 CH3 – CH3 CH3 – CH3
б) галогенирование (присоединение галогенов) CH2 = CH2 + Cl – Cl → Cl - CH2 - CH2 – Cl Реакции с бромом используются как качественные реакции для открытия непредельных углеводородов. (Вспоминаем лабораторную работу) в) присоединение галогеноводорода CH2 = CH2 + НCl →CH3 - CH2Cl
|
|||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-28; просмотров: 592; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.118.0.93 (0.006 с.) |




 Изомерия начинается с третьего члена гомологического ряда.
Изомерия начинается с третьего члена гомологического ряда.



