Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Этиленгликоль, получение, значениеСодержание книги
Поиск на нашем сайте
Этиленгликоль – вязкая бесцветная жидкость, сладкая на вкус, tk = 1980С. Сильно понижена температура замерзания воды. 60% раствор гликоля замерзает при -490С. Применяется для приготовления антифриза. Этиленгликоль очень гигроскопичен, поэтому его применяют при изготовлении печатных красок, динитроэтиленгликоль – сильное взрывчатое вещество. В промышленности этиленгликоль получается из окиси этилена
С двухосновными кислотами этиленгликоль вступает в реакцию поликонденсации, образуя высокомолекулярные полиэфиры:
НО – С = О OO | || || R → O - СН2 - СН2 – O- C – R – C - + 2nH2 | НО – С = О n Полиэфиры этиленгликоля широко применяется в различных отраслях промышленности, как пленкообразующие вещества для лаков и красок, в производстве пластмасс, синтетических волокон (лавсан). Этиленгликоль применяется в производстве полиуретановых смол, применяется для изготовления клеев, лаков, синтетических смол, синтетического каучука. В 1906 г. А.Е.Фаворский перегоняя этиленгликоль с серной кислотой получил циклический эфир диоксан.
Диокасан – жидкость, tk = 1010С, растворим в воде в любых отношениях. Применяется как растворитель, в органическом синтезе ядовит. При хранении образует взрывоопасное вещество. Глицерин, его значение: нитроглицерин, динамит, применение. СН2OH – СНОН - СН2ОН-1,23пропан триол. Глицерин получается из жиров или синтезом из пропилена или ацетилена.

м
Глицерин - нейтральная вязкая бесцветная жидкость, сладкая на вкус, tпл = 170С, пл – 1,26, очень гигроскопичен. Смешивается с водой в любых отношениях. При атмосферном давлении кипит при tпл = 2900С. Химические свойства В глицерине 3 гидроксильные группы. Водородные атомы гидроксильных групп замещаются на металлы при действии не только щелочных металлов, но и гидроксидов железа, меди, Ca, Ba и др. Полные соединения называются глицератами (как с этиленгликолем).
 При взаимодействии глицерина с неорганическими и органическими кислотами образуются полные и неполные сложные эфиры.
O
3 НО – С – CH3
СН2OH – СН2 – СН = О СН2 = СН - акролеин.
Фенол. Физические и химические свойства фенола.Взаимное влияние атомов в молекуле фенола: взаимодействие с гидроксидом натрия и азотной кислотой. Применение фенола на основе свойств. Фенолы – это вещества, в которых гидроксогруппа соединена непосредственно с бензольным кольцом. Назовите молекулярную формулу фенил-радикала: C6H5 – фенил. Если к этому радикалу присоединить одну или несколько гидроксильных групп, то мы получим фенолы. Обратите внимание на то, что гидроксильные группы должны быть непосредственно связаны с бензольным кольцом, в противном случае мы получим ароматические спирты.
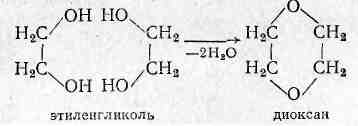
Классификация Так же как и спирты, фенолы классифицируют по атомности, т.е. по количеству гидроксильных групп. Одноатомные фенолы, содержат в молекуле одну гидроксильную группу:
Многоатомные фенолы содержат в молекулах более одной гидроксильной группы:
Самый главный представитель этого класса – фенол. Название этого вещества и легло в основу названия всего класса – фенолы. Многие из вас в скором будущем станут врачами, поэтому о феноле они должны знать как можно больше. В настоящее время можно выделить несколько основных направлений использования фенола. Один из них – производство лекарственных средств. Большинство этих лекарств — производные получаемой из фенола салициловой кислоты: o-HOC6H4COOH. Самое распространенное жаропонижающее — аспирин не что иное, как ацетилсалициловая кислота. Эфир салициловой кислоты и самого фенола тоже хорошо известен под названием салол. При лечении туберкулеза применяют парааминосалициловую кислоту (сокращенно ПАСК). Ну и, наконец, при конденсации фенола с фталевым ангидридом получается фенолфталеин, он же пурген.
Фенолы – органические вещества, молекулы которых содержат радикал фенил, связанные с одной или несколькими гидроксигруппами. Как вы считаете, почему фенолы выделили в отдельный класс, хотя они содержат ту же гидроксильную группу, что и спирты? Их свойства сильно отличаются от свойств спиртов. Почему? Атомы в молекуле взаимно влияют друг на друга. (Теория Бутлерова). Бензольное кольцо изменило свойства гидроксогруппы! Рассмотрим свойства фенолов на примере простейшего фенола. История открытия В 1834г. немецкий химик-органик Фридлиб Рунге обнаружил в продуктах перегонки каменноугольной смолы белое кристаллическое вещество с характерным запахом. Ему не удалось определить состав вещества, сделал это в 1842г. Огюст Лоран. Вещество обладало выраженными кислотными свойствами и было производным открытого незадолго до этого бензола. Лоран назвал его бензол феном, поэтому новая кислота получила название фениловой. Шарль Жерар считал полученное вещество спиртом и предложил называть его фенолом. Физические свойства Фенол C6H5OH (карболовая кислота) — бесцветное кристаллическое вещество, tпл = 430C, tкип = 1820C, на воздухе окисляется и становится розовым, при обычной температуре ограниченно растворим в воде, выше 66 °C смешивается с водой в любых соотношениях. Фенол — токсичное вещество, вызывает ожоги кожи, является антисептиком, поэтому с фенолом необходимо обращаться осторожно! Сам фенол и его пары ядовиты. Но существуют фенолы растительного происхождения, содержащиеся, например, в чае. Они благоприятно действуют на организм человека. Следствием полярности связи О–Н и наличия неподеленных пар электронов на атоме кислорода является способность гидроксисоединений к образованию водородных связей Это объясняет, почему у фенола довольно высокие температуры плавления (+43) и кипения (+182). Образование водородных связей с молекулами воды способствует растворимости гидроксисоединений в воде. Способность растворяться в воде уменьшается с увеличением углеводородного радикала и от многоатомных гидроксисоединений к одноатомным. Метанол, этанол, пропанол, изопропанол, этиленгликоль и глицерин смешиваются с водой в любых соотношениях. Растворимость фенола в воде ограничена. Изомерия и номенклатура Возможны 2 типа изомерии: · изомерия положения заместителей в бензольном кольце; · изомерия боковой цепи (строения алкильного радикала и числа радикалов). Химические свойства Посмотрите внимательно на структурную формулу фенола и ответьте на вопрос: «Что такого особенного в феноле, что его выделили в отдельный класс?» Т.е. фенол содержит и гидроксильную группу и бензольное кольцо, которые, согласно третьему положению теории А.М. Бутлерова, влияют друг на друга. Свойствами каких соединений формально должен обладать фенол? (спиртов и бензола.) Химические свойства фенолов обусловлены именно наличием в молекулах функциональной гидроксильной группы и бензольного кольца. Поэтому химические свойства фенола можно рассмотреть как по аналогии со спиртами, так и по аналогии с бензолом. Вспомните, с какими веществами реагируют спирты.
|
|||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-28; просмотров: 726; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.118.19.89 (0.011 с.) |


 СН2 - СН2 + СН2OH - СН2ОН
СН2 - СН2 + СН2OH - СН2ОН
 Синтез глицерина из пропилена
Синтез глицерина из пропилена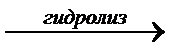

 ||
||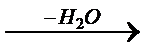 Большое практическое значение имеют полиэфиры глицерина и ароматической двухосновной кислоты (фталевые кислоты). Эти полиэфиры глицеринофталевые смолы (глифтали) применяются для изготовления лаков. При дегидратации глицерина (нагревание с гидросульфатом калия и некоторыми другими водоотнимающими средствами) образуется неправильный альдегил акролеин.
Большое практическое значение имеют полиэфиры глицерина и ароматической двухосновной кислоты (фталевые кислоты). Эти полиэфиры глицеринофталевые смолы (глифтали) применяются для изготовления лаков. При дегидратации глицерина (нагревание с гидросульфатом калия и некоторыми другими водоотнимающими средствами) образуется неправильный альдегил акролеин.