Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Вопросы для повторения. Физиологические основы системы гемостаза и ее составные компонентыСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
1. Физиологические основы системы гемостаза и ее составные компоненты (сосудистая стенка, тромбоциты, системы сверты- вания крови), их роль. 2. Сосудисто-тромбоцитарная фаза тромбообразования. Факторы, способствующие и препятствующие адгезии и агрегации тром- боцитов. 3. Характеристика коагуляционного гемостаза. Стадии свертыва- ния крови. Виды тромбов, их характеристика. 4. Противосвертывающая (антикоагулянтная и плазминовая, или фибринолитическая) системы. 5. Особенности гемостаза в детском возрасте.
К О Н Т Р О Л Ь Н Ы Е В О П Р О С Ы
1. Патология гемостаза. Общая характеристика (классифика- ция) гемостазиопатий. 2.Тромбофилические состояния. 3.Триада Вирхова. Причины, вызывающие нарушение сосуди- стой стенки, нарушение баланса между свертывающей и проти- восвертывающей системами крови, а также нарушение реологи- ческих свойств крови. Значимость отдельных факторов триады Вирхова в тромбообразовании. 4.Первичные (наследственные) и вторичные (приобретенные) тромбофилии. Антифосфолипидный синдром. 5.Исходы и последствия тромбообразования. 6.Методы изучения сосудистого, тромбоцитарного и коагуля- ционного звеньев гемостаза. Агрегатограмма. Тромбоэластогра-
фия. Клиническое значение. Основные показатели и характер их изменений при тромбофилических нарушениях системы гемоста- за. 7.Эмболия. Виды экзогенных и эндогенных эмболий. Ретро- градная и парадоксальная эмболии. 8.Тромбоэмболия. Источники тромбоэмболов сосудов боль- шого круга кровообращения и бассейна легочной артерии.
СИСТЕМА ГЕМОСТАЗА
Система гемостаза – это совокупность функционально- морфологических и биохимических механизмов, поддерживаю- щих кровь внутри сосуда в жидком состоянии и обеспечивающих остановку кровотечения при повреждении сосуда (Иванов Е.П., 1983 в модиф.).
В осуществлении гемостаза принимают участие: сосудистая стенка; форменные элементы крови, в первую очередь тромбо-
циты;
свертывающая система крови (коагулянты); противосвертывающая система крови (антикоагулянты
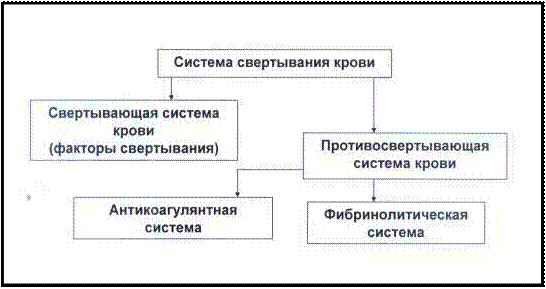
Рис. 60. Функциональные элементы системы свертывания крови
Выделяют два вида гемостаза: первичный (сосудисто- клеточный, или сосудисто-тромбоцитарный) и вторичный (коагу- ляционный, или биохимический). Сосудистая стенка (эндотелий и субэндотелиальный слой) вместе с тромбоцитами осуществляет первичный сосудисто- тромбоцитарный гемостаз. Вторичный гемостаз осуществляется при участии сверты- вающих плазменных факторов крови, а также компонентов про- тивосвертывающей системы (рис. 60).
Первичный (сосудисто-тромбоцитарный) гемостаз
Роль сосудистой стенки в гемостазе
В процессе первичного гемостаза принимают участие все компоненты сосудистой стенки: эндотелий, субэндотелиальный слой, гладкомышечные клетки. Неповрежденный эндотелий обладает антикоагулянтной, антитромботической активностью (тромборезистентность) и
Подложка
Рис. 61. Сосудистая стенка в гемостазе
Антикоагулянтная активность эндотелия обусловлена – наличием:
– синтезом: оксида азота (вазодилататор и антиагрегант);
PgI2 – простациклина (мощный ингибитор агрегации тромбоцитов и вазодилататор); гликопротеина тромбомодулина – активатора протеинов
С и S;
тканевого активатора плазминогена (t-PA) – стимулятор
фибринолиза; ангиокиназы – активатор плазминогена; урокиназы с тромболитической активностью; протеина S (ингибитор комплексов IXa-VIIIa и Xa-Va, а также стимулятор протеина С);
Под влиянием различных патологических факторов (экзо- и эндотоксины, атеросклеротический процесс, иммунные комплек- сы, медиаторы воспаления, протеолитические ферменты и др.) происходит повреждение эндотелия сосудов, что ведет к сниже- нию его антикоагулянтных и усилению прокоагулянтных свойств. В поврежденном эндотелии обнажается субэндотелиальный коллаген, в контакте с которым активируются тромбоциты и сис- тема свертывания крови. Прокоагулянтнаяактивностьэндотелия обеспечивается
- продукцией: фактора Виллебранда; тромбоксана А2;
цитокинов (фактор некроза опухолей и интерлей- кин-1); факторов свертывания крови (V, XI, фибриноген); ингибиторов активатора плазминогена; эндотелина-1 (вазоконстриктор и агрегант); ангиотензина-II; - активацией фактора XII.
В ответ на повреждение тканей под влиянием активных ве- ществ, вырабатываемых сосудистой стенкой и тромбоцитами (се- ротонин, тромбоксан А2, эндотелины), микрососуды спазмируют- ся, что приводит к временному запустеванию капилляров и венул и кровотечение из них в первые 20-30 с приостанавливается. Обнажение субэндотелиального слоя, состоящего из базаль- ной мембраны, коллагена, эластиновых волокон, протеогликанов, неколлагеновых гликопротеинов (фибронектина, фактора фон Виллебранда, тканевого тромбопластина), при повреждении эн- дотелия способствует уменьшению антиадгезивных свойств эн- дотелия, прилипанию к сосудистой стенке тромбоцитов, их акти- вации, секретированию содержимого гранул, агрегации, образо- ванию тромбоцитарного тромба и активации системы свертыва- ния крови (рис. 62). Важнейший индуктор агрегации тромбоци- тов – аденозиндифосфат (АДФ), простагландин – тромбоксан А2 и другие биологические вещества. Рефлекторное сокращение гладкомышечных клеток под- держивается биологически активными веществами, высвобож- дающимися из тромбоцитов и эндотелиальных клеток (PgF2α, эн- дотелины и др.).
Тромбоциты (кровяные пластинки) – безъядерные формен- ные элементы (d 2–4 мкм) с продолжительностью жизни до 7–10 дней (рис. 62).
Рис. 62. Тромбоциты в электронном микроскопе
Содержание тромбоцитов в периферической крови состав- ляет (180–320) × 109/л – при ручном подсчете в мазках крови и (150–450) × 109/л – при подсчете с помощью автоматических ана- лизаторов. Тромбоциты играют ключевую роль в сосудисто- тромбоцитарном гемостазе. Материнскими клетками тромбоцитов являются находящие- ся в костном мозге мегакариобласты. Это большие клетки (диа- метром 20-25 мкм) с очень большим ядром. Ядро мегакариобла- ста округлое, занимает большую часть клетки, хроматин имеет нежную структуру, содержит 1-3 нуклеолы. Цитоплазма окружа- ет ядро узким ободком, базофильная, беззернистая. Мегакариоб- ласты постепенно теряют способность к делению, но продолжают репликацию ДНК (эндомитоз). Следующие стадии созревания – промегакариоцит, мегакариоцит, тромбоцит. Мегакариоцит – клетка гигантских размеров, диаметр 30- 120 мкм. Ядро – причудливой формы, структура хроматина плот- ная, многодольчатая, с обилием складок, вырезов, резких углуб- лений. Цитоплазма – голубая, серая, сиренево-розовая. По мере созревания мегакариоцита в цитоплазме появляют- ся гранулы и цитоплазма разделяется демаркационными перего- родками на полоски, напоминающие четки из отдельных тромбо- цитов, из которых образуются выпячивания цитоплазмы мегака- риоцитов (псевдоподии), которые проходят через миграционные поры эндотелия костномозговых синусов в циркуляцию, где рас- падаются на тромбоциты (рис. 63). Каждый мегакариоцит спосо- бен продуцировать около 1000-2000 тромбоцитов.
a б
Рис. 63. Зрелый мегакариоцит без отшнуровки тромбоцитов (а); мегакариоцит с отшнуровкой тромбоцитов (б)
Основным и универсальным фактором, стимулирующим образование мегакариоцитов и тромбоцитов, является тромбоци- топоэтин (тромбопоэтин). Важную роль в регуляции тромбоци- топоэза играют также цитокины КL (фактор стволовых клеток); интерлейкины-3, -6, -11; гранулоцитарно-макрофагальный коло- ниестимулирующий фактор (GM-CFF). Тромбоцитопоэтин (тромбопоэтин) – специфический цито- кин, регулирующий тромбоцитопоэз, идентифицирован в 1994 г., представляет собой полипептид, состоящий из 353 аминокислот с молекулярной массой 36 килодальтон. Ген, кодирующий синтез тромбопоэтина, располагается на хромоcоме 3q. Тромбопоэтин образуется в печени, однако небольшие количества тромбопоэти- на обнаруживаются в почках, мозге и яичниках. Тромбопоэтин в организме не депонируется, а сразу высвобождается и поступает в кровоток после синтеза.
64.
Рис. 64. Структура тромбоцита, основные компоненты
К мембранам тромбоцитов прилегает аморфный белковый слой (10-50 нм), получивший название «плазматической атмо- сферы» или «гликокаликса», имеющий высокое содержание не- которых белков, в том числе факторов свертывания крови. Из внутренних органелл тромбоцитов наиболее важны: 1. Система микротрубочек, содержащая сходный с актомио- зином сократительный белок.
2. Гранулярный аппарат: a) безбелковые плотные -гранулы высокой плотности, содержащие АТФ, АДФ, серотонин, катехоламины,
кальций, магний; b) белковые -гранулы, содержащие -тромбоглобулин, фибронектин, антигепариновый фактор (4 тромбоци- тарный фактор), тромбоцитарный фактор роста, тром- боспондин, фактор Виллебранда, фибриноген, факторы свертывания V, VIII, XIII. При активации тромбоцитов содержимое гранул выходит из клетки (реакция высвобождения) и играет важную роль в процес- се образования первичной гемостатической пробки (первичный гемостаз).
ции:
В гемостазе тромбоциты осуществляют следующие функ-
ангиотрофическая – обеспечение жизнеспособности
эндотелиальных клеток и поддержание нормальной структуры и функции стенок сосудов микроциркуляторного русла;
коагуляционная – участие в процессе свертывания кро- ви и в регуляции фибринолиза (12 тромбоцитарных факторов (ТФ), среди которых одним из наиболее активных является 3ТФ);
атеросклероза, ишемической болезни сердца, реакции отторже- ния трансплантата, развитии опухолевых метастазов.
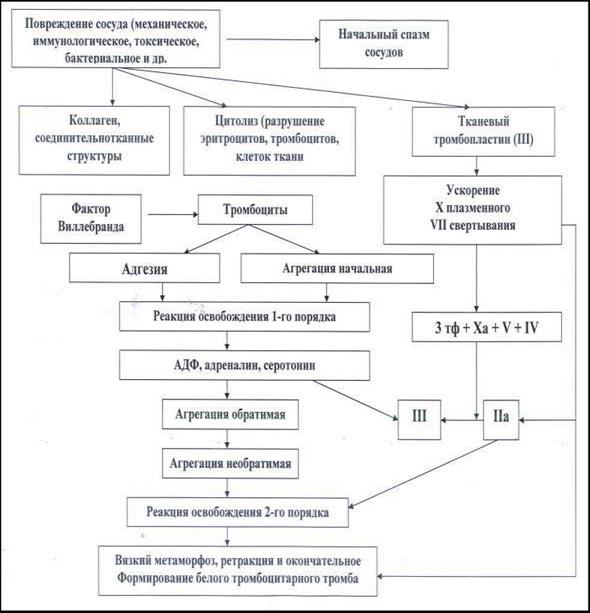
В механизмах тромбообразования выделяют две фазы: 1-я – сосудисто-клеточная (фаза адгезии и агрегации тром- боцитов или образование первичного тромба) (рис.66) и 2-я – плазматическая (фаза коагуляции) (рис. 68). Образование первичного (белого) тромба связано с процес- сами адгезии, агрегации и секреции тромбоцитами биологически активных веществ.
Адгезия тромбоцитов. В нормальных условиях в неповре- жденных сосудах тромбоциты не адгезируют (не прилипают) к эндотелию. В определенной мере это обусловлено продукцией эндотелием 13-гидроксиоктадекадиеновой кислоты (13-ГОДК), простагландина I2 (PgI2), которая угнетает адгезию и агрегацию тромбоцитов, а также продукцию тромбоксана. При повреждении сосуда нарушается целостность эндоте- лия, обнажается субэндотелий и тромбоциты прилипают к нему за несколько секунд. Адгезивная реакция тромбоцитов опосреду- ется взаимодействием их соответствующих гликопротеиновых рецепторов с лигандами (коллагеном, фибронектином, тромбос- пондином, витронектином, ламинином, тканевым фактором, ко- торые становятся доступными для тромбоцитов при повреждении сосуда), а также с фактором фон Виллебранда. Выраженность тромбоцитарных реакций зависит от тяжести и глубины повреждения сосудистой стенки. При небольшой сте- пени повреждения сосуда, когда имеется только десквамация эн- дотелия с обнажением базальной мембраны, тромбоциты прили- пают к базальной мембране, распластываются на ней, но при этом не выделяют веществ, стимулирующих агрегацию. При бо- лее значительном повреждении сосуда (например, при разрыве атеросклеротической бляшки) происходит обнажение более глу- боких сосудистых структур. При этом тромбоциты не только прилипают к поврежденной поверхности, но и выделяют факто- ры, способствующие агрегации тромбоцитов и активации плаз- менных факторов свертывания. Главным кофактором адгезии тромбоцитов к различным ви- дам коллагена и к субэндотелию является фактор фон Виллеб-
Рис. 65. Ориентация гликопротеинов Iвα, Iвβ, IIвα IIвβ и IIIа на мембране тромбоцита
При взаимодействии GPIb/IХ-рецепторов и фактора Вил- лебранда происходит активация GPIIb/IIIa-рецепторов, которые связываются с циркулирующим в крови фибриногеном. Под влиянием GPIIb/IIIa-рецепторов между тромбоцитами формиру- ются фибриновые мостики и происходит локальное скопление тромбоцитов. Этот процесс называется когезией (сohesion) или сцеплением тромбоцитов. GPIIb/IIIa-рецепторы тромбоцитов связываются также с циркулирующими в плазме адгезивными молекулами, включаю- щими фактор Виллебранда, фибронектин, витронектин, тромбос- пондин. В результате указанных процессов – адгезии и когезии – в месте поврежденного эпителиального покрова сосудистой стен- ки на субэндотелии образуется монослой тромбоцитов.
Агрегация тромбоцитов. В результате адгезии происходит активация тромбоцитов и выход содержимого их гранул в плазму (рис. 66). Под влиянием биологически активных веществ тромбо- цитов, а также адреналина, тромбина, коллагена происходит аг- регация тромбоцитов. Агрегации тромбоцитов предшествует изменение их формы, обусловленное изменением микротубулярной системы и сокра- щением микрофиламентов внутри тромбоцитов, в результате чего образуются псевдоподии. Наиболее важную роль в агрегации тромбоцитов играют аденозиндифосфат (АДФ), тромбин и тромбоксан А2. Под влиянием АДФ происходит конформация рецепторов GPIIb/IIIa на поверхности тромбоцитов с последующим связыва- нием фибриногена. Тромбин стимулирует выделение аденозиндифосфата, кото- рый вызывает необратимую агрегацию тромбоцитов, активирует фосфолипазу тромбоцитарных мембран, инициируя, таким обра- зом, синтез тромбоксана А2 и может индуцировать агрегацию тромбоцитов непосредственно. Взаимодействие тромбина с ре- цепторами тромбоцитов активирует внутриклеточную фосфоли- пазу С – фермент, гидролизирующий мембранный фосфолипид фосфотидилинозитол 4,5-бифосфат с образованием двух внут- ренних эфекторных молекул, 1,2-диацилглицерола и 1,4,5- инозитолтрифосфата (IP3). Диацилглицерол активирует протеин- киназу С, которая фосфорилирует протеин pleckstrin. В результа-
Рис. 66. Механизм сосудисто-тромбоцитарного гемостаза
те происходит агрегация и высобождение содержимого гранул. IP3 вызывает высвобождение Ca2+ в цитозоль, который взаимо- действует с кальмодулином и миозином легких цепей киназы, приводя к фосфорилированию легких цепей миозина. Эти цепи взаимодействуют с актином, вызывая изменение формы тромбо- цитов. Коллаген-индуцированная активация фосфолипазы А2 в присутствии Са2+ приводит к высвобождению арахидоновой ки- слоты из мембранных фосфолипидов, образованию тромбоксана А2, который взаимодействует с G-белком с последующей актива- цией фосфолипазы С и активацией агрегации тромбоцитов.
Тромбоксан А2 (ТXA2) является метаболитом арахидоновой кислоты, образуется под влиянием ферментов циклооксигеназы и тромбоксансинтетазы и индуцирует агрегацию тромбоцитов как непосредственно, так и в качестве синергиста аденозиндифосфа- та, тромбина и коллагена (рис. 67). Аспирин в дозе 30 мг/сут блокирует циклооксигеназу-1 и образование тромбоксана А2 в тромбоцитах, оказывая антиагре- гационный эффект. Также он блокирует на несколько часов обра- зование простациклина в эндотелиальных клетках.
Рис. 67. Схематическое изображение образования в цитоплазме арахидоновой кислоты и ее липоксигеназный и циклооксигеназный метаболизм
• ФЛА2- фосфолипаза А2 • АА – арахидоновая кислота • НРЕТЕ – гидроксиэйкозатетраеновая кислота • 5-LO – липоксигеназа • СОХ – циклооксигеназа • PGE2 – простогландин Е2 • PGF2α – простогландин F2α • PGI2 – простациклин • ΤΧΑ2 – тромбоксан А2
Наряду с агрегационным эффектом тромбоксан А2 оказыва- ет выраженный сосудосуживающий эффект, что также способст- вует гемостазу. В эндотелиоцитах из арахидоновой кислоты под влиянием
ферментов циклооксигеназы и простациклинсинтетазы образует- ся простациклин РgI2, который ингибирует агрегацию тромбоци- тов и оказывает сосудорасширяющий эффект. Соотношение ТXА2, продуцируемого тромбоцитами, и простациклина, синте- зируемого эндотелиоцитами, определяет гемостатическую реак- цию в месте повреждения сосуда. Наряду с циклооксигеназным путем метаболизма арахидо- новой кислоты существует второй путь – липооксигеназный. С помощью фермента липоксигеназы, расположенного в цитозоле тромбоцитов, арахидоновая кислота превращается в 12- гидроксиэйкозотетраеновую кислоту (12-ГЭТК или НРЕТЕ), ко- торая стимулирует адгезию тромбоцитов. Если продукция тром- боксана подавлена, тромбоциты сохраняют способность синтези- ровать 12-ГЭТК и способность к адгезии. И наоборот, когда про- дукция 12-ГЭТК ингибирована и адгезия тромбоцитов нарушена, они могут синтезировать тромбоксан А2 и сохранять способность к агрегации. Для нормального осуществления агрегации тромбоцитов необходимы также ионы Са++ и Мg++. Таким образом, эндотелий сосудов и тромбоциты осуществ- ляют так называемый первичный, или сосудисто- тромбоцитарный гемостаз. Он реализуется в течение нескольких минут. В месте повреждения сосуда развиваются вазоспазм, адге- зия тромбоцитов, высвобождение из их гранул активных веществ и в конечном итоге – агрегация тромбоцитов и формирование тромбоцитарных тромбов. Фаза высвобождения, во время которой происходит секре- ция содержимого сначала α-гранул, а затем плотных гранул, уси- ливает агрегацию, делая ее необратимой. Увеличивающаяся кон- центрация АДФ, тромбина, серотонина и других тромбоцитарных агрегантов вовлекает новые тромбоциты в образование первич- ного тромба. Из поврежденных лейкоцитов и эндотелия выделяется фос- фолипид, названный тромбоцит-активирующим фактором (ТАФ или PAF), который вызывает дальнейшую агрегацию тромбоци- тов и высвобождение из них PF-4 (4 тромбоцитарного фактора) и тромбоксана B2 (TXB2). Необратимые изменения агрегации тромбоцитов наступают через 2-3 мин с момента повреждения сосудов (появление мно-
жественных псевдоподий, потеря тромбоцитарных гранул, обра- зование на поверхности фибриновых волокон) – фаза «вязкого метаморфоза». Образующийся белый тромб не является прочным и спосо- бен обеспечивать гемостаз в мелких сосудах с низким давлением. С момента распада тромбоцитов и выхода тромбоцитарных факторов свертывания крови в окружающую среду начинается следующий этап тромбоза – плазматическая фаза (фаза коагуля- ции крови).
Тромбоцитарные факторы свертывания крови и фибринолиза
Тромбоцитарные факторы свертывания принято делить на эндогенные (о бразующиеся в самих тромбоцитах) и экзогенные (факторы плазмы, адсорбированные на поверхности тромбоци- тов). Эндогенные факторы тромбоцитов принято обозначать арабскими цифрами, в отличие от плазменных факторов, которые обозначаются римскими цифрами. Наиболее изучены 12 эндо- генных тромбоцитарных факторов. Фактор 1 тромбоцитов (ТФ-1) участвует в образовании протромбиназы и ускоряет образование тромбина из протромби- на, подобно фактору V плазмы. Находится в неактивном состоя- нии. Для его перевода в активное состояние необходимы следы тромбина. Фактор 2 тромбоцитов – акцелератор тромбина, фибри- нопластический фактор – ускоряет превращение фибриногена в фибрин. Фактор 3 тромбоцитов – тромбоцитарный тромбопла- стин, мембранный фосфолипидный фактор – представляет со- бой липопротеид. Служит матрицей для взаимодействия плаз- менных факторов гемокоагуляции, образования их активных комплексов. По своим свойствам этот фактор идентичен кефали- ну и мембранному фактору эритроцитов – эритроцитину, эрит- рофосфатиду. Необходим для эндогенного образования протром- биназы, способствующей превращению протромбина в тромбин. Фактор 3 выделяется при агрегации тромбоцитов.
Фактор 4 тромбоцитов (ТФ-4) – антигепариновый – об- ладает выраженной антигепариновой активностью. Освобожде- нию фактора 4 из тромбоцитов способствует тромбин, а отчасти – и фактор Хагемана. Снижение количества тромбоцитов повыша- ет чувствительность крови к гепарину.
Фактор 5 тромбоцитов – свертываемый – по своим свой- ствам сходен с фибриногеном плазмы. Интенсивно выделяется из тромбоцитов под влиянием тромбина. Фактор 5 тромбоцитов принимает участие в агрегации тромбоцитов и тем самым спо- собствует созданию прочного тромба. Фактор 6 тромбоцитов – антифибринолитический. За- держивает фибринолиз. Фактор 7 тромбоцитов – антитромбопластический. Пре- пятствует образованию активной протромбиназы, а также замед- ляет перевод протромбина в тромбин. В присутствии гепарина его антикоагулянтное действие усиливается. Фактор 8 тромбоцитов – ретрактозим. Представляет со- бой сократительный белок тромбоцитов – тромбостенин, напо- минающий актомиозин мышечных волокон. При сокращении тромбостенина происходит ретракция кровяного сгустка. При этом тромбоциты подтягиваются друг к другу, что в свою оче- редь приводит к сближению нитей фибрина. Сгусток обезвожи- вается, становится более компактным. Фактор 9 тромбоцитов – серотонин, или сосудосуживаю- щий фактор. Тромбоциты обогащаются серотонином при прохо- ждении через сосуды желудочно-кишечного тракта и печени. Се- ротонин выделяется из тромбоцитов во время их агрегации, вы- званной АДФ, адреналином, коллагеном. Серотонин обладает многими свойствами: усиливает сокращение сосудов и ретрак- цию кровяного сгустка, изменяет артериальное давление, являет- ся антагонистом гепарина; при тромбоцитопении способен нор- мализовать ретракцию кровяного сгустка и в присутствии тром- бина ускорять переход фибриногена в фибрин. Фактор 10 тромбоцитов – пластиночный кофактор, кот- ромбопластин, или активатор тромбопластина. Его аналог со- держится в змеином яде. Котромбопластин способен ускорять переход протромбина в тромбин не только в сочетании со змеи- ным ядом, но также в присутствии тромбопластина легочной
ткани, фактора V плазмы и Ca2+. Роль котромбопластина в про- цессе свертывания крови в условиях нормы не ясна. Фактор 11 тромбоцитов – фибринстабилизирующий фактор – вещество, аналогичное фактору XIII плазмы. Участвует в стабилизации фибрина (превращении растворимого фибрина в нерастворимый). Фактор 12 тромбоцитов – АДФ (аденозиндифосфат) – фактор агрегации тромбоцитов. При выходе на поверхность тромбоцитов АДФ способствует их склеиванию между собой. Кроме того, АДФ усиливает адгезию тромбоцитов к поврежден- ной стенке сосуда.
Также в белковых гранулах тромбоцитов содержатся:
ный антифибринолитический потенциал;
боцитов;
|
||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-08-15; просмотров: 691; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.11 (0.015 с.) |


 и факторы фибринолиза).
и факторы фибринолиза). обеспечивает свободный ток крови по кровеносным сосудам (рис.
обеспечивает свободный ток крови по кровеносным сосудам (рис.

 61).
61).





















 Кровь
Кровь

 Эндотелий
Эндотелий
 Субэндотелий тканевая
Субэндотелий тканевая отрицательно заряженных гликозаминогликанов в соста- ве гликокаликса;
отрицательно заряженных гликозаминогликанов в соста- ве гликокаликса;

 Роль тромбоцитов в гемостазе
Роль тромбоцитов в гемостазе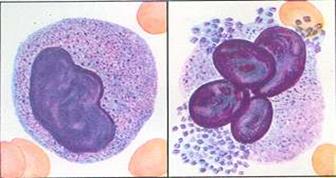
 Тромбоцит окружен двухслойной фосфолипидной мембра- ной, в которую встроены рецепторные гликопротеины, взаимо- действующие со стимуляторами адгезии (фактором Виллебранда и коллагеном) и агрегации этих клеток (АДФ, адреналином), рис.
Тромбоцит окружен двухслойной фосфолипидной мембра- ной, в которую встроены рецепторные гликопротеины, взаимо- действующие со стимуляторами адгезии (фактором Виллебранда и коллагеном) и агрегации этих клеток (АДФ, адреналином), рис.
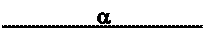
 ранда – мультимерный гликопротеин, входящий в состав ком- плекса антигемофильного фактора VIII плазмы. Фактор фон Вил- лебранда является связующим звеном между специфическими гликопротеиновыми тромбоцитарными рецепторами GPIа/IIa, GPIb/IХ-V b GPVI и тканями субэндотелия (рис.65).
ранда – мультимерный гликопротеин, входящий в состав ком- плекса антигемофильного фактора VIII плазмы. Фактор фон Вил- лебранда является связующим звеном между специфическими гликопротеиновыми тромбоцитарными рецепторами GPIа/IIa, GPIb/IХ-V b GPVI и тканями субэндотелия (рис.65).