
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Основы прогнозирования обстановки на объекте экономики при аварии со взрывом газо-, паровоздушных смесей (ГПВС) и взрывчатых веществСодержание книги
Поиск на нашем сайте
Определение максимального давления при дефлаграционном Горении ГПВС Как уже отмечалось в п.1.4., процесс окисления хорошо перемешанных ГПВС с воздухом, т.е. кинетическая реакция горения, представляет собой процесс послойного горения, при котором образуются продукты сгорания, расширяющиеся равномерно во все стороны со скоростью нормального горения. При горении в замкнутых объемах в зоне послойного горения образуется большое количество продуктов сгорания, которые, расширяясь в объеме помещения, приводят к плавному повышению давления. Поэтому, когда говорят о максимальном давлении при дефлаграционном горении ГВС, то учитывают условия, при которых данный процесс обладает максимальными термодинамическими параметрами. Для этого принимают следующие допущения: процесс происходит в абсолютно герметичном помещении; во всем объеме помещения горючий газ и воздух полностью перемешаны с образованием смеси стехиометрического состава; точечный источник инициирования расположен в центре помещения и его энергия достаточна для активации; потери теплоты отсутствуют. В адиабатическом процессе, т.е. термодинамическом процессе без потерь теплоты, но с выделением теплоты сгорания и возможным изменением количества молей газа в процессе реакции горения, изменение конечного давления (оно же и максимальное давление горения ГВС) будет пропорционально изменению температуры и количества молей газа, то есть:
где р1 – конечное давление процесса сгорания ГВС, кПа; р0 – давление в помещении до взрыва (принимается равным атмосферному давлению, 101,3 кПа); Т1 и Т0 – соответственно конечная и начальная температуры процесса, К; n0 и n1 – соответственно начальное количество кМолей газа и конечное для продуктов сгорания (значения определяются из уравнения химической реакции). Выразим из формулы (2.31) конечное давление процесса, которое будет соответствовать максимальному:
Формулой 2.32 можно пользоваться, когда экспериментально известны значения температур. Определение конечной температуры для каждого расчетного случая не представляется возможным, поэтому выразим ее через теплоту реакции, т.к. при адиабатном расширении температура продуктов сгорания зависит от удельной теплоты сгорания газа и средней теплоемкости продуктов сгорания и определяется отношением:
где Q – теплота реакции, выделившаяся при сгорании всей массы газа, кДж; сi – удельная теплоемкость i – го газа в продуктах сгорания; m – количество газов в продуктах сгорания; Мi – масса i-го газа в объеме помещения. Зная плотность газа ρ2 и его объем Vг, можно определить массу i-го газа по формуле 2.32 с учетом стехиометрического состава, в замкнутом объеме помещения-Vп. При этом, если процесс горения горючего газа происходит в воздухе, то необходимо учитывать нетеоретическую плотность чистого газа (2.34):
где М –молярная масса газа, кг/кмоль; Vm – молярный объем газа, м3/кмоль (из закона Авогадро); ρсм – плотность горючей смеси, определяемая из соотношения
где
Для смеси стехиометрического состава плотность горючего газа определяется зависимостью:
где Ссх – стехиометрическая концентрация горючего газа в газовоздушной смеси стехиометрического состава. Тогда массу газа в смеси с воздухом стехиометрического состава – МГ можно определить по формуле:
Теплоту реакции, выделившейся при сгорании смеси с массой газа – МГ в формуле (2.33) можно определить через удельную теплоту сгорания горючего газа –
С учетом зависимостей (2.36) и (2.37) формула (2.38) примет вид:
Поставим выраженное значение теплоты реакции в формулу (2.33), тогда:
Так как содержание воздуха в ГПВС превышает содержание горючего газа, например для пропана составляет 1,32 % объема, а воздуха 98,68 %, т.е. почти в 75 раз больше, то для практических расчетов можно пренебречь различием в теплофизических свойствах горючего газа и считать в качестве рабочего тела не горючий газ, а воздух. В соответствии с принятым допущением не произойдет изменение молекулярного состава смеси до и после реакции, т.е. n1= n0, и в формуле (2.32) продуктом реакции будет только воздух. Тогда можно записать упрощенную формулу определения увеличения температуры при реакции горения газов:
где Св – удельная теплоемкость воздуха, кДж/(кг К);
Из формулы (2.41) выразим конечную температуру процесса:
Перепишем уравнение (2.42) с учетом выраженного значения конечной температуры процесса (2.32) и допущения равенства n1=n0. Максимальное давление дефлаграционного горения ГПВС в герметичном объеме, с учетом принятого допущения, равно:
Преобразуем его в виде:
где рmax – максимальное давление при дефлаграционном взрыве ГПВС, кПа; р0 – атмосферное давление, 101,3 кПа;
Таким образом, полученная зависимость позволяет определить максимальное давление при горении ГПВС в замкнутом объеме. Для более точного определения необходимо уточнять теплоемкость воздуха в продуктах реакции. Как правило, максимальный интервал температуры реакции горения ГПВС находится в границах 2300-2800 К. Формула (2.44) позволяет определить давление при дефлаграционном горении ГПВС с концентрациями стехиометрического состава и смесей, у которых соотношение горючего газа и воздуха находится между стехиометрическим и составом, соответствующим нижнему концентрационному распространению пламени (НКПР). Особенность процессов горения ГПВС при избытке горючих газов в смеси, т.е. при концентрациях между стехиометрической и соответствующей верхнему концентрационному пределу распространения пламени, заключается в том, что количество непрореагировавшего газа увеличивается и при этом происходит существенное снижение температурного процесса, что не позволяет использовать данную формулу без уточнения теплоемкости воздуха и массы участия газа.
Пример 1. Помещение кубической формы V=4´4´4м2 заполнено в объеме пропано-воздушной смесью стехиометрического состава при нормальных условиях. Определить максимальное избыточное давление при дефлаграционном горении ГВС и избыточное давление при концентрации, соответствующей смеси с НКПР пламени.
QHр – низшая теплота реакции, кДж/кг, по данным табл. 4 приложения 3. rг – плотность газа, кг/м3 :
где М – молярная масса пропана; Vm – молярный объем, занимаемый газом.
Ссх – стехиометрическая концентрация, % об.
где n – количество молей вещества в смеси из уравнения реакции горения
1С3H8+5O2+5×3,76 ×N2=3CO2+4H2O+5×3,76N2+Q
СВ – удельная теплоемкость воздуха, кДж/(кг×к), по условию изохорного процесса (объем помещения постоянный, можно принять по табл. 3 приложения 3, где
Подставим найденные данные в формулу:
Определим давление при дефлаграционном горении пропано-воздушной смеси при концентрации соответствующей НКПР пламени. Плотность смеси будет равна:
Тогда:
Ответ: в результате дефлаграционного процесса горения пропано-воздушной смеси стехиометрического состава в замкнутом объеме помещения максимальное давление равно 825 кПа, а смеси, соответствующей НКПР–510 кПа.
|
|||||||||||
|
Последнее изменение этой страницы: 2016-08-10; просмотров: 537; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.64.210 (0.011 с.) |

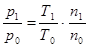 , (2.31)
, (2.31) . (2.32)
. (2.32) , (2.33)
, (2.33) , (2.34)
, (2.34) (2.35)
(2.35) – плотность чистого газа, при нормальных условиях кг/м3;
– плотность чистого газа, при нормальных условиях кг/м3; – объем газа в смеси соответствующего состава, в данном случае принимается для стехиометрического, % объема;
– объем газа в смеси соответствующего состава, в данном случае принимается для стехиометрического, % объема;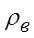 – плотность воздуха при нормальных условиях;
– плотность воздуха при нормальных условиях; – объем воздуха в смеси соответствующего состава, принимается для стехиометрического.
– объем воздуха в смеси соответствующего состава, принимается для стехиометрического. , (2.36)
, (2.36)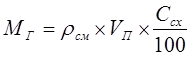 . (2.37)
. (2.37)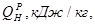 определяем по справочным данным из табл. 5 приложения 3:
определяем по справочным данным из табл. 5 приложения 3: . (2.38)
. (2.38)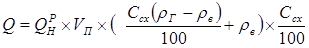 . (2.39)
. (2.39)
 . (2.40)
. (2.40) , (2.41)
, (2.41) – плотность воздуха до реакции (при нормальных атмосферных условиях
– плотность воздуха до реакции (при нормальных атмосферных условиях 
 . (2.42)
. (2.42)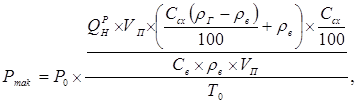 (2.43)
(2.43) , (2.44)
, (2.44) – удельная теплота сгорания горючего газа, кДж/кг;
– удельная теплота сгорания горючего газа, кДж/кг; – стехиометрическая концентрация газа в смеси с воздухом, % об.;
– стехиометрическая концентрация газа в смеси с воздухом, % об.; – начальная температура процесса, К;
– начальная температура процесса, К; – теплоемкость воздуха при отсутствии данных, рекомендуется принимать 1,01 кДж/(кг К) либо по табл. 3 приложения 3.
– теплоемкость воздуха при отсутствии данных, рекомендуется принимать 1,01 кДж/(кг К) либо по табл. 3 приложения 3.
 , кПа
, кПа
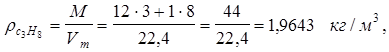
 ,
,

 .
. соответствует 2800 К), тогда
соответствует 2800 К), тогда

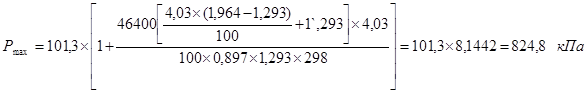 .
. .
.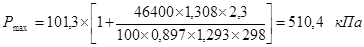 .
.


