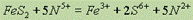Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Окислительно-восстановительные реакции и электрохимические процессы. Процессы окисления и восстановления.Содержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте Цель: научиться решать окислительно-восстановительные реакции, составлять окислительно-восстановительный баланс. План 1. Окислительно-восстановительные реакции в растворахПроцессы окисления и восстановления 2. Определение стехиометрических коэффициентов в уравнениях окислительно-восстановительных реакций.. 3. Стандартные потенциалы окислительно-восстановительных реакций.Электрохимические процессы. Окислительно-восстановительные реакции в растворах. Химические реакции, протекающие с изменением степени окисления элементов, входящих в состав реагирующих веществ, называются окислительно-восстановительными. Окисление — это процесс отдачи электронов атомом, молекулой или ионом. Если атом отдает свои электроны, то он приобретает положительный заряд:
Если отрицательно заряженный ион (заряд -1), например Сl-, отдает 1 электрон, то он становится нейтральным атомом:
Если положительно заряженный ион или атом отдает электроны, то величина его положительного заряда увеличивается соответственно числу отданных электронов:
Восстановление — это процесс присоединения электронов атомом, молекулой или ионом. Если атом присоединяет электроны, то он превращается в отрицательно заряженный ион:
Если положительно заряженный ион принимает электроны, то величина его заряда уменьшается:
или он может перейти в нейтральный атом:
Окислителем является атом, молекула или ион, принимающий электроны. Восстановителем является атом, молекула или ион, отдающий электроны. Окислитель в процессе реакции восстанавливается, восстановитель — окисляется. Следует помнить, что рассмотрение окисления (восстановления) как процесса отдачи (и принятия) электронов атомами или ионами не всегда отражает истинное положение, так как во многих случаях происходит не полный перенос электронов, а только смещение электронного облака от одного атома к другому. Однако для составления уравнений окислительно-восстановительных реакций не имеет существенного значения, какая связь при этом образуется — ионная или ковалентная. Поэтому для простоты будем говорить о присоединении или отдаче электронов независимо от типа связи. 1. Определение стехиометрических коэффициентов в уравнениях окислительно-восстановительных реакций. При составлении уравнения окислительно-восстановительной реакции необходимо определить восстановитель, окислитель и число отдаваемых и принимаемых электронов. Как правило, коэффициенты подбирают, используя либо метод электронного баланса, либо метод электронно-ионного баланса (иногда последний называют методом полуреакций). В качестве примера составления уравнений окислительно-восстановительных реакций рассмотрим процесс окисления пирита концентрированной азотной кислотой. Прежде всего определим продукты реакции. HNO3 является сильным окислителем, поэтому сера будет окисляться до максимальной степени окисления S6+, а железо — до Fe3+,при этом HNO3 может восстанавливаться доN0или NO2. Мы выберем NO:
Где будет находиться H2O (в левой или правой части), мы пока не знаем. 1. Применим сначала метод электронно-ионного баланса (полуреакций). В этом методе рассматривают переход электронов от одних атомов или ионов к другим с учетом характера среды (кислая, щелочная или нейтральная), в которой протекает реакция. При составлении уравнений процессов окисления и восстановления для уравнивания числа атомов водорода и кислорода вводят (в зависимости от среды) или молекулы воды и ионы водорода (если среда кислая), или молекулы воды и гидроксид-ионы (если среда щелочная). Соответственно и в получаемых продуктах в правой части электронно-ионного уравнения будут находиться ионы водорода и молекулы воды (кислая среда) или гидроксид-ионы и молекулы воды (щелочная среда). Т. е. при написании электронно-ионных уравнений нужно исходить из состава ионов, действительно имеющихся в растворе. Кроме того, как и при составлении сокращенных ионных уравнений, вещества малодиссоциирующие, плохо растворимые или выделяющиеся в виде газа следует писать в молекулярной форме. Рассмотрим для нашего случая полуреакцию окисления. Молекула FeS2 превращается в ион Fe3+ (Fе(NО3)3 полностью диссоциирует на ионы, гидролизом пренебрегаем) и два иона SO42- (диссоциация H2SO4): Для того чтобы уравнять кислород, в левую часть добавим 8 молекул Н2О, а в правую — 16 ионов Н+ (среда кислая):
Заряд левой части равен 0, заряд правой +15, поэтому FeS2 должен отдать 15 электронов:
Рассмотрим теперь полуреакцию восстановления нитрат-иона:
Необходимо отнять у NО3 2 атома О. Для этого к левой части добавим 4 иона Н1+ (кислая среда), а к правой — 2 молекулы Н2О:
Для уравнивания заряда к левой части (заряд+3) добавим 3 электрона:
Окончательно имеем:
Сократив обе части на 16Н+ и 8Н2О, получим сокращенное ионное уравнение окислительно-восстановительной реакции:
Добавив в обе части уравнения соответствующее количество ионов NO3- и Н+ находим молекулярное уравнение реакции:
Обратите внимание, что для определения количества отданных и принятых электронов вам ни разу не пришлось определять степень окисления элементов. Кроме того, мы учли влияние среды и автоматически определили, что Н2О находится в правой части уравнения. Несомненно то, что этот метод гораздо больше соответствует химическому смыслу, чем стандартный метод электронного баланса, хотя последний несколько проще для понимания. 2. Уравняем данную реакцию методом электронного баланса. Процесс восстановления описывается:
Сложнее составить схему окисления, поскольку окисляются сразу два элемента — Fe и S. Можно приписать железу степень окисления 2+, сере 1- и учесть, что на один атом Fe приходится два атома S:
Можно, однако, обойтись без определения степеней окисления и записать схему, напоминающую схему
Правая часть имеет заряд +15, левая — 0, поэтому FeS2 должен отдать 15 электронов. Записываем общий баланс:
пять молекул НNО3 идут на окисление FeS2, и еще три молекулы HNO3 необходимы для образования Fe(NО3)3:
Чтобы уравнять водород и кислород, добавляем в правую часть две молекулы Н2О:
Метод электронно-ионного баланса более универсален по сравнению с методом электронного баланса и имеет неоспоримое преимущество при подборе коэффициентоввомногих окислительно-восстановительных реакциях, в частности, с участием органических соединений, в которых даже процедура определения степеней окисления является очень сложной. Рассмотрим, например, процесс окисления этилена, происходящий при пропускании его через водный раствор перманганата калия. В результате этилен окисляется до этиленгликоля НО—CH2—СН2—ОН, а перманганат восстанавливается до оксида марганца (IV), кроме того, как будет очевидно из итогового уравнения баланса, справа образуется также гидроксид калия:
После проведения необходимых сокращений подобных членов записываем уравнение в окончательном молекулярном виде
Стандартные потенциалы окислительно-восстановительных реакций. Возможность протекания любой окислительно-восстановительной реакции в реальных условиях обусловлена рядом причин: температурой, природой окислителя и восстановителя, кислотностью среды, концентрацией веществ, участвующих в реакции, и т. д. Учесть все эти факторы бывает трудно, но, помня о том, что любая окислительно-восстановительная реакция протекает с переносом электронов от восстановителя к окислителю, можно установить критерий возможности протекания такой реакции. Количественной характеристикой окислительно-восстановительных процессов являются нормальные окислительно-восстановительные потенциалы окислителей и восстановителей (или стандартные потенциалы электродов). Чтобы понять физико-химический смысл таких потенциалов, необходимо проанализировать так называемые электрохимические процессы.
|
||
|
Последнее изменение этой страницы: 2016-12-10; просмотров: 638; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.137.166.244 (0.012 с.) |