

Мы поможем в написании ваших работ!
ЗНАЕТЕ ЛИ ВЫ?
|
Основные звенья патогенеза ГБ
Похожие статьи вашей тематики
Антигипертензивные средства
| Определение фармакологической группы
| Область применения
| | Лекарственные средства, снижающие САД при его патологическом повышении.
| Терапия
Неврология
Для лечения артериальной гипертензии (АГ - гипертонической болезни, симптоматической гипертонии) и купирования гипертонического криза, при спазмах периферических сосудов.
| | В основе развития АГ лежит нарушение регуляции САД сосудодвигательным центром в результате действия раздражителей: эмоциональных стрессов, нервно-психического перенапряжения, генетически обусловленной предрасположенности.
Ведущие факторы в генезе АГ: ↑ МОС, ↑ ОПС, ↑ ОЦК.
|
РАЗДРАЖИТЕЛИ
↓
↑ симпатические центры ствола ГМ
↑ САС (СНС, надпочечники: ↑ адреналина, NA в крови)
КА
↓
↓ ↓ ↓ ↓
β1-АР α1-АР β1,2-АР ЮГА α1,2-АР
сердца вен почек артерий
↓ ↓ ↓ ↓
↑ ЧСС, ↑ тонус вен ↑ ренин ↑ тонус артерий
↓ ↓ ↓ ↓
↑МОС ↑ преднагрузка ↑ АТ-ΙΙ ↑ ОПС
↑ ↓
↑ОЦК ↓ ↓ ↓
↑ альдостерон ↑ АДГ ↑ выброс КА
↓ ↓ ↓
↑ реабсорбция Na+, Н2О ↓ синтез Pg, NO
Основные звенья патогенеза ГБ
| ↑ ОПС
| ↑ ОЦК
| ↑ МОС
| | Активация САС (КА)
Увеличение собственного базального тонуса сосудов (не связанное с КА)
| Активация РААС
(ренин-альдостерон → реабсорбция Na+ и Н2О)
| Активация САС (КА)
Гипертрофия сердца (увеличение массы миокардиоцитов)
| На уровень САД влияют: РС, ОПС, эластичность стенок сосудов, ОЦК, вязкость крови, электролитный
состав крови, тонус скелетных мышц, активность адрен-, дофамин-, холин- и
пуринергических нервов.
Факторы риска ГБ: неблагоприятное течение ГБ при отягощенном семейном анамнезе,
гиперхолестеринемии, избыточной массе тела, гиперинсулинемии (снижении
толерантности к глюкозе), гиперурикемии, поражении сосудов почек, мозга,
сердца, курении, лиц мужского пола.
Классификация артериальной гипертонии (США) у людей от 18 лет и старше (без лечения)
| Давление
| Систолическое (мм рт ст)
| Диастолическое (мм рт ст)
| | Оптимальное
Нормальное
Повышенное нормальное
Артериальная гипертония:
1 стадия (Мягкая)
2 стадия (Умеренная)
3 стадия (Выраженная)
4 стадия (Тяжелая)
| ≤ 120
120 – 129
130 – 139
140 – 159
160 – 179
180 – 209
≥ 210
| ≤ 80
80 - 84
85 – 89
90 – 99
100 – 109
110 – 119
≥ 120
|
Принципы патогенетического лечения ГБ
| ↓ ОПС.
(↓ Постнагрузки -расширение артериол,
↓ Преднагрузки - расширение венул).
| ↓ МОС (↓ СНС).
| Учитывать механиз-мы саморегуляции: если АД ↑, значит в каком то регионе оно ↓ до нормы. Если ↓ САД, в кровь поте-
кут ренин и др.
| ↓ ОЦК.
Ограничить потреб-ление соли до 5-6 г/сут (в норме потре-бность в NaCl = 10 - 15г/сут).
| Индивидуальный подбор доз.
Постепенно отменять препарат (профилак-тика синдрома отме-ны). Учитывать воз-можные осложнения.
|
Виды сосудистого тонуса
| Нейрогенный
| Гуморальный
| Миоге нный (базальный)
|
Напарвленность действия антигипертензивных средств
| І Нейротропные
| І І Гуморальные
| І І І Миотропные
|
Основные точки приложения действия антигипертензивных средств
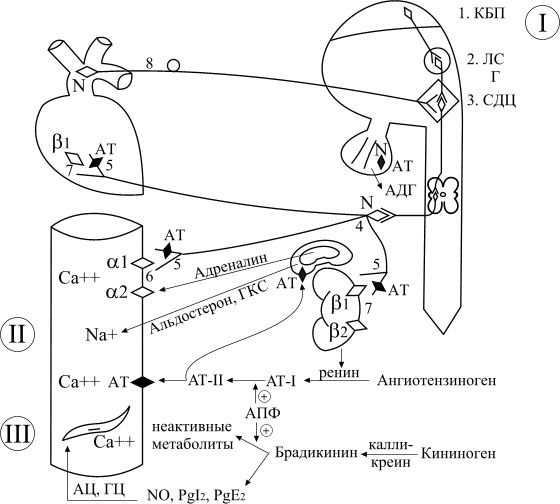
Обозначения: I – нейротропные Л.С.
II – гуморальные Л.С.
III – миотропные Л.С.
КБП – кора больших полушарий
ЛС – лимбическая система
Г – гипоталамус
СДЦ – сосудодвигательный центр
АДГ – антидиуретический гормон (вазопрессин)
АПФ – ангиотензинпревращающий фермент
АТ-Ι – ангиотензин-Ι; АТ-ΙΙ – ангиотензин-ΙΙ
АТ – ангиотензиновый рецептор
АЦ – аденилатциклаза
ГЦ - гуанилатциклаза
Краткая характеристика антигипертензивных средств
| 1. Нейротропные антигипертензивные средства центрального действия
| | Препараты
| Особенности действия и применения
| Побочные эффекты
| | 1.1. Вещества седативного
действия:
А) Седативные (препараты валерианы, пустырника, брома, барбитураты в седа-тивных дозах);
Б) Анксиолитики (сибазон, оксилидин, мезапам, триоксазин);
В) Нейролептики (аминазин, резерпин).
| Успокаивают высшие центры эмоцио-нальной активности: ЛС, КГМ → ↓ акти-вация медуллярных центров → ↓ прес-сорной зоны гипоталамуса, ↓ сосудосу-живающих импульсов. Устраняют отрицательные эмоции, стрессорные факторы при лабильной гипертонии. Не обладают гипотензивным действием. Применение: больным с лабильной психикой в начальных стадиях АГ.
Нейролептики – обладают антиадренер-гическим гипотензивным действием. Аминазин– при гипертоническом кризе.
|
Явления бромизма, заторможен-ности, сонливости.
Депрессия.
| | 1.2. Вещества, угнетающие СДЦ:
- Клонидин (клофелин),
- Гуанфацин (эстулик),
- Моксонидин (цинт),
- Рилменидин,
- Метилдофа (альдомет).
| ↑α2 и Ι! Рецепторы.
↓ высвобождение КА – медиаторов прессорной зоны.
↓ ОПС, ↓ МОС, ↓ ОЦК.
↑ образование брадикинина, Pg.
↓ РФ - центральное седативное действие.
Применение: при АГ (вместе с салурети-ками), при гипертоническом кризе.
| ↑ САД (на несколько мин.) при в/в-струйном введении (↑α2 внеси-наптические рецепторы).
↑ задержка Na+ и Н2О в организме.
Ортостатические реакции.
Потенцирующее действие (сонли-вость, вялость, замедление реак-ции). Привыкание, синдром отме-ны. ↑ аппетита (↓ центр насыще-ния). Сухость во рту, запоры
(↓ высвобождения АН). Паркинсонизм, гиперпролактин-емия (↓ DA).
|
Гипертензивные средства
| Определение фармакологической группы
| Область применения
| | Лекарственные средства, применяемые при острой и хронической сосудистой недостаточности (гипотензии), острой сердечной недостаточности
(↓ МОС при ИМ, дистрофии миокарда, отравлении химическими веществами, микробными токсинами и др.), при шоках.
| Терапия
Кардиология
Неврология
Токсикология
Для лечения острой и хронической гипотензии.
|
Средства терапии хронической гипотензии
| Симпатомиметики
| Аналептики
| Общетонизирующие
| Минералокортикоиды
| | Эфедрин
| Кордиамин, стрихнин
| Лимонник, Жень-шень
| ДОКСА
|
Антиангинальные средства
| Определение фармакологической группы
| Область применения
| | - Средства терапии недостаточности коронарного кровообращения (ИБС*), купирования и профилактики приступов стенокардии.
| Кардиология
Терапия
| | * ИБС – патологическое состояние, связанное с коронарной недостаточностью.
Проявления: стенокардия (angina pectoris – грудная жаба, лат.);
инфаркт миокарда (ранняя стадия – до 30мин., поздняя стадия – до 24час.).
|
Патогенез ИБС
| Несоответствие между потребностью сердца в кислороде и уровнем доставки кислорода сердцу.
| | Потребность в кислороде
| Доставка кислорода
| | Диастолическое давление (преднагрузка)
Систолическое давление (постнагрузка)
Напряжение стенки миокарда
Объем желудочков сердца
Размер (радиус) сердца
Желудочковое давление
Сократимость
ЧСС
| % экстракции О2 из крови
Коронарный кровоток (объемная скорость КК)
Коллатеральное коронарное кровообращение (ККК)
Эндокардиально-эпикардиальный кровоток
Диаметр крупных коронарных артерий
Сопротивление коронарных артерий
Диастолическое давление в аорте
Метаболическая ауторегуляция КК
| | Патогенетические механизмы
| Основные причины
| | Нарушение кровоснабжения и метаболизма миокар-да. Увеличение потребности миокарда в кислороде (Qо2) в большей степени, чем доставки кислорода с коронарной кровью. Qо2 определяется преднагруз-кой (венозным наполнением и растяжением камер сердца, увеличением сократимости миокарда по закону Франка-Старлинга); постнагрузкой (ОПС артерий); ЧСС (время диастолы).
| Атеросклероз коронарных артерий,
Спазм коронарных артерий,
Тромбоз и эмболия коронарных артерий,
Снижение перфузионного давления в коронарных артериях,
Увеличение КДДЛЖ,
Артериальная гипертензия,
Отек легких,
Анемия, курение, тахикардия, неадекватные физические нагрузки.
|
Принципы терапии ИБС
| ↓ Потребности миокарда в О2
| ↑ Доставки О2 к пораженному миокарду
| | ↓ РС
| ↓ Нагрузки на миокард
| ↑ Оксигенации миокарда
| | ↓ адренергической иннервации,
↓ поступления Са++ в миокард,
↓ метаболизма сердца.
| ↓ САД,
↓ преднагрузки,
↓ постнагрузки,
↓ УО,
↓ размеров сердца.
| ↑ ККК,
↓ Экстраваскулярной компрессии коронарных артерий (↓ диастолического напряжения стенки левого желудочка),
↓ Тонуса коронарных сосудов,
↓ Коронаросуживающих рефлексов,
Тромболизис коронарных артерий,
↑ Содержания аденозина в миокарде.
| | При стабильной и нестабильной стенокардии, при стенокардии напряжения и покоя – предупреждение развития ОИМ (коронарной смерти).
| | Купирование приступов стенокардии
| Профилактика приступов стенокардии
|
Фармакокинетика нитратов
Разная, в зависимости от используемого препарата и лекарственной формы (таб., мази, ТТС, пленки, аэрозоли, растворы).
Фармакодинамика нитратов
| ↓ Потребности в кислороде миокарда
| ↑ Доставки кислорода к миокарду
| | Расширение вен
(в основном)
большого круга кровообращения →
↓ ВД (преднагрузка) →
↓ РС → ↓ Qо2
| Расширение артерий большого круга кровообращения →
↓ АД (постнагрузка) →
↓ РС →
↓ Qо2
| ↓ Пред- и постнагрузки →
↓ Экстраваскулярной компрессии →
расширение крупных коронарных сосудов
| Расширение крупных коронарных артерий →
↑ коллатерального коронарного кровообращения (ККК)
| | | | | |
Применение: при всех формах стенокардии.
Побочные эффекты нитратов
Головная боль – следствие расширения церебральных сосудов и растяжения окружающих тканей.
При приеме после перерыва (рабочие на динамитном производстве отвыкают за выходные
дни, во время отпуска) → в первые дни рабочей недели – головная боль. Для профилактики
– накожные повязки с нитратом. Можно уменьшить выраженность боли предварительным
приемом 40мг анаприлина, 10мг коринфара под язык за 1 час до приема нитрата.
Головокружение – следствие гипотензии более, чем на 10-15мм рт ст от исходного уровня. При в/в введении
развивается у 18% больных и зависит от скорости инфузии.
Ортостатический коллапс – головокружение с обмороком. Не применять стоя сублингвально (таб., аэроз.).
Высокий риск при приеме с алкоголем, диуретиками, при высокой температуре воздуха.
Брадикардия – результат активации Vagus. При в/в введении у 4% больных. При ОИМ нитроглицерин
противопоказан!, т.к. вызывает ↓ САД и ↓ ЧСС.
Тахикардия – результат рефлекторного ↑ СНС (нитраты в неодинаковой степени) более, чем на 10-12уд/мин
по сравнению с исходом. При в/в введении у 1% больных.
Метгемоглобинемия – редко, при частом и длительном приеме пролонгированных нитратов и при в/в
введении в высоких дозах и длительной инфузии.
Обострение глаукомы.
Взрывоопасность нитроглицерина после испарения спирта.
Местное жжение под языком (таблетки нитроглицерина).
Онемение слизистой оболочки рта (аэрозоли).
Контактный дерматит (ТТС, мази).
Замедление скорости реакции (при вождении автомобиля).
Синдром отмены – после курсового лечения и внезапного прекращения введения нитроглицерина (↑ РААС:
↑ ОПС, ↑ ЧСС, ↑ САД).
Толерантность – результат истощения S-Н групп цистеина, ↓ активности ГЦ, цГМФ, и NO в тканях
(нитраты в течение 2-х месяцев вызывают снижение эффекта у 66,6% больных и
укорочение действия у 100% больных. Чаще развивается при приеме пролонгированных
форм, в т.ч. пластырей и ТТС. Чем больше доза, тем больше вероятность толерантности.
Нитросорбит по 80мг каждые 12час или по 20-40мг каждые 6час – толерантность через 2
недели и 8 недель соответственно у 58% больных).
Критерии эффективности нитратов
| - легкая головная боль
| - ↑ ЧСС на 7 – 10 уд/мин
| - ↓ систолического АД на 10 – 15%
| - ↑ толерантности к физической нагрузке
| - ↓ интенсивности и количества приступов стенокардии в сутки
|
| Профилактика толерантности
| Помощь при развитии толерантности
| | - Прерывистый прием (через 10 – 12 час): перед физической нагрузкой (тринитролонг, нитросорбит), не применять ночью.
- Ассиметричное назначение (интервальная терапия): в 8 и 12 час (нитросорбит в тех же дозах не вызывает толерантность, изосорбит 5-мононитрат 2р/д: утром и вечером, утром и днем, 1р/д: утром или вечером при дневных или ночных приступах).
- Чередовать (но не комбинировать) нитраты с ЛС другого механизма действия: АПФ-блок., Са++-блок., β-блок., ментолом.
- Использовать ЛС, действующие не менее 4-12 час, т.к. чем чаще приемы, тем быстрее толерантность и чем больше доза, тем быстрее толерантность.
- Увеличение дозы дает временный эффект.
| - Отменить нитрат на 3 – 5 дней.
- Назначить донаторы S-Н групп: ацетилцистеин, метионин, каптоприл, периндоприл (потенцируют действие нитратов), гидралазин (подавляет метаболизм ЭРФ).
|
Блокаторы Са-каналов
| Эффекты
| Верапамил
| Нифедипин
| | Коронарный кровоток
АД
ЧСС
А-В проводимость
Qо2
| ↑
↓
↓
↓
↓
| ↑↑
↓↓
↑
-
↑
|
| Верапамил
↓
↓ вход Са++ → ↑ тропонин-тропомиозиновое торможение → ↓ взаимодействие актина с миозином → ↓ сокращение → ↓ Qо2
| Верапамил
↓
↓ взаимодействие Са++ с кальмодулином → ↓ киназа легких цепей миозина → ↓ тонус мелких коронарных артерий → ↑ доставка О2
| Применение: вазоспастическая и реже стенокардия напряжения
Осложнения: «Синдром обкрадывания», ↓ силы и ЧСС, ↓ А-В проводимость, ↓ САД.
Нифедипин
Расширяет мелкие КА и ↑ доставку О2 к сердцу; расширяет артериолы > круга и ↓ САД → ↑ ЧСС.
Применение: вазоспастическая стенокардия.
Осложнения: «Синдром обкрадывания» при стенокардии напряжения.
Гиполипидемические средства
| Определение фармакологической группы
| Область применения
| | - ЛС, снижающие повышенное содержание в плазме крови атерогенных липопротеидов и повышающие содержание в плазме крови антиатерогенных липопротеидов.
| Кардиология,
Терапия.
Для лечения атеросклероза.
| | Атеросклероз – хроническое заболевание артерий с поражением прежде всего интимы (внутренний слой – состоит из эндотелиальных клеток, базальной и внутренней мембран, коллагена и эластина – высокомолекулярные соединительнотканные элементы). Связывают с повышенным уровнем холестерина и триглицеридов в плазме крови.
|
Механизмы развития атеросклероза (А)
При накоплении в клеточных мембранах интимы сосудов избытка Х: меняется активность встроенных в них ферментов, обмен веществ (проникновение гормонов, микроэлементов, полиненасыщенных ЖК) и нормальное функционирование клеток. Они начинают усиленно делиться, ↑ пролиферация (разрастание) клеток артерий → клетки захватывают > ЛПНП, в них откладывется > липидов (липоидоз) → разрастает соединительная ткань (фиброз) → сужение просвета сосуда. В пораженных сосудах ↑ тромбообразование.
При ↓ α-ЛП (ЛПВП) - ↓ содержание ФЛ, к тому же обедненных полиненасыщенными ЖК, которые не синтезируются в организме, а поступают только с пищей.
При ↑ β-ЛП (ЛПНП) - ↑ атеротромбоз: на месте надрыва бляшки ↑ образование ТХ-А2 из ненасыщенных ЖК, ↑ агрегация ТЦ. Необходимо стабилизировать бляшки.
α-ЛП (ЛПВП): ↓ агрегацию ТЦ и ↓ атерогенез.
β-ЛП (ЛПНП): ↑ агрегацию ТЦ и ↑ атерогенез.
Группы ЛП
| Хиломикроны (ХМ)
| ЛПОНП (пре-β-ЛП)
| ЛПНП (β-ЛП)
| ЛПВП (α-ЛП)
| | Образуются в клетках эпителия тонкого кишеч-ника при всасывании триацилглицерола (триглицеридов, ТГ).
| Образуются в печени и используются для экспо-рта триацилглицерола (ТГ).
| Конечная стадия катабо-лизма ЛПОНП и ЛППП. Мембраны клеток содер-жат ЛП-рецепторы для эндоцитоза ЛПНП.
| Образуются в печени, в кишечнике и при катабо-лизме ХМ и ЛПОНП.
Содержат ФЛ и специи-фический белок.
| | Основной липид ХМ и ЛПОНП – триацилглицерол. Поступает в плазму и покидает ее 70-150г/сут.
| Основные липиды ЛПНП и ЛПВП – Х и ФЛ. Поступают в плазму и покидают ее 1-2г/сут
| | Самые крупные ЛП – пе-реносят экзогенные (пи-щевые) ТГ от кишечника через грудной проток в венозную систему. Появляются в крови через 2-10ч. после еды. 90% глицеридов отщеп-ляется ЛП-липазой в ка-пиллярах жировой и мы-шечной ткани с образо-ванием ЖК и глицерина, которые поступают в адипоциты и мышечные клетки, где запасаются для образования Е, и ре-синтеза ТГ. Остатки ХМ поглощает и катаболизи-рует печень.
| Переносят эндогенные ТГ из печени в перифе-рические адипоциты и мышечные клетки для запасания и утилизации. ЛП-липазы эндотелия сосудов быстро разруша-ют ЛПОНП с образова-нием ЛППП (содержат ТГ-40% и Х - 30%), кото-рые при участии ТГ-ли-пазы печени, за 2-6ч, ра-спадаются далее, теряя еще больше глицеридов и превращаясь липоли-зом в ЛПНП (в них Х – атерогенен) и 50% захва-тываются печенью через ЛП-рецепторы.
| Т1/2 = 3-4сут. Транспортируют 60-75% эфиров Х. 60% ЛПНП удаляется из циркуляции в крови печенью, связы-ваясь с апобелком В. Небольшая часть ЛПНП удаляется из крови нере-цепторным путем (пог-лощается макрофагами-мусорщиками, способ-ными мигрировать в стенку артерий, где Х участвует в образовании пенистых клеток атеро-склеротической бляшки).
| Самые мелкие частицы.
Переносят 20-25% Х. ЛПВП легко проникают через неповрежденный эндотелий и удаляют избыток Х из тканей. В ЛПВП из Х образуются осколки ХМ и сложные эфиры Х с ненасыщен-ными ЖК (линолевой, арахидоновой), которые транспортируются в пе-чень или самими ЛПВП или специальными тран-спортными белками в ЛПОНП, ЛППП, ЛПНП.
| Х, ТГ, ФЛ переносят Х в плазме крови в составе макромолекулярных комплексов – ЛП. Гидрофобное ядро ЛП содержит ТГ и эфиры Х, а оболочка – ФЛ, Х и апопротеины. Апопротеины – составная часть ЛП, необходимы для растворения и транспорта липидов (Х, сложных эфиров Х, ТГ, ФЛ).
Группы апобелков
| Апо-А
| Апо-В
| Апо-С
| Апо-Е
| Апо-Д
| | В ЛПВП и ХМ.
↑ образование эфиров Х в плазме крови.
Обеспечивает холестерином синтез клеточных мембран при их повреждении.
| Апо-В-100 (синтезируется в печени) –
в ЛПНП (5% в составе УВ – гликопротеиды: Апо-В + глюкоза)
и в ЛПОНП.
Апо-В-48 (синтезируется в кишечнике) - в ХМ.
| В ЛПОНП, ЛПВП и ХМ. Небольшие полипептиды, которые могут переходить от одного ЛП к другому. Освобождают кровь от ТГ.
| В ЛПОНП. 5-10% от общего количества апобелков в ЛПОНП.
| В ЛПВП. Переносят эфиры Х от ЛПВП в клетки печени.
| | Функции: сохранение структуры ЛП; связывание с рецепторами ЛП в печени и др. тканях; ко-факторы ферментов, метаболизирующих циркулирующие ЛП.
|
Метаболизм ЛП плазмы крови
| Метаболизм СЖК
| | СЖК (неэстерифицированные ЖК) поступают в плазму крови в результате липолиза ТГ, катализируемого липазой в жировой ткани. В плазме СЖК (пальмитиновая, стеариновая, олеиновая, линолевая…) связаны с сывороточными альбуминами. Концентрация СЖК уменьшается в плазме сразу после приема пищи. В цитозоле многих клеток есть Z-белок, связывающий ЖК и обеспечивающий их транспорт внутри клеток многих тканей. При голодании СЖК окисляются и поставляют 25-50% Е, необходимой для жизнедеятельности организма. При голодании и употреблении жирной пищи, сахарном диабете уровень СЖК в крови увеличивается и они поглощаются печенью.
| | Метаболизм хиломикронов и ЛПОНП
| | Образование ХМ и ЛПОНП
| Катаболизм ХМ и ЛПОНП
| | ХМ и ЛПОНП сходно образуются и содержат апобелок-В.
ХМ находятся в хилусе (млечном соке), образующемся только в лимфатической системе кишечных ворсинок. ХМ образуются даже при голодании и переносят 50% ТГ и Х лимфы. При всасывании ТГ после приема пищи количество ХМ возрастает. Источниками липидов, необходимых для их образования являются желчь и секрет кишечника.
Хиломикроны образуются в клетках кишечника.
ЛПОНП образуются в печени и переносят ТГ из печени в другие ткани.
| После поступления в кровь: Т1/2 ХМ = 1ч. (мелкие живут дольше, чем крупные). ХМ поступают в жировую ткань, сердце и мышцы (80%), в печень (20%). ЛП-липаза на стенке эндотелия капилляров катализирует гидролиз триацилглицеролов (ТГ) в крови до диацилглицерола, затем до моноацилглицерола и до СЖК и глицерола.
ФЛ и апобелок-С – кофакторы ЛП-липазы.
Т.о. ХМ и ЛПОНП обеспечивают фермент, катализирующий их метаболизм, как субстратом, так и кофактором.
| | Метаболизм ЛПНП
| | ЛПНП образуются из ЛПОНП в печени. Содержат апобелок-В (Т1/2= 2,5 сут). на гладкой мускулатуре артерий, мембране лимфоцитов есть рецепторы (участки связывания) В-100 для ЛПНП.
При семейной гиперХемии эти рецепторы не работают.
Деградируются ЛПНП в печени (50%) и других тканях (50%).
| | Метаболизм ЛПВП
| | ЛПВП синтезируются в кишечнике и печени и транспортируют Х от различных тканей к клеткам печени.
Содержат апобелки-С и Е, необходимые для метаболизма (↑ липазы) ХМ и ЛПОНП. Апобелок-Д переносит эфиры Х из ЛПВП в клетки печени.
Уровень ЛПВП уменьшается при физической нагрузке и умеренном потреблении алкоголя и увеличивается при курении ожирении, стероидной контрацепции с прогестинами.
| | Метаболизм ТГ
| | ТГ образуются в печени при участии ЖК, которые либо синтезируются в печени из АцКоА (образуется из УВ), либо поступают в виде СЖК из крови (при голодании, сахарном диабете).
ТГ входят в состав ЛПОНП и в таком виде транспортируются из печени.
Увеличивается образование ТГ и секреция ЛПОНП печенью при: употреблении пищи богатой УВ (сахарозой, фруктозой); ↑ содержания СЖК в крови (при голодании, употреблении жирной пищи, сахарном диабете), они поглощаются печенью и превращаются в ЖК; употреблении этанола; ↑ концентрации инсулина и ↓ концентрации глюкагона.
| 
| Роль печени в метаболизме ЛП
| Жировое перерождение печени
| | - Ускоряет переваривание и всасывание липидов, вырабатывая желчь в состав которой входит Х и желчные кислоты, синтезируемые печенью;
- Содержит активные ферментные системы, катализирующие синтез и окисление ЖК, синтез ФЛ, Х, ТГ;
- Синтезирует ЛП плазмы крови, интегрирует их метаболизм;
- Превращает ЖК в кетоновые тела.
| - Липиды (главным образом ТГ) могут накапливаться в печени, вызывать фиброзные изменения и цирроз;
- Увеличение концентрации СЖК в плазме крови (в результате повышенной мобилизации из жировой ткани, повышенного гидролиза ТГ входящих в состав ЛП или ХМ внепеченочной ЛП-липазой) → ↑ поглощение и эстерификация СЖК клетками печени → недостаток ЛП, необходимых для утилизации поступающих СЖК и последние накапливаются в печени в виде ТГ → жировое перерождение печени.
|
Биосинтез холестерола (Х)
- В микросомах эндоплазматического ретикулума и в цитозоле всех клеток не утративших ядро.
АцКоА – источник всех атомов углерода в молекуле Х.
| Стадии синтеза Х:
| | 1. АцетилКоА в цитозоле клеток печени → мевалонат (содержит 6 атомов углерода).
2. Мевалонат-СО2 → изопентилпирофосфат.
3. 6 изопреноидных единиц (изопентилпирофосфат) конденсируются → сквален.
4. Сквален циклизуется → ланостерол.
5. Ланостерол → зимостерол → холестадиенол (удаление 3-х метильных групп от стероида) → демостерол (24 дегидрохолестерол) → холестерол (в мембранах эндоплазматического ретикулума печени).
| АцКоА
↓
ацетоАцКоА
↓
β-окси-β-метилглутарил КоА
↓ГМГ-КоА-редуктаза
Мевалоновая кислота
↓
промежуточные продукты
↓
Сквален
↓
ХОЛЕСТЕРИН
|
Регуляция синтеза Х:
| ↓ Синтеза: при голодании,
при связывании ЛПНП с апо-В-100,
под действием глюкагона и ГКС,
при содержании Х в пище > 2%;
Ограничивают скорость ночного синтеза Х печенью: всасывание Х и реабсорбция желчных кислот.
↑ Синтеза: под действием инсулина и тиреоидных
гормонов.
| Полного прекращения синтеза Х не происходит даже при большем увеличении содержания в пище - синтез снижается только в печени. При содержании Х только 0,05% в пище – синтез эндогенного Х на 70-80% осуществляется в печени, тонком кишечнике, надпочечниках. Т.о. уменьшая количество Х в пище можно снизить уровень Х в крови. При повышении уровня Х: активность ГМГ-КоА-редуктазы уменьшается (принцип обратной связи).
|
Баланс Х в тканях:
| Во все ткани Х поступает через рецепторы к ЛПНП (апо-В-100). Катаболизм Х осуществляется через рецепторы печени. Освобождение клеток почти всех тканей (кроме печени, коры надпочечников, тестикул) от избытка Х осуществляется эстерификацией, т.е. связыванием с ЖК либо при участии ЛПВП.
| | Увеличение Х в тканях
| Уменьшение Х в тканях
| | - При захвате холестеринсодержащих ЛП рецепторами ЛПНП;
- При захвате ЛПНП без участия рецепторов апо-В;
- При захвате свободного Х, содержащегося в богатых им ЛПНП и ЛПОНП, клеточными мембранами;
- При синтезе Х;
- При гидролизе эфиров Х под действием гидролазы;
- При дефиците вит.С (↓ образование желчных кислот из Х на стадии гидроксилирования).
| - При переходе Х из мембран в ЛПВП при участии апо-1-белка и ЛХАТ (лецитин-холестерин-ацетил-трансфераза);
- При эстерификации Х при участии АХАТ (ацетил-КоА-холестерин-ацетилтрансфераза, у человека низкая активность);
- При использовании Х для синтеза других стероидов: гормонов или желчных кислот в печени.
| 
Рецепторы ЛПНП
Апо-В-100 захватывает ЛПНП путем эндоцитоза в клетку. В лизосомах ЛПНП распадаются, при этом эфиры Х гидролизуются, а свободный Х выходит в цитоплазму, где подавляет синтез Х и активирует эстерификацию Х (связывание с ЖК). Количество рецепторов регулируется в зависимости от потребности клетки в Х, необходимом для образования мембран и биосинтеза гормонов. При увеличении концентрации Х в клетке – уменьшается количество рецепторов ЛПНП.
Апо-В-100 и Апо-Е – высокоаффинные рецепторы ЛПНП на мембранах клеток, легко насыщаются (есть низкоаффинные рецепторы).
Транспорт Х между тканями
В плазме крови человека ~ 200мг Х/100мл и с возрастом содержание Х увеличивается.
Большая часть Х находится в эстерифицированной форме и переносится в составе ЛП. Наибольшая доля Х находится в ЛПНП. Но при преобладании ЛПОНП, доля Х больше в них.
Х, поступающий с пищей приходит в равновесие с Х плазмы через несколько дней, а с Х тканей через несколько недель. Период полуобновления Х в печени непродолжителен, но для организма в целом он составляет несколько недель. Равновесие между Х плазмы крови и печени достигается за несколько часов.
ЭХ, поступающие с пищей гидролизуются до свободного Х, который смешивается с поступившим свободным Х и Х желчи перед абсорбцией вместе с другими липидами. Далее Х смешивается с Х, синтезированным в стенке кишечника и встраивается в ХМ. 80-90% абсорбированного Х эстерифицируется в слизистой оболочке кишечника длинноцепочечными ЖК. Плохо всасываются ситостеролы (стеролы растительного происхождения).
Когда ХМ атакуются ЛП-липазой и образуются их остатки, теряется только 5% ЭХ. После взаимодействия с апо-Е рецептором остатки ХМ поступают в печень, где ЭХ гидролизуются до свободного Х. Образующиеся в печени ЛПОНП переносят Х в плазму крови. Большая часть Х в ЛПОНП поглощается печенью, либо превращается в ЛПНП. ЛПНП связываются с рецепторами печени и других тканей. ЛПВП переносят Х из тканей в печень и содержат апобелок-А-1 и обладают активностью ЛХАТ (участвует в образовании ЭХ при переходе Х из мембран в ЛПВП). Апобелок в составе ЛПВП (переносчик ЭХ в плазме крови) идентичен апобелку Д, он ускоряет перенос ЭХ от ЛПВП к ЛПОНП, ЛПНП и ХМ.
Т.о. белок переносчик ЭХ способствует уменьшению ингибирования ЛХАТ, связанной с ЛПНП. У человека большая часть ЭХ, образованных при действии ЛХАТ в ЛПВП, поступает в печень в составе ЛПОНП или ЛПНП.
В конце концов весь Х, который должен быть выведен из организма, поступает в печень и экскретируется с желчью либо в виде Х, либо в виде солей желчных кислот.
Выведение Х и образование желчных кислот
Из организма выделяется ~ 1г Х/день: ~ 50% с фекалиями после превращения в желчные кислоты, ~ 50% в виде нейтральных фекальных стероидов (капростанол – образуется под действием флоры кишечника). Большая часть Х попав в желчь реабсорбируется в кишечнике и вновь через воротную вену поступает в печень и желчь (энтеро-гепатическая циркуляция).
Первичные желчные кислоты синтезируются из Х в печени путем гидроксилирования при участии О2, НАДФН и цитохрома Р-450: образуются холевая и хенодезоксихолевая кислоты. Их синтез уменьшается при недостатке вит.С → ↑ накопление Х → атеросклероз. В норме эти желчные кислоты поступают в желчь в виде коньюгатов с глицерином и таурином в соотношении 3:1. в желчи много Na+ и К+ → щелочная рН → желчные кислоты находятся в форме солей («желчные соли»). В кишечнике часть первичных желчных кислот под действием бактерий деконьюгируются и дегидроксилируются в результате образуются вторичные желчные кислоты: из холевой – дезоксихолевая, из хенодезоксихолевой – литохолевая (она плохо растворяется и не реабсорбируется в кишечнике).
Продукты переваривания липидов, в т.ч. Х, всасываются в верхнем отделе (первые 100см) тонкого кишечника. Первичные и вторичные желчные кислоты – только в подвздошной кишке. 98-99% (~ 3-5г) желчных кислот, поступивших в кишечник возвращаются через систему воротной вены в печень (6-10 раз/сут). За 1 цикл из организма выводится ~ 1-2% желчных кислот (кроме литохолевой). ~ 500мг/сут желчных кислот не абсорбируется и выделяется с фекалиями (это основной путь выведения Х). для восполнения потери желчных кислот с фекалиями, в печени постоянно синтезируются желчные кислоты из Х (регулируется синтез по принципу обратной связи).
ГиперХемию можно лечить прервав ЭГЦ: назначить холестираминовую смолу или выключить хирургически подвздошную кишку.

Дислипопротеинемии
| - Нарушение обмена ЛП плазмы крови в результате нарушения одной из стадий синтеза, транспорта или деструкции ЛП: первичная гипер- или гипоЛПемия. У больных сахарным диабетом, гипотиреозом, атеросклерозом – нарушения обмена ЛП сходные с наследственной дисЛПемией.
| | Гиперлипопротеинемии
| Гиполипопротеинемии
|
Гиперлипопротеинемии
| Тип
| Клиника
| Лечение
| | Ι.
– Экзогенная гиперТГемия, семейная индуцируемая жирами липидемия, гиперХМемия.
Редкая врожденная аутосомно-рецессивная недостаточность ак-тивности ЛП-липазы либо активи-рующего белка-катализатора апо-липопротеина С-2 → нарушение очищения крови от ХМ (замед-ленное их выведение).
| Проявляется в детстве или моло-дости (боли в животе, розово-жел-тые ксантомы на сдавливаемых участках кожи и разгибательных поверхностях, липемия сетчатки, увеличение печени и селезенки), особенно при увеличении в рацио-не жиров → ↑ ХМ. Панкреатит, ↑ болей после жирной пищи. Атеро-склероз не развивается. Уровень Х N; ТГ ↑; ЛПОНП ↑ или N; ЛПНП и ЛПВП ↓ или N.
| Диета с ↓ содержанием всех исто-чников жира, который вызывает гиперТГемию (насыщенные, нена-сыщенные, полиненасыщенные Ж необходимо заменить жирными кислотами, которые не образуют ХМ, а связываются с альбумина-ми и поступают в систему ворот-ной вены и печень).
Отказ от алкоголя.
Диета с ↑ содержанием сложных УВ.
| | ΙΙ.
– Семейная гиперХемия, гипер- βлипопротеинемия, семейный ги-перХемический ксантоматоз.
Частая аутосомно-доминантная болезнь – генетическое наруше-ние липидного обмена. Семейный характер обусловленный домина-нтным геном с полной пенетрант-ностью. Причина – отсутствие или дефект клеточных рецепторов ЛПНП → ↓ элиминации Х ЛПНП ↑ в крови Х ЛПНП. ГиперХемия в результате ↓ активности гидролаз.
ΙΙ В
Семейная смешанная гиперХемия.
Встречается редко. Наследуется как доминантныйпризнак и не проявляется до полового созрева-ния. Обусловлена избыточным образованием апобелка-В в пече-ни (главный белок ЛПНП и ЛПОНП) → ↑ ЛПНП + ↑ ЛПОНП.
ΙΙ А
Полигенная гиперХемия. Гетерогенная группа заболеваний наиболее частая. ↑ ЛПНП, кото-рые плохо связываются с рецепто-рами, т.к. ЛП аномальны → ↓ очи-щение плазмы (↓ элиминации).
Семейная гиперαЛПемия.
↑ Уровень ЛПВП.
Вторичная гиперХемия.
При билиарном циррозе печени (↑ ФЛ и Х). ↑ Концентрация ЛПНП при гипотиреозе, сахарном диабете.
↑ концентрация ЛПВП у женщин в период постменопаузы или при гормональной контрацепции эстрогенами.
| ↑ уровень ОХ в крови в сочетании с ксантелазмой, ксантомами сухо-жилий и бугорчатыми ксантома-ми, ювенильной дугой роговицы, ускоренным развитием атероскле-роза и ранней смертью от ИМ. Тяжелее протекает у гомозигот, чем у гетерозигот. ↑ в крови Х ЛПНП накопление ЛПНП в облас-ти суставов, в местах сдавления кожи и сосудах (ксантомы в области ахилловых сухожилий, надколенника и разгибателей пальцев). До 55 лет развитие ИБС. Уровень Х > N в 2-3 раза. Уровень ТГ N, уровень ФЛ N. Высокий риск атеросклероза коронарных артерий, особенно быстро разви-вается у мужчин. Появляется еще до 10 лет.
Предрасположенность к преждевременному развитию ИБС.
Благоприятно для здоровья человека.
| Диета не менее 6 мес. с ↓ содержа-нием Х и насыщенных Ж (т.к. они ↓ активность печеночных рецеп-торов ЛПНП → ↑ их накопление).
Насыщенные Ж заменить на мо-ноненасыщенные → ↓ ЛПНП и не ↓ ЛПВП; на полиненасыщенные → ↓ и ЛПНП и ЛПВП; на УВ → ↑ ТГ и ↓ ЛПВП. Уменьшить массу тела (лишний вес и избыток калорий → ↓ ЛПВП |
|










