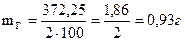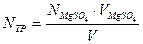Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Приготовление раствора ЭДТА (комплексна III)Содержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Определение нормальности и титра раствора комплексона III по сульфату магния Цель: Изучить комплексонометрический метод титрования Посуда и реактивы: Трилон Б, фиксанал сульфата магния или титрованный раствор, бюретка, пипетка, коническая колба, аммиачная буферная смесь, индикатор хром темно-синий, или эриохром черный Задание: Выполните опыты, оформите отчет. Правила техники безопасности: 1.Правила работы с реактивами. 2.Правила работы с химической посудой Методические указания к выполнению лабораторной работы: В основе метода находятся реакции образования комплексных соединений (металло-лигандные реакции). Наибольшее значение из комплексонов имеет этилендиаминтетрауксусная кислота и ее двунатриевая соль (комплексон III или трилон Б – Na2H2T). Формула Трилона Б HOOCH3C H H CH3COONa \ | | / N – C = C – N NaOOCH3 / | | \ CH3COOH H H Ход работы: 1.Производим расчет навески для приготовления 100мл 0,05н. раствора Трилона Б, (динатриевая соль этилендиаминтетрауксусной кислоты) необходимо взять:
2.Установливаем титр раствора по 0,05 н. раствору сульфату магния, титрованному из фиксанала. 3.Отбираем пипеткой раствор в коническую колбу, добавляем половину объема аммиачного буфера, 80-90мл воды, щепотку индикатора, раствор окрасится в бурячный цвет.
| ||||||||||||||||||||||||||
|
| |||||||||||||||||||||||||||
| Изм | Лист | № докум. | Подп. | Дата | |||||||||||||||||||||||
| Разраб. | Лит. | Лист | Листов | ||||||||||||||||||||||||
| Пров. | |||||||||||||||||||||||||||
|
| |||||||||||||||||||||||||||
| Н. контр. | |||||||||||||||||||||||||||
| Утв. | |||||||||||||||||||||||||||
4.Титрование производим до перехода окраски от бордовой в синею. 5.По среднему значению трех сходящихся результатов объемов титранта рассчитываем нормальность раствора Трилона Б.
Результаты заносим в таблицу:
Таблица
Рассчитываем нормальность и титр Трилона Б:
Контрольные вопросы 1. Суть комплексонометрического метода. 2. Индикатор, применяемый при установлении титра раствора Трилона Б. 3. Понятие о буферных растворах, их назначение и классификация.
4. Как готовиться титрованный раствор сульфата магния? 5. Расчет нормальности раствора. 6. Ход работы по приготовлению титрованного раствора Трилона Б и установлення его титра. 7. Техника безопасности, соблюдаемая при работе. 8. Какой необходимо предусмотреть переход окраски индикатора? 9. Формула Трилона Б и его реакционная формула.
| |||||||||||||||||||||||||||
| Лист | |||||||||||||||||||||||||||
| Изм | Лист | № докум. | Подп. | Дата | |||||||||||||||||||||||
|
Лабораторная работа № 29 Определение ионов металлов в растворах данным методом Цель: Научиться определять содержание металлов в их солях комплексонометрическим методом прямого и обратного титрования с использованием различных индикаторов. Посуда и реактивы: бюретка, пипетка, колба коническая, пробирка аналитическая, реактивы для получения качественных реакций, стакан для слива, ЭДТА титрованный, 25%-ный аммиак, мурексид, насыщенный раствор ацетата аммония, 2%-ный аммиак, аммиачный буферный раствор, эриохром черный Т,. контрольные растворы солей: меди, никеля, кобальта, магния, цинка Задание: Выполните опыты, оформите отчет.
|
|||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-05-12; просмотров: 449; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.149.238.67 (0.008 с.) |
|||||||||||||||||||||||||||