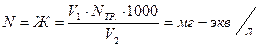|
Лабораторная работа № 20 Определение временной жесткости воды Цель: научиться определять временную жесткость воды, производить расчеты, применяя «закон эквивалентов», отработать навыки проведения анализа методом кислотно-основного титрования. Посуда и реактивы: мерная колба, исследуемая вода, индикатор, раствор соляной кислоты, бюретка. Задание: Выполнить опыты, оформить отчет. Правила техники безопасности: 1.Правила работы с реактивами. 2.Правила работы с химической посудой Методические указания к выполнению лабораторной работы: Уравнение реакции Са(НСО3)2+2НСl=СаСl2+2Н2О+2СО2 Мg(НСО3)2+2НСl=МgСl2+2Н2О+2СО2 Ход работы 1. Получить образцы воды для исследования. 2.Мерную колбу на 100мл два-три раза ополаскиваем исследуемой водой. 3.Наполняем ее до метки и количественно переносим в коническую колбу. 4. Прибавляем 1-2капли метил-оранжевого. 5.Титрование производим соляной кислотой до бледно-розового окрашивания. Рассчитываем жесткость воды. Результаты титрования записать в таблицу:
| |||||||||||||||||||||||||||||||
| Изм | Лист | № докум. | Подп. | Дата | |||||||||||||||||||||||||||
| Разраб. | Лит. | Лист | Листов | ||||||||||||||||||||||||||||
| Пров. | |||||||||||||||||||||||||||||||
| . | |||||||||||||||||||||||||||||||
| Н. контр. | |||||||||||||||||||||||||||||||
| Утв. | |||||||||||||||||||||||||||||||
Оформление результатов Рассчитать временную жесткость воды (Ж врем в мэкв/л) по формуле:
Сн (HCl) × V сред(HCl) Ж врем = --------------------------------- · 1000 V(H2O) Контрольные вопросы 1. В чем суть кислотно-основного метода титрования? 2.Что такое титрант? 3. Почему вода содержащая гидрокарбонаты кальция и магния имеет щелочную среду? 4. Какие виды жесткости вам известны? Какими ионами обусловлен тот или иной вид жесткости? 5.В каких единицах измеряется жесткость и как она рассчитывается? 6.На чем основано определение временной жесткости воды? 7. Какой закон применяется при обработке результатов кислотно-основного титрования. 8. Охрана труда при выполнении лабораторной работы.
| |||||||||||||||||||||||||||||||
| Лист | |||||||||||||||||||||||||||||||
| Изм | Лист | № докум. | Подп. | Дата | |||||||||||||||||||||||||||
|
| |||
| МИНИСТЕРСТВО ОБРАЗОВАНИЯ, НАУКИ И МОЛОДЕЖИ РЕСПУБЛИКИ КРЫМ | |||
| ГБОПУ РК «КЕРЧЕНСКИЙ ПОЛИТЕХНИЧЕСКИЙ КОЛЛЕДЖ» | |||
|
| |||
|
| |||
|
| |||
|
| |||
|
| |||
|
| |||
| Лаборатория | химического анализа | ||
|
| |||
|
| |||
|
ЖУРНАЛ | |||
|
| |||
| ЛАБОРАТОРНЫХ РАБОТ | |||
| (ОТЧЕТЫ) | |||
| по дисциплине ОП.03 Аналитическая химия | |||
|
| |||
|
| |||
| ЛР.____.18.02.01.___.___ | |||
|
| |||
|
| |||
|
| |||
|
| |||
|
| |||
|
| |||
|
| |||
|
| |||
|
| |||
| Группа | _______________ | ||
|
| |||
| Студент | ________________ | ||
|
| ________________ | ||
|
| |||
| Преподаватель | ________________ | ||
|
| ________________ | ||
|
| |||
|
| |||
|
| |||
|
| |||
| Керчь | |||
| 20__ г. | |||
|
| |||
|
Лабораторная работа № 1 Реакции на ионы Na +, K +, NH 4 + Цель: освоить технику лабораторного качественного анализа, освоить методику анализа катионов I аналитической группы и характерные реакции обнаружение ионов Na+, К+, NH4+. Посуда и реактивы: пробирки, микроскоп, сушильный шкаф,пробирка держатель, спиртовка, фильтровальная бумага, индикаторная бумага, стеклянные палочки, предметное стекло, синее (кобальтовое) стекло, тигель (фарфоровая чашка), пипетки, водяная баня, раствору солей натрия, калия, аммония, уранилацетат магния, гексагидроксиантимонат калия(V) – K[Sb(OH)6], кобальтинитрит натрия (гексанитрокобальтиат натрия) - Na3[Co(NO2)6], гидротартрат натрия – NaHC4H4O6,, Реактив Несслера -K2[HgJ4] – щелочной р-р комплексной соли ртути.
Задание: Выполнить задание, оформить отчет.
|
||||||||||||||
|
Последнее изменение этой страницы: 2021-05-12; просмотров: 150; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.136 (0.008 с.) |
||||||||||||||




 OOCH2C CH2COO
OOCH2C CH2COO