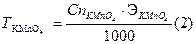Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Правила техники безопасности:. 1.Правила работы с реактивами.
1.Правила работы с реактивами. 2.Правила работы с химической посудой. 3.Правила работы с нагревательными приборами.
Методические указания к выполнению лабораторной работы: Для установки титра раствора KMnO4 предложено много различных стандартных веществ, например Н2С2O4·2Н2О, Na2С2O4, К4[Fе(СN)6]·3Н2О, Аs2O3, металлическое железо и т. п. Оксалат аммония обладает некоторыми преимуществами по сравнению с другими установочными веществами: хорошо кристаллизуется и легко растворяется в воде, имеет определенный химический состав и не изменяется при хранении, не взаимодействует с кислородом воздуха и СО2 Уравнение реакции: 5(NH4)2C2O4 + 2KMnO4 + 8H2SO4 = 2MnSO4 + K2SO4 + 5(NH4)2SO4 +8H2O + 10CO2↑
Ход работы:
1. Бюретку заполняем титрованным раствором перманганата калия по правилу. Определение ведем по верхнему мениску! 2. Пипеткой отбираем точный объем раствора оксалата аммония. 3. Добавляем столько же мензуркой 2н. серной кислоты. 4. Коническую колбу нагреваем на водяной бане, не доводя до кипения. 5. Горячий раствор в конической колбе титруем раствором KMnO4. 6. Титрование прекращаем, когда в конической колбе раствор окрасится в бледно розовый цвет. 7. Результаты титрования записываем в таблицу.
| ||||||||||||||||||||||||||
|
| |||||||||||||||||||||||||||
| Изм | Лист | № докум. | Подп. | Дата | |||||||||||||||||||||||
| Разраб. | Лит. | Лист | Листов | ||||||||||||||||||||||||
| Пров. | |||||||||||||||||||||||||||
|
| |||||||||||||||||||||||||||
| Н. контр. | |||||||||||||||||||||||||||
| Утв. | |||||||||||||||||||||||||||
Таблица
По среднему объему KMnO4 производим расчеты нормальности и титра раствора перманганата калия:
Кф- фактор пересчета, или поправочный коэффициент Расчет:
Контрольные вопросы 1. Почему этот метод титрования называется окислительно-восстановительным? 2. Какова роль величины электродного потенциала в определении направления химической реакции процесса? 3. Почему здесь не применяется индикатор? 4. Почему серную кислоту необходимо лить в воду? Для чего она применяется в этой реакции? Напишите уравнение реакции. 5. Ход работы по определению титра перманганата калия.
6. Как рассчитать нормальность и титр раствора, фактор пересчета. 7. Техника безопасности, соблюдаемая при работе. | |||||||||||||||||||||||||||
| Лист | |||||||||||||||||||||||||||
| Изм | Лист | № докум. | Подп. | Дата | |||||||||||||||||||||||
|
Лабораторная работа № 24 Определение железа в соли Мора Цель: Углубить навыки титрования растворов окислительно-восстановительного метода. Определить наличие ионов Fe2+ в растворе соли Мора. Посуда и реактивы: Колба с исследуемым раствором соли Мора, бюретка, пипетка, 2н. серная кислота, титрованный раствор перманганата калия, колба коническая, мензурка. Задание: Выполните опыты, оформите отчет.
|
|||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-05-12; просмотров: 95; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.191.135.224 (0.005 с.) |
|||||||||||||||||||||||||||