
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Дослід 1. Окиснення альдегіду реактивом ФелінгаСодержание книги
Поиск на нашем сайте
МАТЕРІАЛИ: розчини Фелінга, альдегіду. У пробірку долити 3-4 краплі свіжоприготовленого розчину Фелінга і додати 1-2 краплі альдегіду. Суміш нагріти. Спостереження. Висновок. Напишіть рівняння реакції. Дослід 2. Окиснення альдегідів аміачним розчином аргентум оксид МАТЕРІАЛИ: аміачний розчин окису срібла. У знежирену пробірку налити 3 краплі аміачного розчину окису срібла і додати 10 крапель розчину альдегіду. Повільно нагріти. Спостереження. Висновок. Напишіть рівняння реакції. Дослід 3. Окиснення альдегідів купрум (ІІ) гідроксид МАТЕРІАЛИ: розчини NaOH, СuSO4, формальдегіду. У пробірку помістити 4 краплі розчину їдкого натрію, додати 2 краплі розчину сірчанокислої міді. До осаду, що випав, додати одну краплю розчину формальдегіду і збовтати. Нагріти. Спостереження. Висновок. Напишіть рівняння реакцій.
Література: 1 (147-167, 400-405), 2 (192-210); 5 (93-104). ТЕМА 7. КАРБОНОВІ КИСЛОТИ Методичні поради до вивчення теми Карбоновими кислотами називають органічні сполуки, які мають в молекулах функціональну групу карбоксильну
По кількості карбоксильних груп карбонові кислоти розподіляють на одноосновні і багатоосновні. Карбонові кислоти частіше називають за тривіальною номенклатурою. Для всіх кислот характерні реакції з участю карбоксильної групи:
Зміщення електронної густини в карбоксилі приводить до дисоціації кислот:
Усі карбонові кислоти мають кислотні властивості: змінюють забарвлення індикаторів, утворюють солі. Карбонові кислоти можуть давати похідні, коли -ОН у карбоксилі заміщується на іншу групу атомів:
Cl || || O O R - C - O - R - складні ефіри, R - С = О – аміди.
О NH2 У хімічних реакціях беруть участь і вуглеводневі радикали кислот. Радикали насичених і ненасичених кислот по- різному реагують з одним і тим же реагентом. 1) Реакція заміщення водню:
ОН | пропіонова кислота Cl 2 - хлорпропіонова кислота 2) Реакція приєднання:
CH2 = CH – СООН | | пропенова кислота Cl Cl 2, 3 - дихлорпропанова кислота Зверніть увагу на здатність ненасичених кислот приєднувати водень:
CH3 - (CH2)7 - CH = CH - (СH2)7 - COOH ¾¾¾¾® олеїнова кислота (рідина) ® CH3 - (CH2)7 - CH2 - CH2 - (СH2)7 - COOH стеаринова кислота (тверда сполука) Така реакція лежить в основі перетворення рідких олій у тверді жири. Карбоксильна група входить до складу сполук інших класів. Термінологічний словник Ацильний радикал (або ацил) — залишок карбонової кислоти, утворений відніманням гідроксильної групи від карбоксилу кислоти, (від латинського Асіdum — кислота). Дикарбонові кислоти - органічні сполуки, молекули яких містять дві карбоксильні групи. Функціональні похідні карбонових кислот - утворюються при заміщення гідроксилу карбонових кислот (галогенангідриди, ангідриди, складні ефіри, аміди).
Тема 7. Карбонові кислоти План лабораторного заняття 1. Повторення матеріалу теми. 2. Письмова контрольна робота. 3. Виконання експериментальної частини 4. Оцінка знань теорії. Завдання для самостійної підготовки до лабораторного заняття № 7 1. Карбонові кислоти. Класифікація. 2. Гомологічний ряд одноосновних карбонових кислот. Номенклатура. 3. Будова карбоксильної групи і карбоксилат-аніона. 4. Фізичні властивості. 5. Хімічні властивості. Кислотний характер. Похідні карбонових кислот, їх одержання і властивість. 6. Двохосновні карбонові кислоти насиченого і ненасиченого характеру. Особливості фізичних і хімічних властивостей. 7. Вищі жирні кислоти. 8. Ароматичні кислоти. Бензойна кислота як сполука з двоїстою функцією. 9. Методи одержання карбонових кислот 10. Значення органічних кислот у харчовій промисловості. Окремі представники: мурашина, оцтова, масляна, щавлева, бурштинова, глутарова, адипінова, сорбінова, олеїнова, лінолева, ліноленова, малеїнова, фумарова, бензойна кислоти. 11. Одержати ізомасляну кислоту виходячи з пропілену і деяких неорганічних речовин. Як одержати пропіонову кислоту з бромистого етилу? 12. Виходячи з ацетооцтового ефіру напишіть схеми синтезу: а) масляної кислоти; б) брометилкетону. Завдання до лабораторного заняття №7 та методичні рекомендації
|
|||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-07; просмотров: 212; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.138.190.225 (0.01 с.) |

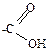 , зв’язану з вуглеводневим радикалом
, зв’язану з вуглеводневим радикалом  .
.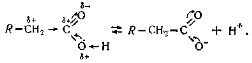
 R - С = О - галогенпохідні, R - C - O - С - R - ангідриди,
R - С = О - галогенпохідні, R - C - O - С - R - ангідриди, || |
|| | CH3 - CH2 - С = О
CH3 - CH2 - С = О 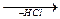 CH3 - CH - СОOH
CH3 - CH - СОOH CH2 - CH - СООН
CH2 - CH - СООН


