
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Размер, состав и заряд атомного ядра. Массовое и зарядовое числоСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте Атомное ядро было открыто английским физиком Э. Резерфордом в 1911 году в опытах по рассеянию α-частиц при прохождении их через вещество. Схема этого опыта была приведена нами в первой лекции (см. рис. 1.1), там же было дано его краткое описание. Опыт Резерфорда послужил нам в первой лекции отправной точкой для обсуждения планетарной модели атома и проблемы нестабильности атома в этой модели. Теперь же нас будет интересовать само ядро. Ядро - центральная массивная часть атома, состоящая из протонов и нейтронов. В ядре сосредоточена почти вся масса атома (более 99,95%). Размеры ядер порядка 10-15÷10-14 м. Ядра имеют положительный заряд, кратный элементарному заряду е:
Целое число Z называется зарядовым числом. Оно совпадает с порядковым номером элемента в периодической системе элементов (см. лекцию 9, § 2). Ядро состоит из протонов и нейтронов (ниже мы уточним это утверждение). Термин "протон" (от греческого protos - первый) был введен Резерфордом в начале 20-х годов. Протон обозначают символом "р", он имеет следующие характеристики. Протон - одна из двух стабильных элементарных частиц (другой стабильной частицей является электрон). Масса протона:
здесь mе - масса электрона. В ядерной физике и в физике элементарных частиц массы принято выражать в единицах энергии, умножая их значение в системе СИ, на квадрат скорости света с2, в соответствии с релятивистской формулой, связывающей массу частицы с ее энергией покоя (см. Ч.1, (12.7)): W0 = m с2. Так масса частицы, равная 1 МэВ (точнее - 1 Мэв/с2) в системе СИ будет равна:
Выраженная в МэВ масса электрона равна:
Заряд протона - равен элементарному:
Протон имеет спин s = 1/2 и, следовательно, подчиняется принципу запрета Паули (см. лекцию 9, § 1). Протон обладает собственным магнитным моментом:
здесь
-единица измерения магнитного момента, называемая ядерным магнетоном. (Сравните с магнетоном Бора, введенным в части 2 формулой (13.19), там в формуле, аналогичной (16.7) на месте mр стояла масса электрона mе, значит ядерный магнетон в 1836 раз (см. (16.2)) меньше магнетона Бора). Магнитный момент протона примерно в 660 раз меньше магнитного момента электрона. Нейтрон был открыт в 1932 году английским физиком Д. Чедвиком - учеником Резерфорда. Обозначение нейтрона - символ "n". Электрический заряд нейтрона равен нулю. Масса нейтрона:
Так как масса нейтрона больше массы протона, то он нестабилен и распадается в свободном состоянии по схеме:
здесь
Время, за которое распадается половина первоначального количества нейтронов (период полураспада) Т1/2 ≈ 12 минут. Нейтрон, как и протон, имеет спин s=1/2 и поэтому подчиняется принципу запрета Паули. Несмотря на свою электрическую нейтральность, нейтрон обладает собственным магнитным моментом:
Знак "-" указывает на то, что магнитный момент направлен против механического (спинового). Уже этот факт говорит о наличии внутренней структуры у нейтрона. Отношения магнитного момента протона к магнитному моменту нейтрона с большой точностью равно 3/2. Объяснение этому было дано на основе представления о кварковой структуре протона и нейтрона. Протонно-нейтронная модель атомного ядра была предложена в 1932 г. советским физиком Д. Иваненко после открытия нейтрона. Затем эта модель была развита немецким физиком В. Гейзенбергом. Протоны и нейтроны получили общее название нуклонов, т.е. ядерных части. Отметим, что в ядре нейтрон является стабильной частицей. Общее число нуклонов в ядре означается буквой А и называется массовым числом ядра. Число нейтронов в ядре обозначают буквой N. Если учесть, что число протонов в ядре (зарядовое число) обозначается буквой Z, то для числа нейтронов имеем:
По современным представлениям протоны и нейтроны состоят из кварков и глюонов и атомное ядро - сложная система, состоящая из большого количества кварков, глюонных и мезонных полей, взаимодействующих друг с другом. Задача последовательного теоретического описания атомного ядра ставится в рамках квантовой хромодинамики. Однако в силу своей сложности эта задача пока не решена. При описании атомного ядра и ядерных реакций, происходящих при небольших энергиях (≤ 1 ГэВ на нуклон) можно с хорошей точностью считать, что ядро состоит из вполне определенного числа нуклонов, движущихся с нерелятивистскими скоростями (v2/c2~0,1). Размер ядра довольно точно определяется формулой:
здесь Ф - ферми - единица длины в ядерной физике, равная 10-15 м. Для обозначения ядер применяют следующий символ:
здесь Х - химический символ данного элемента в таблице Менделеева, А - массовое число, Z - зарядовое число. Ядра с одинаковыми Z, но разными А называются изотопами. Химические свойства элементов определяются валентными электронами. У протонов числа электронов одинаковы, значит по своим химическим свойствам атомы протонов совершенно одинаковы. Большинство химических элементов имеет по нескольку стабильных протонов. Например, у водорода три изотопа:
Обычный водород и дейтерий стабильны, тритий - радиоактивен, его период полураспада Т1/2=12,35 года.
|
||
|
Последнее изменение этой страницы: 2016-04-19; просмотров: 2203; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.214 (0.01 с.) |










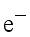 - обозначение электрона,
- обозначение электрона,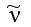 - символ, обозначающий антинейтрино.
- символ, обозначающий антинейтрино.







