
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Работа № 27. измерение скорости гидратации уксусного ангидрида методом кондуктометрииСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Цель работы – использование метода кондуктометрии в кинетических исследованиях. Определение средней константы скорости реакции и её энергии активации.
Гидратация уксусного ангидрида протекает по уравнению (СH3СО)2O + Н2О →2CH3COOН. Эта реакция бимолекулярная, но в разбавленных растворах, когда концентрация воды велика и практически не меняется, она протекает как реакция первого порядка. Для измерения скорости этой реакции проводят измерение электропроводности раствора, которая пропорциональна концентрации уксусной кислоты и в ходе реакции значительно возрастает вследствие образования последней. Измерения электропроводности проводят с помощью реохордного моста или кондуктометра. Правила пользования прилагаются к самим приборам.
Порядок выполнения работы
1. Налить в сосуд для измерения электропроводности 15 мл дистиллированной воды и 2-3 мл уксусного ангидрида. Осторожно, не задевая электродов, перемешать содержимое сосуда стеклянной палочкой, закрыть сосуд крышкой и поместить в термостат с заданной температурой. 2. Провести измерения либо электрического сопротивления раствора с помощью реохордного моста, либо электропроводности с помощью кондуктометра. Измерения начинать не позднее, чем через 1-1,5 мин. от начала реакции. За начало реакции принять момент смешения ангидрида с водой. Произвести два-три измерения через 30 с, три-четыре измерения через 1 мин., два-три измерения через 5 мин. и два измерения через 10 мин. Постоянство сопротивления раствора или электропроводности указывает на конец реакции. 3. Записать результаты измерений в таблицу:
4. Построить график зависимости 5. Рассчитать константу скорости для трех-четырех измерений времени τ при установившемся режиме (в середине процесса) по кинетическому уравнению первого порядка. Учитывая, что увеличение электропроводности во времени пропорционально увеличению концентрации уксусной кислоты, а количество кислоты пропорционально количеству введенного в раствор уксусного ангидрида, можно считать, что наибольшая электропроводность, а следовательно и наименьшее сопротивление будет пропорционально начальной концентрации уксусного ангидрида. Тогда где R0 − сопротивление раствора в момент начала реакции; Rτ − сопротивление в момент времени τ от начала реакции; R∞ − сопротивление, соответствующее последнему измерению. Величина R0 экспериментально не определяется, так как от начала реакции до первого измерения проходит некоторое время. Поэтому 6. Вычислить среднее значение константы скорости. 7. Определить константу скорости по графику как тангенс угла наклона прямой к оси абсцисс. 8. Сравнить константу, найденную графически с вычисленной. 9. Вычислить величину энергии активации данной реакции, зная, что при 0°C k = 0,027.
|
|||||||||||
|
Последнее изменение этой страницы: 2021-03-09; просмотров: 473; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.119.124.24 (0.006 с.) |

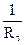
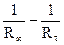
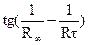
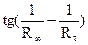 = f(τ),откладывая время в минутах на оси абсцисс. Для реакции первого порядка эта зависимость выражается прямой.
= f(τ),откладывая время в минутах на оси абсцисс. Для реакции первого порядка эта зависимость выражается прямой.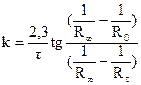 ,
,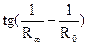 находят экстраполяцией, продолжив полученную прямую на графике до значения τ = 0.
находят экстраполяцией, продолжив полученную прямую на графике до значения τ = 0.


