
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
I. Реакції по карбонільній групіСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
1. ОКИСНЕННЯ (для альдегідів) – призводить до утворення відповідних кислот. a)реакція "срібного дзеркала":
б) реакція "мідного дзеркала":
в) реакція з концентрованою азотною кислотою:
2. ВІДНОВЛЕННЯ – призводить до утворення багатоатомних спиртів. Як відновник використовують водень
II. Реакції по гідроксильних групах (здійснюються, як правило, в напівацетальній (циклічної) формі). 1. АЛКІЛУВАННЯ (утворення простих ефірів) -атом водню гликозидного гідроксилу заміщується на 1 метильну групу.
При використанні більш сильних алкілуючих засобів (йодний метил СH3I), подібне перетворення зачіпає ВСІ гідроксильні групи моносахариду.
2. АЦИЛЮВАННЯ (утворення складних ефірів). При дії на глюкозу оцтового ангідриду утворюється складний ефір – пентаацетилглюкоза.
3. Як і всі багатоатомні спирти, глюкоза з гідроксидом міді (II) дає інтенсивне синє забарвлення (ЯКІСНА РЕАКЦІЯ). III. Специфічні реакції БРОДІННЯ - процес розщеплення молекул цукрів під впливом ферментів (ензимів). Бродінню піддаються цукру з числом вуглецевих атомів, кратним трьом. Існує багато видів бродіння, серед яких найбільш відомі наступні:
a) спиртове бродіння C6H12O6 →2CH3–CH2OH (етиловий спирт) + 2CO2
Згадані види бродіння, що викликаються мікроорганізмами, мають широке практичне значення. Наприклад, спиртове – для отримання етилового спирту, у виноробстві, пивоварінні і т.д., а молочнокисле – для отримання молочної кислоти і кисломолочних продуктів. Застосування Енергія для біохімічних перетворень в живих організмах. Добування: етанолу, молочної кислоти, сорбіту. У кондитерській промисловості. У медицині для лікування дистрофій. Лекція № 16. ДИСАХАРИДИ. ЇХ БУДОВА ТА ВЛАСТИВОСТІ
Класифікація і номенклатура
Дисахариди ділятся на дві групи:
þ До НЕВІДНОВНИХдисахаридів відноситься САХАРОЗА (буряковий або тростинний цукор). Вона міститься в цукровому очереті, цукровому буряці (до 28% від сухої речовини), соках рослин і плодах. Молекула сахарози побудована з а, D- глюкопіранозиі β, D- фруктофуранози.
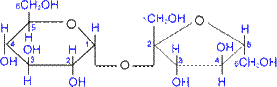
(САХАРОЗА: a,D- глюкопіранозил -(1>2) -b,D- фруктофуранозид) Для сахарози характерні реакції по гідроксильних групах. Як і всі дисахариди, сахароза при кислотному або ферментативному гідролізі перетворюється на моносахариди, з яких вони складаються. ВІДНОВНІ: 1) МАЛЬТОЗА (солодовий цукор) – міститься в солоді, тобто пророслих, а потім висушених і подрібнених зернах хлібних злаків. Утворюється при неповному гідролізі крохмалю.
(МАЛЬТОЗА: α,D- глюкопіраноза + α,D- глюкопіраноза) Мальтоза здатна вступати в реакції, характерні для альдегідів, і, зокрема, давати реакцію "срібного дзеркала", тому її називають ВІДНОВНИМдисахаридом. Крім того, мальтоза вступає в багато реакцій, характерних для моносахаридів, наприклад, утворює прості і складні ефіри (див. хімічні властивості моносахаридів).
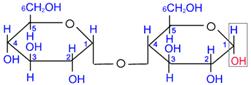
2) ЦЕЛОБІОЗА, утворюється при неповному гідролізі полісахариду целюлози.
(ЦЕЛОБІОЗА: b,D- глюкопіраноза + b,D- глюкопіраноза)
Целлобіоза, як і мальтоза складається з двох залишків D- глюкопіранози.
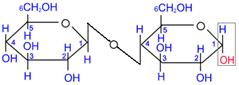
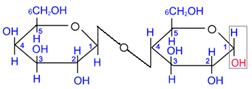
3) ЛАКТОЗА (молочний цукор) міститься в молоці (4-5%) і одержується з молочної сироватки. Лактоза побудована із залишків D- галактопіранози і D- глюкопіранози. Може мати як a- (a-лактоза) так і b-конфігурацію (b-лактоза).
(ЛАКТОЗА: b,D- галактопіраноза + a,D- глюкопіраноза) Застосування 1. Сахароза – основне джерело вуглеводнів у їжі людини. 2. Кондитерська промисловість. 3. Добувають штучний мед (продукт харчування). 4. Добування моносахаридів. 5. Утворення полісахаридів. 6. Сахарозу використовують для виготовлення деяких ліків та сиропів. ПОЛІСАХАРИДИ Загальна формула полісахаридів (C6H10O5)n. Найважливіші з полісахаридів – це КРОХМАЛЬ і ЦЕЛЮЛОЗА (клітковина). Вони побудовані із залишків ГЛЮКОЗИ. КРОХМАЛЬ Будова молекули (розгалужений ланцюг)
Фізичні властивості Крохмаль – це аморфний білий порошок, що складається з дрібних зерен, не розчинний в холодній воді. Хімічні властивості Крохмаль легко піддається гідролізу: при нагріванні у присутності сульфатної кислоти утворюється глюкоза. (C6H10O5)n(крохмаль) + nH2O ––H2SO4,t→ nC6H12O6(глюкоза) Залежно від умов проведення реакції гідроліз може здійснюватися ступенево з утворенням проміжних продуктів. (C6H10O5)n(крохмаль)→ (C6H10O5)m(декстрини (m<n))→ xC12H22O11(мальтоза)→ nC6H12O6(глюкоза)
þЯкісною реакцією на крохмаль є його взаємодія з йодом – спостерігається інтенсивне синє забарвлення. Таке забарвлення з'являється, якщо на зріз картоплі або скибочку білого хліба помістити краплю розчину йоду. L Крохмаль не вступає в реакцію "срібного дзеркала".
Знаходження в природі Крохмаль утворюється в рослинах при фотосинтезі і відкладається у вигляді "резервного" вуглеводу в корінні, бульбах і насінні. Наприклад, зерна рису, пшениці і інших злаків містять 60-80% крохмалю, картопля – 15-20%. Споріднену роль в тваринному світі виконує полісахарид глікоген, що "запасається", в основному, в печінці. Крохмаль є цінним харчовим продуктом. Для полегшення його засвоєння продукти, що містять крохмаль, піддають термообробці, тобто картоплю і крупи варять, хліб печуть.
Застосування У харчовій промисловості крохмаль використовується при виробництві ковбасних, кондитерських і кулінарних виробів. Застосовується також для отримання глюкози, при виготовленні паперу, текстильних виробів, клеїв, лікарських засобів і т.д. ЦЕЛЮЛОЗА (КЛІТКОВИНА) Будова молекули (лінійний ланцюг)
Як і у крохмалю, структурною одиницею целюлози є D- глюкопіраноза. Проте, від крохмалю целюлоза відрізняється β-конфігурацією глікозидних зв'язків між циклами і строго лінійною будовою.
Фізичні властивості Тверда волокниста речовина, нерозчинна у воді, нерозчинна у органічних сполуках. Хімічні властивості 1. Реакції етерифікації (утворення складних ефірів). Найбільше практичне значення мають реакції з азотною кислотою і оцтовим ангідридом.
Піроксилін після відповідної обробки перетворюється на бездимний порох. Залежно від умов нітрування можна одержати динітрат целюлози, він так само використовується при виготовленні пороху і твердих ракетних палив, на його основі виготовляють целулоїд. При взаємодії целюлози з оцтовим ангідридом у присутності оцтової і сірчаної кислот утворюється триацетилцелюлоза.
Триацетілцелюлоза (або ацетилцелюлоза) є цінним продуктом для виготовлення негорючої кіноплівки і ацетатного шовку.
2. Як і крохмаль, целюлоза при кислотному гідролізі дає глюкозу. (C6H10O5)n (целюлоза) + nH2O ––H2SO4,t→ nC6H12O6 (глюкоза) R Целюлоза не дає реакції "срібного дзеркала". Знаходження в природі ЦЕЛЮЛОЗА – найпоширеніший рослинний полісахарид. Вона має велику механічну міцність. Деревина містить 50-70% целюлози, бавовна є майже чистою целюлозою. β-Глікозидний зв'язок не руйнується травними ферментами людини, тому целюлоза не може служити їжею (!), хоча в певній кількості є необхідною для нормального харчування речовиною. В шлунках жуйних тварин є ферменти, що розщеплюють целюлозу, тому такі тваринні використовують клітковину як компонент їжі.
Застосування 1. Продукт горіння, енергія. 2. Як будівельний матеріал, виготовлення меблів. 3. Виробництво тканин (штучного шовку). 4. Добування деревного вугілля, метанолу, ацетону. 5. Добування тринітроцелюлози, з якої виготовляють вибухові речовини. 6. Виготовлення паперу. Заняття № 26
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-23; просмотров: 472; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.22.70.169 (0.012 с.) |

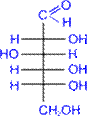 D- глюкоза
D- глюкоза
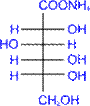 аммонієва сіль D- глюконової кислоти
аммонієва сіль D- глюконової кислоти
 D- галактоза
D- галактоза
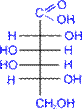 D- галактонова кислота
D- галактонова кислота
 D- глюкоза
D- глюкоза
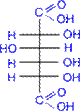 цукрова
(D- глюкарова) кислота
цукрова
(D- глюкарова) кислота
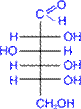 D- глюкоза
D- глюкоза
 D- сорбіт
D- сорбіт
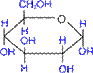 α, D- глюкопіраноза
α, D- глюкопіраноза
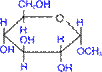 метил- α,D- глюкопіранозид
метил- α,D- глюкопіранозид

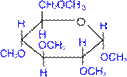 пентаметил- α, D- глюкопіраноза
пентаметил- α, D- глюкопіраноза

 ––––––→
––––––→
 пентаацетил- α,D- глюкопіраноза
пентаацетил- α,D- глюкопіраноза



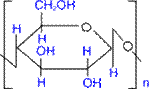
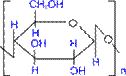 целюлоза
целюлоза
 тринітрат целюлози
ПІРОКСИЛІН
тринітрат целюлози
ПІРОКСИЛІН
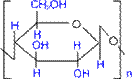

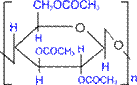 триацетилцелюлоза
триацетилцелюлоза



