Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Случай из практики: дыхательная недостаточность в палате пробужденияСодержание книги
Поиск на нашем сайте
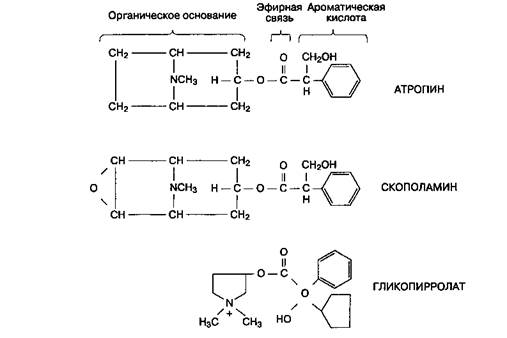
Женщина, 66 лет, с массой тела 85 кг поступила в палату пробуждения после холецистэктомии. Во время анестезии применяли изофлюран и пан-куроний. По завершении операции анестезиолог ввел 6мг морфина сульфата для предотвращения послеоперационной боли, а также 3 мг неостигми-на с 0,6 мг гликопирролата для устранения остаточной миорелаксации. Доза ингибитора ацетилхолинэстеразы была выбрана эмпирически, на основе клинических наблюдений. Хотя в момент поступления в палату пробуждения дыхание у больной было адекватным, постепенно дыхательный объем стал прогрессивно снижаться. При анализе газов артериальной крови (FiO2 40 %) получены следующие данные: PaCO2 62 мм рт. ст., PaO2 110 мм рт. ст., рН 7,26. Какие из примененных лекарственных средств могли вызвать гиповентиляцию? Изофлюран, морфина сульфат и панкуроний — все эти препараты угнетают реакцию вентиляции на гиперкапнию. Почему дыхательная недостаточность возникла только в палате пробуждения? Это могло произойти из-за отсроченного действия морфина сульфата, отсутствия сенсорной стимуляции в палате пробуждения, усталости дыхательной мускулатуры, а также при невозможности глубокого вдоха вследствие боли в области операционной раны. Могла ли у больной сохраняться остаточная миорелаксация? Если перед назначением неостигмина не проводили стимуляцию периферического нерва или недостаточно внимательно оценивали восстановление нервно-мышечной проводимости уже после введения препарата, то риск остаточной миорелаксации достаточно высок. Предположим, что при тетани-ческой стимуляции с частотой 100 Гц не получено мышечного ответа или же он чрезвычайно слаб. В этом случае даже максимальная доза неостигмина (5 мг) не приведет к восстановлению нервно-мышечной проводимости. Чувствительность к миорелаксантам средней продолжительности действия и длительного действия чрезвычайно варьируется, поэтому при их использовании обязательно проводят мониторинг нервно-мышечной проводимости с помощью стимуляции периферического нерва. Даже если нервно-мышечная проводимость частично восстановилась, гиповентиля-ция может потенцировать миорелаксацию. К прочим факторам (помимо респираторного ацидоза), которые препятствуют устранению эффекта недеполяризующих миорелаксантов, относят: глубокий нервно-мышечный блок, электролитные расстройства (гипомагниемия, гипокалиемия и гипо-кальциемия), гипотермию (температура < 32 0C), некоторые лекарственные средства (см. табл. 9-4), метаболический алкалоз (вследствие сопутствующей гипокалиемии и гипокальциемии) и ряд сопутствующих заболеваний (см. табл. 9-7). Как проверить степень устранения нервно-мышечного блока? Тетаническая стимуляция — чувствительный метод оценки нервно-мышечной проводимости, но он вызывает дискомфорт у бодрствующего больного. Такой больной легче перенесет стимуляцию в режиме двойной вспышки благодаря ее кратковременности. Многие клинические тесты нервно-мышечной проводимости, такие как определение жизненной емкости легких и дыхательного объема, имеют низкую чувствительность: они могут быть успешно выполнены, даже если блокировано 70-80 % н-холинорецепторов скелетных мышц. Кроме того, 70 % рецепторов могут оставаться блокированными при нормальном мышечном ответе на стимуляцию в TOF-режиме. Однако если больной способен удерживать приподнятую голову в течение 5 с, то блокировано менее 33 % рецепторов. Какое лечение следует назначить? Во избежание респираторного ацидоза проводят вспомогательную вентиляцию. Даже если экскурсии диафрагмы кажутся адекватными, остаточная миорелаксация может вызвать нарушение проходимости дыхательных путей. Необходимо ввести дополнительную дозу неостигмина (вместе с м-хо-линоблокатором). Общая доза при этом должна составить 5 мг. Если эти меры не приведут к успеху, то следует перевести больную на ИВЛ через эндотрахеальную трубку. ИВЛ выполняют до тех пор, пока полностью не восстановится нервно-мышечная проводимость. Избранная литература Bevan D. R., Donati F., Kofman A. F. Reversal of neuromuscular blockade. Anesthesiology, 1992; 77: 785. В этой статье представлены современные методы оценки нервно-мышечной проводимости, фармакология ингибиторов ацетилхолинэстеразы, а также клинические состояния, которые влияют на устранение нервно-мышечного блока. Connely R. Muscle relaxant antagonists. Chapter 13. In: Muscle Relaxants: Basic and Clinical Aspects. Katz R. L. (ed.). Grune & Stratton, 1985. Глава содержит ответы на многие вопросы, касающиеся устранения действия недеполяризующих миорелаксантов. Pappano A. J., Watanabe A. M. Cholinoreceptor-activating & cholinesterase-inhibiting drugs. Chapter 7. In: Basic & Clinical Pharmacology, 5th ed. Katzung B. G. (ed.) Appleton & Lange, 1994. Stocking R. K. Pharmacology and Physiology in Anesthetic Practice, 2nd ed. Lippincott, 1991. Современный взгляд на ингибиторы ацетилхолинэстеразы. Taylor P. Anticholinesterase agents. Chapter 7., In: The Pharmacological Basis of Therapeutics, 8th ed. Gilman A. G. et al. (eds). Pergamon, 1990. Хороший источник информации, позволяющий разобраться во взаимоотношении между структурой и активностью ингибиторов ацетилхолинэстеразы, а также в их клиническом применении. Глава 11 М-холиноблокаторы Ранее были рассмотрены недеполяризующие миорелаксанты, которые блокируют главным образом никотиночувствительные холинорецепторы (н-хо-линорецепторы) скелетных мышц. Эта глава посвящена фармакологии веществ, которые блокируют мускариночувствительные холинорецепторы (m-холинорецепторы). Хотя по умолчанию под холи-ноблокаторами подразумевают именно препараты последней группы, все же предпочтительно использовать точный термин — "м-холиноблокаторы". В данной главе описан механизм действия и клиническая фармакология трех наиболее распространенных м-холиноблокаторов: атропина, скопол-амина и гликопирролата. Для анестезиолога важно знание действия этих препаратов на системы кровообращения, дыхания, ЦНС и ЖКТ (табл. 11-1). Механизм действия М-холиноблокаторы представляют собой сложные эфиры органического основания и ароматической кислоты (рис. 11-1). М-холиноблокаторы — конкурентные антагонисты ацетилхолина, благодаря эфирной связи в молекуле они эффективно связываются с м-холинорецепторами, препятствуя их активации. Блокада м-холинорецепторов устраняет клеточные эффекты ацетилхолина, опосредуемые вторичными мессенджерами, например циклическим гуанозинмонофосфатом (цГМФ). М-холино-рецепторы не представляют собой гомогенной группы (так, обнаружены м1- и м2-подтипы рецепторов), поэтому их чувствительность к действию м-холиноблокаторов в разных тканях варьируется. Клиническая фармакология Основные сведения При введении в обычных дозах описанные ниже м-холиноблокаторы блокируют только м-холино-рецепторы. Степень блокады зависит от исходного тонуса блуждающего нерва. М-холиноблокаторы влияют на многие системы органов. А. Сердечно-сосудистая система. Блокада м-холинорецепторов синоатриального узла вызывает тахикардию, поэтому м-холиноблокаторы эффективно устраняют рефлекторную брадикардию при стимуляции блуждающего нерва (например, барорецепторный рефлекс, окулокардиальный рефлекс, раздражение брюшины). М-холиноблокаторы в низких дозах вызывают преходящее замедление сердечного ритма, потому что они не являются чистыми антагонистами и могут в незначительной степени стимулировать периферические м-холинорецепторы. М-холиноблокаторы облегчают проведение через атриовентрикулярный (AB) узел, что проявляется укорочением интервала P-R на ЭКГ и используется для лечения АВ-блокад на фоне повышенной активности блуждающего нерва, но иногда вызывает предсердные ТАБЛИЦА 11-1. Эффекты м-холиноблокаторов
Рис. 11-1. Структуры м-холиноблокаторов аритмии и узловые ритмы. М-холиноблокаторы очень незначительно влияют на функцию желудочков и тонус периферических сосудов, поскольку несмотря на достаточное количество холино-рецепторов эти области практически лишены прямой холинергической иннервации. В больших дозах м-холиноблокаторы вызывают расширение сосудов кожи (атропиновый прилив). Б. Система дыхания. М-холиноблокаторы ин-гибируют секрецию желез слизистой оболочки дыхательных путей от носа до бронхов; до появления мало раздражающих слизистую оболочку ингаляционных анестетиков этот эффект был особенно важен. М-холиноблокаторы расслабляют гладкие мышцы бронхов, что снижает сопротивление дыхательных путей и увеличивает анатомическое "мертвое пространство". Этот феномен наиболее выражен при наличии хронического обструктив-ного заболевания легких и бронхиальной астмы. В. Центральная нервная система. Различные м-холиноблокаторы в зависимости от дозы могут вызвать широкий спектр психических отклонений — от депрессии до стимуляции. Стимуляция проявляется психомоторным возбуждением, беспокойством и галлюцинациями, депрессия — седа-тивным эффектом и амнезией. Физостигмин, проникающее через гематоэнцефалический барьер антихолинэстеразное средство, устраняет действие м-холиноблокаторов на ЦНС. Г. Желудочно-кишечный тракт. М-холиноблокаторы подавляют секрецию слюнных желез. Они также ингибируют желудочную секрецию, но для этого требуются большие дозы препаратов. Снижая двигательную и перистальтическую активность ЖКТ, м-холиноблокаторы замедляют опорожнение желудка и снижают тонус нижнего пищеводного сфинктера. М-холиноблокаторы не имеют особых преимуществ перед другими средствами при использовании их с целью профилактики аспираци-онной пневмонии (см. "Случай из практики", гл. 15). Д. Глаза. М-холиноблокаторы вызывают мид-риаз (расширение зрачка) и циклоплегию (паралич аккомодации, глаз устанавливается на дальнюю точку видения); при системном применении острый приступ закрытоугольной глаукомы обычно не возникает. E. Мочеполовая система. М-холиноблокаторы снижают тонус гладких мышц мочеточников и мочевого пузыря, что может привести к задержке мочи, особенно у пожилых мужчин с гипертрофией предстательной железы. Ж. Терморегуляция. Подавление секреции потовых желез вызывает повышение температуры тела (атропиновая лихорадка). 3. Иммунологическая гиперчувствительность. Снижение внутриклеточного цГМФ создает теоретические предпосылки для применения м-холиноблокаторов для лечения реакций гиперчувстви- тельности (аллергии), но клинически эти препараты неэффективны. Отдельные м-холиноблокаторы Атропин Структура Атропин — это третичный амин, представляющий собой сложный эфир троповой кислоты (ароматическая кислота) и тропина (органическое основание). Активна натуральная левовращающая форма (L-форма), но на практике применяют синтетическую рацемическую смесь. Доза и форма выпуска Для премедикации атропин вводят в/м или в/в в дозе 0,01-0,02 мг/кг, обычная доза для взрослых составляет 0,4-0,6 мг. При лечении тяжелой бра-дикардии может потребоваться до 2 мг. В табл. 10-3 указаны дозы для уменьшения побочных эффектов антихолинэстеразных средств при устранении действия антидеполяризующих миорелаксантов. Атропина сульфат выпускают в растворах различной концентрации. Применение Атропин оказывает сильное влияние на сердце и гладкие мышцы бронхов, из всех м-холиноблокато-ров он наиболее эффективен для лечения бради-аритмий. При ИБС тахикардия, вызванная введением атропина, усугубляет ишемию миокарда из-за повышения потребности миокарда в кислороде и снижения доставки кислорода. Производное атропина, ипратропиум бромид, выпускаемое в форме дозированного аэрозоля для ингаляций, применяют для лечения бронхоспазма. Раствор ипратропиума для ингаляций (0,5 мг в 2,5 мл) особенно эффективен для лечения и профилактики приступов бронхоспазма при ХОЗЛ в сочетании с β-адреномиметиком (например, албутеролом). Несмотря на то что атропин (третичный амин) легко проникает через гематоэнцефалический барьер, в стандартных дозах он мало влияет на ЦНС. После применения атропина в послеоперационном периоде может наблюдаться легкая амнезия, а его передозировка чревата психомоторным возбуждением. В дозе 0,01-0,02 мг/кг внутримышечно атропин подавляет секрецию слюнных желез. При закрытоугольной глаукоме, гипертрофии предстательной железы и обструкции шейки мочевого пузыря атропин применяют с особой осторожностью. Скополамин Структура Скополамин отличается от атропина наличием дополнительного кислородного мостика в составе органического основания, которое называется скопином. Доза и форма выпуска Доза скополамина для премедикации идентична дозе атропина, препарат вводят в/м. Скополамина бромид выпускают в растворах, содержащих 0,3 мг, 0,4 мг и 1 мг в 1 мл. Применение Скополамин по сравнению с атропином сильнее подавляет секрецию слюнных желез и выраженнее действует на ЦНС. При использовании в клинических дозах обычно возникает сонливость и амнезия, хотя в некоторых случаях препарат вызывает беспокойство и делирий. Седативный эффект является дополнительным преимуществом для применения с целью премедикации, но при коротких операциях препарат затрудняет пробуждение. Скополамин используют также для профилактики укачивания в транспорте. Липофильность скополамина позволяет использовать его в виде трансдер-мальных лекарственных форм. Скополамин значительно затрудняет отток жидкости из передней камеры глаза, поэтому его не следует применять при закрытоугольной глаукоме. Гликопирролат Структура Гликопирролат — это синтетическая четвертичная аммониевая соль, где место троповой кислоты занимает миндальная. Доза и форма выпуска Гликопирролат назначают в дозах, составляющих половину от дозы атропина. Например, для премедикации вводят 0,005-0,01 мг/кг, обычная доза для взрослых равна 0,2-0,3 мг. Гликопирролат для инъекций выпускают в виде раствора, содержащего 0,2 мг/мл. Применение Так как четвертичная аммониевая соль не проникает через гематоэнцефалический барьер, глико-пирролат практически не оказывает влияния на центральную нервную систему и глаза. Из всех м-холиноблокаторов гликопирролат является самым мощным ингибитором секреции слюнных желез и желез слизистой оболочки дыхательных путей. Тахикардия возникает при введении препарата в/в, но не в/м. Гликопирролат имеет большую продолжительность действия, чем атропин (2-4 ч и 30 мин после в/в инъекции соответственно).
|
|||||||||||||
|
Последнее изменение этой страницы: 2016-04-20; просмотров: 411; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.217.89 (0.013 с.) |