
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Мелкоузловой (портальный) цирроз печениСодержание книги
Поиск на нашем сайте
БОЛЕЗНЬ КРОНА Болезнь Крона (БК) — хроническое прогрессирующее гранулема-тозное воспаление кишечника. Чаще всего патологический процесс поражает тонкую кишку (в 45 % — поражается илеоцекальная область, в 30 % — ее проксимальный отдел), толстая кишка поражается реже — в 25 % случаев. В 5 % случаев болезнь может дебютировать с поражением пищевода или желудка, или двенадцатиперстной кишки, или перианальной области. Воспалительный процесс распространяется на всю толщу кишечной стенки и характеризуется наличием инфильтратов с изъязвлением слизистой оболочки, развитием абсцессов и свищей с последующим рубцевани- ем и сужением просвета кишки. Протяженность поражения пищеварительного тракта при Б К весьма различна: от 3 — 5 см до 1 ми более. Точные сведения о распространенности Б К среди населения отсутствуют. Отмечено, что Б К страдают чаще люди трудоспособного возраста (20 — 50 лет) обоего пола. Этиология.Причины развития болезни неизвестны. Предполагают этиологическую роль бактерий, вирусов, пищевых аллергенов, генетических факторов (семейный характер болезни отмечен в 5 % случаев). Отмечено, что БК ассоциируется с антигеном гистосовместимости HLA-B27- Патогенез.Точные представления о механизмах развития болезни отсутствуют. Отмечено, что кишечной микрофлоре принадлежит важная роль, так как при Б К выявляются значительные нарушения микробиоценоза кишечника. Характерно уменьшение количества бифидобактерий при одновременном увеличении числа энтеробактерий и появление энтеробактерий с признаками патогенности. Возможно, что в патогенезе имеют значение и аутоиммунные механизмы. Предполагают, что органами иммуногенеза вырабатываются аутоантитела к клеткам слизистой оболочки кишечника, а также сенсибилизированные лимфоциты, обладающие повреждающим действием. Воспалительный процесс при БК начинается в подслизистом слое и распространяется на все слои кишечной стенки. В подслизистом слое на фоне диффузной инфильтрации лимфоцитами и плазматическими клетками отмечается гиперплазия лимфоидных фолликулов, которые могут изъязвляться. Язвы при БК имеют удлиненную щелевидную форму и глубоко проникают в подслизистый и мышечные слои, образуя свищи и абсцессы. Наличие свищей, стриктур и кишечного стаза способствует развитию дис-бактериоза. Распространенное поражение тонкой кишки вызывает тяжелый синдром нарушения всасывания (мальабсорбция). Снижение всасывания железа, витамина В)2 и фолиевой кислоты вызывает анемию, чему способствуют и повторные кровопотери. Возникновение воспалительного процесса и изъязвлений в кишечнике приводит также к интоксикации, профузным поносам, потере массы тела, нарушениям электролитного обмена. Клиническая картина.Клинические проявления и характер течения заболевания определяются тяжестью морфологических изменений, анатомической локализацией и протяженностью патологического процесса, наличием осложнений и внекишечных поражений. К проявлению собственно кишечных поражений относят боль в животе, диарею, синдром недостаточного всасывания, поражения аноректаль-ной области (свищи, трещины, абсцессы), ректальные кровотечения (редко). К внекишечным признакам относят лихорадку, анемию, снижение массы тела, артрит, узловатую эритему, афтозный стоматит, поражения глаз (ирит, увеит, эписклерит), вторичную аменорею у женщин. Однако, несмотря на значительную вариабельность клинических проявлений при БК, в 90 % случаев доминируют боль в животе, диарея, снижение массы тела. На I этапе диагностического поиска, при наиболее часто встречающейся хронической форме БК, выявляется диарея, имеющая упорный характер. Частота стула достигает 4 — 6 раз (редко — до 10 раз), масса испражнений — более 200 г/сут, кал разжиженный или водянистый. Диарея возникает после каждого приема пищи, но может быть и ночью. Объем стула зависит от локализации патологического процесса в кишечнике: при поражении высоких отделов тонкой кишки объем кала оказывается большим, нежели при дистальной локализации воспалительного процесса. Тенезмы отмечаются лишь при вовлечении в процесс аноректальной области. Ректальные кровотечения, обычно необильные, отмечаются у половины больных. Боли в животе бывают практически у всех больных, они носят чаще тупой или схваткообразный характер (при поражении толстой кишки). Максимальная выраженность болей отмечается при вовлечении в процесс тонкой кишки. Причины болей разнообразны: а) вовлечение в патологический процесс брюшины; б) повышение давления в просвете кишки в результате повышенного газообразования и увеличения объема кишечного содержимого вследствие нарушения всасывания; в) наличие осложнений (частичная кишечная непроходимость, свищи, абсцессы). В период обострения отмечается лихорадка, сочетающаяся с общей слабостью и уменьшением массы тела. Температура тела может повышаться до 39 °С. В ряде случаев повышение температуры «опережает» местные кишечные симптомы, такая ситуация может продолжаться в течение длительного времени, что создает большие диагностические трудности. Другое частое внекишечное проявление болезни — артралгии в крупных суставах. Таким образом, при сборе анамнеза выявляются кишечные симптомы и системные (внекишечные) проявления. Эти признаки не позволяют еще сформулировать определенную диагностическую концепцию, однако направление диагностического поиска можно определить. Гораздо сложнее, когда в клинической картине доминируют «общие» признаки (лихорадка, уменьшение массы тела, артралгии, артрит). На II этапе диагностического поиска уточняются симптомы со стороны желудочно-кишечного тракта в виде болезненности при пальпации живота (преимущественно вокруг пупка), урчания, болезненного уплотнения терминального отдела подвздошной кишки, болезненности, урчания и «шума плеска» при пальпации слепой кишки. Отмечается уменьшение массы тела, особенно при длительном течении болезни. Снижение массы тела обусловлено прежде всего синдромом нарушенного всасывания. Синдром нарушенного всасывания имеет сложный патогенез и обусловлен рядом факторов: а) уменьшением всасывающей поверхности кишки из-за воспалительного процесса слизистой оболочки; 6) дефицитом кишечных ферментов (дисахаридазы, лактазы); в) снижением активности панкреатических ферментов; г) нарушением всасывания желчных кислот, что приводит к блокированию всасывания воды и электролитов. Кроме того, снижение массы тела связано с уменьшением приема пищи вследствие ано-рексии (особенно в период обострения болезни). В 25 % случаев можно обнаружить перианальные поражения: отек кожи вокруг анального сфинктера, трещины и изъязвления сфинктера, свищи и периректальные абсцессы. При этом наружные анальные поражения превалируют над поражением слизистой оболочки прямой кишки в отличие от неспецифического язвенного колита (НЯК), при котором эти соотношения обратные. При осмотре могут быть выявлены внекишечные проявления в виде артрита крупных суставов (дефигурация сустава), узловатой эритемы, поражения глаз. При тяжелом течении болезни и выраженном синдроме нарушенного всасывания отмечаются симптомы гиповитаминоза и дефицита железа: сухость кожи, выпадение волос, ломкость ногтей, хейлит, глоссит, кровоточивость десен. На III этапе диагностического поиска необходимо убедиться в характере и обширности поражения кишечника, а также оценить выраженность обменных расстройств и внекишечных поражений. Для постановки окончательного диагноза прежде всего необходимо сделать эндоскопию (колоноскопию), позволяющую осмотреть слизистую оболочку всей толстой кишки и терминального отдела подвздошной. Выявляется отечность слизистой оболочки, исчезновение сосудистого рисунка, небольшие афтозные язвы с последующим образованием глубоких ще-левидных трещин, изменяющих рельеф слизистой оболочки по типу «булыжной мостовой», возможно появление стриктур кишки. Биопсия слизистой оболочки кишки выявляет характерные морфологические изменения в виде гранулем туберкулоидного и саркоидного типов. Аналогичные изменения слизистой оболочки выявляются и при гастродуоденоскопии (в случаях поражения верхних отделов желудочно-кишечного тракта). Рентгенологическое исследование кишечника (ирригоскопия, энтеро-скопия) в выраженных случаях болезни демонстрирует сегментарность поражения кишечника с наличием неизмененных участков кишки между пораженными сегментами. В области поражения отмечают волнистый или неровный контур кишки, продольные язвы, образующие рельеф «булыжной мостовой», псевдодивертикулы (представляющие собой глубокие язвы, проникающие в результате фиброзных изменений в кишечной стенке — «симптом шнура»). Лабораторное исследование крови позволяет определить степень и характер анемии (железодефицитная, В^-дефицитная). Для рецидива болезни характерны повышение СОЭ, иногда достигающее значительных величин (50 — 60 мм/ч). Биохимическое исследование крови отражает нарушения белкового, жирового и электролитного обмена (гипоальбуминемия, гиполипидемия, гипогликемия, гипокальциемия), обусловленные выраженностью синдрома нарушенного всасывания. Для выявления нарушения всасывания используют также тест с D-ксилозой и витамином В12 (тест Шиллинга). Более детально на этих тестах мы останавливались при описании хронического энтерита. Анализ кала предусматривает микроскопию, химическое и бактериологическое исследование. Недостаточность переваривания и всасывания в тонкой кишке проявляется большим количеством мышечных волокон, значительным количеством жирных кислот и мыл; определяется небольшое количество соединительной ткани, нейтрального жира и йодофильной флоры. Степень изменений копрограммы обусловливается тяжестью болезни и ее фазой (ремиссия — обострение). При вовлечении в патологический процесс других органов системы пищеварения (печень, желчные пути, поджелудочная железа) лаборатор-но-инструментальным исследованием можно обнаружить соответствующие изменения. Осложнения.Большинство осложнений БК являются хирургической проблемой: кишечная непроходимость, перфорация кишки с развитием абсцессов и перитонита, кишечные кровотечения, формирование энтеро-энтеральных, кишечно-кожных, кишечно-пузырных и ректовагинальных свищей. Диагностика.Распознавание болезни в развитой форме при наличии типичных кишечных симптомов не представляет сложностей. Однако достаточно часто возникают ситуации, когда в течение длительного периода доминируют общие симптомы: лихорадка, снижение массы тела, признаки гиповитаминоза, неспецифические лабораторные показатели при отсутствии местных кишечных признаков. Это существенно затрудняет своевременную диагностику, заставляя врача предполагать совершенно иное заболевание. Во всяком случае в круг диагностического поиска при Б К включается большое количество заболеваний, имеющих сходные черты с БК. Прежде всего в круг диагностического поиска включаются злокачественные образования, хронические инфекции, системные заболевания (диффузные заболевания соединительной ткани). Несмотря на совершенство методов исследования, диагноз Б К ставится спустя 1 — 2 года после появления первых симптомов. Если доминируют «кишечные» симптомы, то диагноз можно поставить значительно раньше. При наличии «кишечных» симптомов дифференциальная диагностика проводится с кишечными инфекциями (дизентерия, сальмонеллез), неспецифическим язвенным колитом (НЯК), хроническим неязвенным колитом, хроническим энтеритом, раком толстой кишки. Бактериологическое и эндоскопическое исследование (в сочетании с клиническими признаками) позволяет поставить точный диагноз. Во всяком случае при наличии «кишечных» симптомов у больного Б К должна включаться в круг диагностического поиска. Формулировка развернутого клинического диагнозастроится по следующей схеме: 1) клиническая форма (с учетом преимущественного поражения тех или иных отделов желудочно-кишечного тракта); 2) степень тяжести поражения кишечника (с учетом данных эндоскопии); 3) фаза заболевания (ремиссия — обострение); 4) внекишечные поражения; 5) осложнения. Лечение.При лечении БК следует учитывать локализацию процесса, активность и продолжительность заболевания, возраст и общее состояние больного. Диета, приближаясь к нормальной, не должна содержать плохо переносимые продукты. При поражении тонкой кишки с наличием стеатореи и непереносимости жиров рекомендуется диета с высоким содержанием белка и ограничением жира, лактулезы и грубоволокнистых продуктов. Этиологическая терапия Б К невозможна, так как этиология и патогенез болезни неизвестны. Тем не менее к препаратам первого ряда относятся сульфасалазин, глюкокортикоиды и метронидазол. Сульфасалазин назначают при умеренной активности процесса по 0,5—1 г/сут, а затем по 2 — 4 г/сут в течение 6 — 8 нед с постепенным переходом на поддерживающую дозу (половина лечебной), которая сохраняется не менее 1 года. Препарат принимают вместе с пищей, что предупреждает раздражение желудка. В тяжелых случаях Б К используют глюкокортикоидные препараты — внутрь преднизолон по 40 — 8- мг/сут на протяжении 4 — 8 нед с последующим снижением дозы (по 5 мг каждую неделю). Поддерживающая доза может составлять 5— 10 мг в течение 6 мес и более. При перианальных поражениях и свищах назначают метронидазол (0,75-2 г/сут). При диарее назначают антидиарейные препараты (имодиум, реасек), ферментные препараты. Гипоальбуминемия корригируется введением плазмы, растворов альбумина и аминокислот, при электролитных нарушениях вводят растворы калия, кальция. По достижении ремиссии лекарственное лечение прекращают. Проводится заместительная терапия, включающая витамины Вп, фолиевую кислоту, микроэлементы. Антидиарейные препараты (имодиум, реасек) назначают при необходимости. Продолжительность ремиссии БК различна, в среднем она составляет 2 года (и не зависит от методов предшествующей терапии). Прогноз.Зависит от распространенности поражения, выраженности синдрома нарушенного всасывания и осложнений. Комплексная терапия может существенно смягчить проявления болезни, однако длительная ремиссия обычно не наступает. Хирургические вмешательства при патологии аноректальной области улучшают состояние больных. Профилактика.Специфических методов профилактики не существует. Профилактика сводится к предупреждению обострений, что достигается упорным лечением. Больных ставят на диспансерный учет, чтобы своевременно выявить начинающееся обострение или осложнение. ХРОНИЧЕСКИЙ ГЕПАТИТ Хронический гепатит — диффузное воспалительно-дистрофическое хроническое поражение печени различной этиологии, характеризующееся (морфологически) дистрофией печеночных клеток, гистиолимфо-плазмоцитарной инфильтрацией и умеренным фиброзом портальных трактов, гиперплазией звездчатых ретикулоэндотелиоцитов при сохранении дольковой структуры печени. Согласно Международной классификации болезней, термин «хронический гепатит» обозначает диффузный воспалительный процесс в печени, продолжающийся более б мес. Хронический гепатит может быть самостоятельным в нозологическом отношении заболеванием, а также быть частью какого-либо другого заболевания, например системной красной волчанки (в этом случае его рассматривают как синдром). Следует разграничить хронический гепатит от неспецифического реактивного гепатита, являющегося синдромом различных патологических процессов, в первую очередь поражений желудочно-кишечного тракта. Течение неспецифического реактивного гепатита зависит от основного заболевания. Хронический гепатит является распространенным заболеванием, им страдают люди обоего пола и самого различного возраста, однако отмечают большую его частоту у лиц пожилого и старческого возраста (это связывают с возрастным ослаблением иммунных реакций, что имеет отношение к механизмам развития патологического процесса в печени). Классификация. Внастоящее время общепринятой классификации хронических гепатитов нет. Предложения Международной группы экспертов, высказанные на Всемирном конгрессе гастроэнтерологов в Лос-Анджелесе (1994), не являются общепринятыми, а некоторые их положения в настоящее время невозможно использовать в практической деятельности врача. Классификация хронических гепатитов, предложенная в 1993 г. С. Д. Подымовой, представлена в несколько сокращенном и упрощенном виде. Этиологическая: 1. Вирусный. 2. Лекарственный. 3. Токсический. 4. Алкогольный. 5. Генетически детерминированный. Морфологическая: 1. Агрессивный. 2. Персистирующий. 3. Лобулярный. 4. Холестатический. Клиническая: 1. Хронический активный вирусный гепатит. 2. Аутоиммунный. 3. Персистирующий. 4. Лобулярный. /7о активности процесса: 1. Активный (степень активности незначительная, умеренная, выра 2. Неактивный. Ло функциональному состоянию печени: 1. Компенсированный. 2. Декомпенсированный. Этиология. Из классификации вытекает чрезвычайное разнообразие этиологических факторов, приводящих к развитию болезни. Основную массу хронических гепатитов составляют заболевания вирусной этиологии. Наиболее частой причиной их развития считается пер-систенция вируса В (HBV) самостоятельно или в сочетании с вирусом гепатита дельта (HDV), а также вируса гепатита С (HCV). Для этих вирусов характерны одинаковые пути распространения (главным образом парентеральный) и длительная персистенция в организме. Вирусы гепатита A (HAV) и Е (HEV) имеют орально-фекальный механизм передачи, не могут длительно персистировать в организме и поэтому практически не являются причиной хронических гепатитов (после перенесенного вирусного гепатита А хронический гепатит формируется в 1-2 % случаев). В рамках инфицирования HBV возможно развитие всех видов хронического гепатита — хронического персистирующего гепатита (ХПГ), хронического лобулярного гепатита (ХЛГ), хронического активного гепатита (ХАГ). У 40-50 % больных ХПГ, у 70-80 % больных ХЛГ и у 35 % больных ХАГ заболевание начинается с типичной картины острого вирусного гепатита. Не исключается роль вирусов и в развитии хронического аутоиммунного гепатита (HBV, HCV, HDV, вируса Эпштейна — Барр и вируса простого герпеса). Несмотря на то что этиология хронического аутоиммунного гепатита (ХАИГ) до сих пор не является точно установленной, в его развитии су- щественная роль принадлежит генетической предрасположенности к нарушениям функционирования иммунной системы. Возможны следующие исходы взаимодействия вируса и иммунной системы: а) отсутствие иммунной реакции на возбудитель и хроническое бес б) острый некроз гепатоцитов; в) полная элиминация вируса и выздоровление; г) недостаточная иммунная реакция (неполная элиминация вируса) и Среди других причин выделяют: 1. Хронические производственные интоксикации: а) хлорированными углеводородами (широко применяются в ма- б) хлорированными нафталинами и дифенилами (применяются для в) бензолом, его гомологами и производными (применяются для г) металлами и металлоидами (свинец, ртуть, золото, марганец, 2. Лекарственные поражения печени: а) прямого гепатотоксического действия (антибиотики, антиметабо б) токсико-аллергического действия (психотропные средства, про Чаще всего поражения печени развиваются на фоне лечения несколькими препаратами или при повторном курсе и не всегда зависят от длительности приема лекарственных средств. 3. Алкоголь (помимо жировой дистрофии печени, вызывает алкоголь Патогенез.Хроническое течение и прогрессирование патологического процесса в печени в настоящее время объясняют: 1) длительным сохранением вируса в организме больного; 2) развитием аутоиммунных процессов. Возбудитель хронического гепатита HBV — крупный ДНК-содержа-щий вирус. На наружной его поверхности находится поверхностный антиген — HBsAg; ядерными антигенами являются HBcAg и HBeAg. Ядро вируса содержит ДНК HBV (HBV-DNA) и ДНК-полимеразу (DNA-P). Все эти вирусные компоненты и антитела к его антигенам являются специфическими маркерами данной инфекции. В своем развитии HBV проходит две фазы: фазу репликации и фазу интеграции. В фазу репликации геномы вируса и клетки автономны (в эту фазу возможна полная элиминация вируса из организма). Повреждение гепатоцитов обусловлено не самим вирусом, а иммунекомпетентными клетками, распознающими его антигены. HBcAg и HBeAg обладают сильными иммуногенными свойствами, a HBsAg — слабыми иммуногенными свойствами. В фазу репликации HBV, когда синтезируются HBcAg и HBeAg, сила иммунных реакций достаточно высока, в результате чего не-кротизируются гепатоциты. В фазу интеграции HBV происходит встраивание генома вируса в область клеточного генома (элиминация вируса в эту фазу невозможна). В большинстве случаев формируется состояние иммунологической толерантности к HBsAg, что приводит к купированию активности процесса (в ряде случаев может происходить регресс хронического гепатита вплоть до формирования «здорового» носительства HBsAg). При инфицировании HBV характер поражения печени и хронизация процесса зависят от иммунного ответа, который во многом генетически детерминирован. Длительное сохранение (персистирование) вируса в организме больного объясняется недостаточной силой иммунной реакции в ответ на появление антигенов вируса в организме. Вероятно, имеется недостаточная продукция противовирусных антител. Даже отсутствие антител к HCV в ряде случаев не исключает диагноз хронического гепатита, вызванного вирусом С. В целом антитела к HCV образуются медленно, что занимает в среднем 20 нед от момента инфицирования. У некоторых больных для образования антител требуется около года. Кроме того, вирус, повреждая мембрану гепатоцита, высвобождает мембранный липопротеид, входящий в структуру специфического печеночного антигена. Этот антиген, воздействуя на Т-лимфоциты, приводит к образованию «агрессивных» форм этих клеток. Однако эти клетки функционально неполноценны, и «атака» ими гепатоцитов, ставших для организма чужеродными (вследствие воздействия на них вируса), хотя и приводит к гибели последних, но не обеспечивает полной элиминации вируса из организма. Аутоиммунные реакции развиваются вследствие того, что под воздействием самых различных патогенных факторов гепатоцит приобретает новые антигенные детерминанты (становится «аутоантигенным»), что обусловливает ответную реакцию иммунной системы в виде продукции ауто-антител. Имеющийся генетический дефект иммунной системы («слабость» Т-супрессоров) обусловливает неконтролируемую продукцию аутоанти-тел, реакция «антиген — антитело» на поверхности гепатоцитов вызывает их гибель; формирующиеся иммунные комплексы (вначале циркулирующие, а затем фиксированные в микроциркуляторном русле) обусловливают наряду с поражением гепатоцитов вовлечение в патологический процесс других органов и систем. Гуморальные и клеточные иммунные реакции и поражение гепатоцитов обусловливают морфологические признаки хронического гепатита — гистио-лимфоцитарную инфильтрацию портальных трактов, дистрофические и некротические изменения гепатоцитов и эпителия желчных ходов (схема 19). Нарушаются основные функции печени во всех видах обмена веществ, изменяется ее внешнесекреторная и дезинтоксикационная способ-
Схема 19. Патогенез хронического гепатита ность, формируются основные клинические печеночные синдромы, лежащие в основе проявления болезни. В зависимости от выраженности тех или иных морфологических проявлений (дистрофия и некроз гепатоцитов, или гистиолимфоцитарная инфильтрация портальных и перипорталь-ных трактов, или инфильтрация стенок желчных ходов с развитием некроза эпителия желчных ходов) формируется тот или иной (активный, персистирующий или холестатический) гепатит. При слабой реакции иммуноцитов на антигены гепатоцитов развивается персистирующий гепатит (ХПГ), а при сильном типе реакции — активный гепатит (ХАГ). В ряде случаев иммунный процесс приводит к повреждению эндоплаз-матического ретикулума гепатоцита, что проявляется нарушением образования желчных кислот из холестерина. Иммунные реакции могут нарушать проницаемость желчных капилляров и повышать вязкость желчи. Эти и другие факторы способствуют развитию внутрипеченочного холестаза. Развитие аутоиммунного процесса при антигенположительном гепатите связано с персистирующей реактивацией Т-лимфоцитов-хелперов вследствие неадекватной элиминации вируса гепатита из организма (в результате недостаточного синтеза антител к HBsAg). При всех вирусах гепатита (HBV, НВС и HBD) определяются аутоантитела. Кроме того, ус- тановлен факт репликации HBV и НВС вне гепатоцитов и вне ткани печени. Это может быть одним из объяснений многосистемности поражения при ХАГ и ХАИГ. При антигенотрицательном гепатите патологический процесс развивается на фоне нормального синтеза антител к поверхностному антигену, что приводит к адекватной элиминации вируса гепатита из организма, а заболевание все-таки прогрессирует. Более вероятно это объяснить генетически детерминированным дефектом супрессивной функции Т-лимфоцитов. Клиническая картина.Проявления болезни чрезвычайно разнообразны. Клиническая картина зависит от формы хронического гепатита (активный, аутоиммунный, персистирующий, лобулярный или холестатичес-кий), активности процесса, функционального состояния печени и определяется выраженностью основных клинических синдромов: 1) цитолити-ческого; 2) мезенхимально-воспалительного (иммуновоспалительного); 3) холестатического; 4) астеновегетативного; 5) диспепсического; 6) геморрагического; 7) синдрома гиперспленизма. • Цитолитический синдром (с признаками печеночно-клеточной не Клинические признаки — снижение массы тела; лихорадка; желтуха; геморрагический диатез; печеночный запах; внепеченочные знаки («печеночный» язык, «печеночные ладони», или пальмарная эритема, сосудистые звездочки, изменение ногтей, оволосения, гинекомастия и пр.). Лабораторные признаки: а) снижение в сыворотке крови уровня альбуминов, протромбина, холестерина, холинэстеразы, V, VII факторов свертывания крови; б) повышение в сыворотке крови содержания билирубина (связанного); в) изменения ферментных показателей сыворотки крови (повышение уровня ACT, АЛТ, ЛДГ, альдолазы, митохондриаль-ных — глутаматдегидрогеназы, сорбитдегидрогеназы — и лизосомальных ферментов — кислой фосфатазы, (3-глюкуронидазы); г) снижение захвата бромсульфалеина и бенгальского розового 1311 — результат уменьшения функциональной способности печени; д) снижение превращения токсичных продуктов обмена в нетоксичные — нарушение дезинтоксикационной функции печени. • Мезенхималъно-воспалительный синдром. Клинические признаки: Лабораторные признаки: а) повышение уровня у-глобулинов, часто с гиперпротеинемией, изменение осадочных проб, уровня иммуноглобулинов классов G, М, А; б) появление LE-клеток, неспецифических антител к ДНК, гладкомышечным волокнам, митохондриям; в) снижение титра комплемента, теста бласттрансформации лимфоцитов (БТЛ) и реакции торможения миграции лейкоцитов (ТМЛ); появление антител к тканевым и клеточным антигенам (гладкомышечным, митохондриальным, нуклеар-ным и др.). • Холестатический синдром. Клинические признаки: а) упорный д) лихорадка (при наличии воспаления); е) потемнение мочи, по-светление кала (нехарактерный симптом). Лабораторные признаки — повышение уровня билирубина (связанного); холестерина, р-липопротеидов, щелочной фосфатазы, у-глутамат-транспептидазы. • Астеновегетативный синдром. Клинические признаки: а) сла • Диспепсический синдром. Клинические проявления: а) тошнота, • Геморрагический синдром. Клинические проявления: а) кровоточи Лабораторные признаки: а) уменьшение количества и изменение функциональных свойств тромбоцитов; б) уменьшение синтеза факторов свертывания крови (II, V, VII). • Синдром гиперспленизма. Лабораторные признаки: а) анемия; Хронический активный гепатит (ХАГ)характеризуется ярко выраженной клинической симптоматикой, которая может быть объединена в три основных синдрома: 1) астеновегетативный; б) диспепсический; в) цитолитический («малой печеночной недостаточности»). С разной степенью выраженности встречаются мезенхимально-воспали-тельный синдром и синдром холестаза. На I этапе диагностического поиска можно выявить связь заболевания с перенесенным ранее вирусным гепатитом (ХАГ может формироваться непосредственно после перенесенного острого вирусного гепатита или же спустя несколько лет); если в анамнезе не удается выявить перенесенный вирусный гепатит, то в таком случае можно предположить, что больной перенес безжелтушную форму болезни. У части больных возможным доказательством перенесенного ранее вирусного гепатита можно считать гемотрансфузии, переливания компонентов крови, частые инъекции, прививки, контакт с больными, страдавшими острыми и хроническими гепатитами. Больных ХАГ часто беспокоит общая слабость, быстрая утомляемость, рассеянность, нередко — подавленное настроение. Диспепсические расстройства (тошнота, понижение аппетита, непереносимость жирной пищи и алкоголя, расстройства стула и пр.) редко достигают значительной выраженности. Преходящая желтуха, кровоточивость и другие жалобы, связанные с проявлением цитолитического синдрома, отчетливо выражены в период обострения заболевания. Желтуха, особенно в сочетании с кожным зудом, может быть результатом и холестаза, также наблюдающегося при этой форме гепатита. В период обострения наблюдаются повышение температуры тела (часто до субфебрильной), боли в суставах, мышцах (нерезко выраженные), проявления мезенхимально-воспалительного синдрома. Указание на проводимое ранее лечение глюкокортикоидами, иммуно-депрессантами служит доводом в пользу ХАГ. На II этапе диагностического поиска выявляют: а) клинические признаки цитолитического синдрома; б) проявления других синдромов: холестаза, геморрагического и пр.; в) увеличение печени. Похудание, изменение оволосения и ногтей, гинекомастия у мужчин, пальмарная эритема, сосудистые звездочки — проявления цитолитического синдрома с признаками печеночно-клеточной недостаточности. Желтушность кожи и слизистых оболочек свидетельствует о поражении печеночных клеток, а также о холестазе. Кожные кровоизлияния являются признаками геморрагического синдрома. Эти симптомы отмечаются непостоянно (примерно у половины больных) и преимущественно в период обострения болезни. Наиболее часто обнаруживают увеличение печени. Печень умеренно плотная, край заострен, пальпация болезненна. Иногда увеличена селезенка. У части больных в период обострения болезни отмечается преходящий асцит (выраженный нерезко). III этап диагностического поиска имеет решающее значение для постановки диагноза ХАГ. Полученные на этом этапе данные позволяют: а) уточнить этиологию (при обнаружении в крови HBsAg); б) определить степень активности процесса; в) определить степень вовлечения в патологический процесс других органов и систем; г) уточнить характер морфологических изменений печени (позволяющий также решить вопрос о возможности трансформации гепатита в цирроз). Клинический анализ крови помогает обнаружить гематологические изменения, характерные для ХАГ: увеличение СОЭ (проявление диспро-теинемии), сочетание анемии, лейкопении и тромбоцитопении — выражение синдрома гиперспленизма. При биохимическом исследовании крови в период обострения ХАГ выявляется значительное нарушение белкового обмена: гипоальбуминемия и гипергаммаглобулинемия, нередко сочетающаяся с гиперпротеинемией; повышение осадочных проб (особенно тимоловой). Нарушения пигментного обмена менее выражены и проявляются умеренным повышением содержания связанного билирубина в крови и уробилина в моче. Как правило, значительно нарушен клиренс бромсульфалеи-на (страдает выделительная функция печени). Задержка бромсульфалеи-на в плазме соответствует тяжести поражения печени. Показателем повреждения клеток печени является изменение активности аминотрансфераз. При ХАГ активность аминотрансфераз (аспартат-и аланинаминотрансферазы) повышается значительно: наблюдается 4 — 8-кратное увеличение их содержания. Значительно повышается уровень лактатдегидрогеназы (ЛДГ) и ее изоферментов ЛДГ-4 и ЛДГ-5. Помимо увеличения содержания аминотрансфераз и ЛДГ (так назы Выраженный синдром цитолиза отражает значительную степень нарушения целостности гепатоцитов и тяжесть течения ХАГ. Снижение уровня холинэстеразы — свидетельство печеночно-клеточной недостаточности. Синдром холестаза, помимо гипербилирубинемии, подтверждается гиперхолестеринемией (при поражении гепатоцитов, свойственном ХАГ, при отсутствии холестаза бывает гипохолестеринемия) и повышением содержания щелочной фосфатазы. На фоне проводимой терапии в случае успеха и достижения ремиссии у большинства больных биохимические показатели частично нормализуются, но иногда не достигают нормальных величин. В особенности это касается сывороточных ферментов (ACT, АЛТ, ЛДГ и др.), содержание в крови которых практически никогда не нормализуется. Иммунологические исследования у 90 % больных выявляют сдвиги, которые выражаются в увеличении содержания IgG, реже — IgM, появлении антител к гладкой мускулатуре и ядерной субстанции. Нарушение иммунологического гомеостаза проявляется также в уменьшении реакции БТЛ (бласттрансформации лимфоцитов) и ТМЛ (торможение миграции лейкоцитов). Для определения маркеров вирусных гепатитов применяют радиоиммунологический или иммуноферментный метод. Маркером вируса гепатита В, определяемым серологическим методом в сыворотке крови, является HBsAg, который выявляется почти во всех случаях ХАГ. При ХАГ в фазе репликации (размножения) серологическими маркерами являются HBeAg, анти-НВс класса IgM, HBV-DNA и DNA-P. Наиболее чувствительными показателями репликации и контагиозности являются DNA вируса (HBD-DNA) и антитела к дельта-вирусу (HDVAg) класса IgM. При одновременном инфицировании HBV и HDV эти антитела сочетаются с анти-HBs и анти-НВс класса IgM. Выявление анти-НВе может указывать на благоприятный прогноз заболевания. Родионуклидное исследование проводится для определения поглотительно-выделительной функции печени. Чаще всего используют два гепа-тотропных красителя — бенгальский розовый и бромсульфалеин, меченные 1311. У больных ХАГ отмечаются снижение поглотительной функции печени и замедление очищения крови от радиоиндикатора. Исследование распределения меченых соединений (чаще всего 198Аи) в печени (сцин-тиграфия) выявляет при ХАГ снижение накопления радиоиндикатора, что свидетельствует об уменьшении функционирующей паренхимы печени. Пункционная биопсия печени — основной метод, позволяющий поставить окончательный клинико-морфологический диагноз и получить представление об активности патологического процесса. Для ХАГ характерны следующие морфологические признаки: а) лимфогистиоцитарная инфильтрация со значительным количест б) некрозы и дистрофические изменения гепатоцитов; наличие пери в) фиброзные изменения портальных трактов, проникающие в дольку. Течение ХАГ может быть непрерывно рецидивирующим или с чередованием обострений и отчетливых клинических, а иногда и биохимических ремиссий. Редко встречается так называемый бессимптомный вирусный ХАГ. У таких больных при обследовании выявляют гепатомегалию, нормальный или нерезко повышенный уровень билирубина, повышение активности аминотрансфераз в 3 — 5 раз. При гистологическом исследовании биоптата печени обнаруживают картину ХАГ с умеренной или незначительной степенью активности. По выраженности клинических проявлений заболевания и нарушения функциональных проб печени выделяют ХАГ с умеренной и высокой активностью воспаления. При умеренной активности в клинической картине доминируют ас-теновегетативный и диспепсический синдромы, а также боли в правом подреберье, обусловленные растяжением печеночной капсулы в связи с гепатомегалией, перигепатитом, поражением внутрипеченочных желчных ходов. При биохимическом исследовании определяют умеренную ги-пергаммаглобулинемию, гипоальбуминемию, гипохолестеринемию, небольшое повышение в сыворотке крови ACT и АЛТ (не более чем в 4 — 5 раз). При высокой активности ХАГ отмечается тяжелое, быстро прогрессирующее течение болезни, сопровождающееся рецидивирующей желтухой, геморрагиями и другими симптомами печеночно-клеточной недостаточности, нередко присоединяются системные проявления (лихорадка, кожные высыпания, артралгии). Значительно нарушаются функции печени, в б и более раз повышено содержание ферментов в плазме крови, в высоком титре обнаруживают антитела к гладкой мускулатуре, ядерной субстанции и др. Этот вариант течения болезни достаточно быстро трансформируется в цирроз печени. Хронический аутоиммунный гепатит (ХАИГ)— хронический активный гепатит, характеризующийся особой выраженностью аутоиммунных процессов, высокой активностью воспалительно-дистрофических изменений печени, а также аутоиммунным поражением других органов и систем. По определению экспертов (Всемирный конгресс гастроэнтерологов, Лос-Анджелес, 1994), ХАИГ — неразрешившийся пе-рипортальный гепатит, протекающий обычно с гипергаммаглобулинемией и тканевыми аутоантителами, который в большинстве случаев положительно отвечает на терапию иммунодепрессантами. Своеобразие клинической симптоматики ХАИГ заключается в следующем: а) во множестве внепеченочных проявлений [лихорадка, артралгии, б) в значительной степени выраженности основных клинических син Заболевание встречается преимущественно у женщин, чаще в возрасте от 10 до 30 лет. Это следует учитывать при проведении диагностического поиска и преобладании внепеченочных проявлений заболевания. На I этапе диагностического поиска можно получить информацию о начале болезни. Часто встречаются и резко отличаются друг от друга следующие варианты: 1) ХАИГ, протекающий по типу острого вирусного гепатита (снача 2) ХАИГ, характеризующийся только выраженными внепеченочными В более поздних стадиях ХАИГ отмечаются различные печеночные синдромы и внепеченочные проявления — желтуха (медленно прогрессирующая), лихорадка, артралгии, миалгии, боли в животе и увеличение печени, кожный зуд и геморрагические высыпания. 3) Редко, но встречается «бессимптомное» течение заболевания, а У большинства больных течение заболевания прогрессирующее, практически без выраженных периодов ремиссии. На II этапе диагностического поиска можно получить много данных, свидетельствующих о поражении различных органов и степени их функциональной недостаточности. Отмечают разнообразные изменения кожных покровов, являющиеся проявлением васкулита (рецидивирующая пурпура, геморрагическая экзантема, узловатая эритема и пр.), эндокринных нарушений (угри, гирсу-тизм, полосы растяжения и синдром Кушинга в целом, гинекомастия, аменорея, сахарный диабет, поражение щитовидной железы с развитием ти-реоидита Хашимото и симптомами как тиреотоксикоза, так и микседемы); аллергических проявлений (крапивница). Очень часто встречаются кожные внепеченочные знаки — сосудистые звездочки, пальмарная эритема. Желтуха перемежающаяся, заметно усиливающаяся при обострении. Часто поражаются суставы. Вовлекаются в процесс преимущественно крупные суставы верхних и нижних конечностей, в отдельных случаях суставы позвоночника. Субъективные ощущения (артралгии) преобладают над объективными изменениями суставов (выпот в суставную сумку встречается редко; де-фигурация объясняется периартикулярным воспалением). Плеврит и перикардит диагностируются редко. Могут выявляться пневмониты и миокардиты. Лимфаденопатия и спленомегалия — выражение мезенхимально-вос-палительного синдрома — непостоянный признак заболевания. Печень умеренно плотная, увеличена у большинства больных, болезненность ее при пальпации различна. Несмотря на многочисленные клинические симптомы и высокую лихорадку (температура тела может повышаться до 38 — 39 °С), самочувствие у больных люпоидным гепатитом часто хорошее в отличие от всех других форм хронического гепатита. Таким образом, после II этапа выявляется полиорганность поражения. Степень вовлечения в процесс органов различна, что создает предпосылки для разнообразной трактовки этих изменений (от СКВ, системного васкулита до рака печени). III этап диагностического поиска приобретает решающее значение при постановке окончательного диагноза. Наиболее характерными являются изменения иммунного статуса: а) в крови часто обнаруживают LE-клетки; б) в сыворотке крови с вы Данные лабораторных исследований, характеризующие функциональное состояние печени и степень активности патологического процесса, изменены незначительно или же практически не отличаются от нормы. В период обострения отмечаются незначительное повышение активности аминотрансфераз, умеренная гиперпротеинемия со слабо выраженной ги-поальбуминемией и гипергаммаглобулинемией. Все эти изменения встречаются менее чем у половины больных. Функциональные пробы печени в период обострения резко изменены: а) активность аланин- и аспартатаминотрансфераз возрастает в большей степени, чем при всех других формах гепатита (превосходит норму в 5—10 раз); б) отмечается гипербилирубинемия, в основном за счет связанного билирубина; в) резко повышается содержание у-глобулинов (до 35 — 45%). При клиническом анализе крови выявляется резко увеличенная СОЭ (40-50 мм/ч). В ряде случаев уже на этом этапе диагностического поиска можно предположить люпоидный гепатит. Окончательный диагноз ставят после изучения биоптата печени. Наиболее важными морфологическими признаками люпоидного гепатита являются: а) массивная клеточная инфильтрация печеночной ткани; б) присутствие в инфильтрате большого числа плазматических клеток; в) деструкция пограничной пластинки; г) выраженные дистрофические и К признакам далеко зашедшего процесса относятся: а) распространенный фиброз внутри долек и портальных трактов; б) нарушения архитектоники дольки. Помимо описанной клинической картины ХАИГ, встречается иное течение заболевания, которое выявляется у лиц старших возрастных групп, характеризуется меньшей выраженностью системных проявлений и отличается хорошим прогнозом. Однако особенно важно правильно диагностировать тот вариант ХАИГ, который протекает с выраженными иммунными нарушениями, и дифференцировать его от ХАГ вирусной этиологии (см. табл. 13). Таблица 13. Признаки хронического аутоиммунного гепатита (ХАИГ) и хронического активного гепатита (ХАГ) вирусной этиологии
Возраст Пол Сопутствующие и иммунные заболевания Контакт с кровью и ее препаратами Клиническое течение Характер воспалительной инфильтрации Активность сывороточных аминотранс-фераз Колебания уровня сывороточных амино-трансфераз Аутоантитела в титре 1:40 Сывороточные маркеры вирусов Ответ на кортикостероидную терапию ХАИГ Молодой или средний Превалируют женщины Могут быть Отсутствует | Непрерывно прогрессирующее без ремиссий Преимущественно плазмо-клеточная Более 10 норм Необычны Присутствуют чаще анти-нуклеарные Отсутствуют Быстрое снижение активности аминотрансфераз ХАГ Любой Нет различий Необычны Многократный С наличием спонтанных ремиссий Преимущественно лимфоидная Менее 10 норм Обычны Отсутствуют Присутствуют Отсутствует или слабый Хронический персистирующий гепатит (ХПГ) отличается скудной клинической картиной. Из всех перечисленных ранее клинических синдромов отмечают умеренно выраженные диспепсический, астеновегетативный. Течение ХПГ монотонное; как правило, не удается выявить прогрес-сирования патологического процесса. На I этапе диагностического поиска жалобы, предъявляемые больным, не отличаются специфичностью: слабость, понижение трудоспособности, диспепсические явления (тошнота, отрыжка и пр.). Ряд больных жалоб не представляют. Заподозрить ХПГ в таких случаях практически не представляется возможным. Наиболее характерными жалобами, позволяющими предположить заболевание гепатобилиарной системы, являются чувство тяжести и давления, боль в области правого подреберья (у половины больных). На II этапе диагностического поиска главный, а у ряда больных единственный симптом нерезкое увеличение размеров печени и ее уплотнение. Желтуха, как правило, отсутствует. Повышение температуры тела, кожные внепеченочные знаки и проявления геморрагического синдрома наблюдаются крайне редко в периоды возможных обострений. В задачу III этапа диагностического поиска входит тщательное обследование больных с предполагаемым диагнозом ХПГ и болями в правом подреберье. Исследуют желчевыделительную систему (дуоденальное зондирование, холецистография, У3-диагностика) и пищеварительный тракт (рентгеноскопия, ирригоскопия, гастродуоденоскопия), так как основная роль в возникновении болевого синдрома принадлежит 11 - 540 нарушению моторной функции желчного пузыря и пищеварительного тракта. В отдельных случаях выявляется небольшое повышение содержания билирубина в крови (как свободного — непрямого, так и связанного — прямого). Наиболее чувствительная функциональная проба — бромсульфалеи-новая — изменяется также незначительно и менее чем у половины больных. При ХПГ в сыворотке крови маркерами вируса гепатита являются HBsAg и антитела: анти-НВс и реже — НВе, характеризующие фазу интеграции (включения) вируса в геном гепатоцита. Из сказанного вытекает, что характерных клинических критериев ХПГ не существует, в связи с чем существенную помощь в диагностике оказывает пункционная биопсия печени. К числу характерных морфологических признаков ХПГ относятся: а) расширение и умеренное склерозирование портальных полей при б) круглоклеточная мононуклеарная инфильтрация портальных трак в) умеренно выраженная дистрофия генатоцитов, в периоды обостре Хронический лобулярный гепатит (ХЛГ)по своим проявлениям занимает промежуточное положение между ОГ и ХПГ; его нередко обозначают как «застывший острый гепатит», после которого не наступило полной ремиссии в течение 6 мес или нескольких лет. ХПГ чаще болеют мужчины в возрасте 20-40 лет. Больных беспокоят тупые боли в правом подреберье. Нередко отмечается диспепсический синдром, выявляются признаки астении. При объективном обследовании у небольшого числа больных обнаруживают иктеричность склер и небольшую желтуху, умеренную гепатомегалию. Печеночные знаки крайне редки. Спленомегалия встречается у 20 % больных. Морфологически ХЛГ характеризуется мелкими некрозами во второй или третьей зоне ацинусов и внутридольковой лимфоидно-клеточной инфильтрацией, которая выражена значительно больше, чем инфильтрация портальных трактов, характерная для ХПГ. Для надежности диагностики ХЛГ необходимо изучение большого числа срезов и анализов повторных биопсий из-за неравномерности инфильтрации. Хронический холестатический гепатит (ХХГ)— вариант хронического гепатита с внутрипеченочным холестазом, обусловленным нарушением желчевыделительной функции печеночных клеток с нарушением образования желчной мицеллы, а также поражением мельчайших желчных ходов. Гистологические критерии ХХГ настолько отличаются от характерных для хронических гепатитов, что некоторые исследователи считают его одной из стадий развития первичного билиарного цирроза печени. Клиническая картина ХХГ определяется выраженностью синдрома холестаза. На I этапе диагностического поиска выявляют основной клинический симптом холестаза — кожный зуд (наблюдается у всех больных). Он не купируется симптоматическими препаратами, носит мучительный характер, часто предшествует желтухе. Желтуха может развиваться медленно, не сопровождается похуданием. При длительном холестазе возможно появление жалоб .связанных с нарушением всасывания в кишечнике жирорастворимых витаминов: расстройство сумеречного зрения, кровоточивость десен и кожи, боли в костях и пр. На этом же этапе пытаются уточнить этиологические факторы: а) длительный прием лекарственных препаратов (аминазина, сульфаниламидных, противодиабетических и диуретиков, антибиотиков, контрацептивов и пр. — аллергический холестаз; метилтестостерона, норэтандроло-на — простой неаллергический холестаз), непереносимость их; б) токсическое воздействие (алкоголь, контакт с ядохимикатами и прочими токсичными веществами); в) вирусный гепатит; г) эндокринные изменения (прием гормональных препаратов, беременность, эндокринные заболевания, чаще тиреотоксикоз). В ряде случаев этиология может остаться неизвестной (так называемый идиопатический холестаз). Это не исключает предположения о первичном холестазе. Тщательно выясняют наличие заболеваний, которые могли бы привести ко вторичному холестазу (желчнокаменная болезнь, опухоли гепатобилиарной системы, хронический панкреатит и пр.). В таких случаях диагноз ХХГ становится маловероятным. На последующих этапах производят уточняющие исследования. На II этапе диагностического поиска выявляют другие проявления холестаза: желтуху, пигментацию кожи (чаще генерализованную), ксантелазмы (приподнятые, узловатые мягкие образования — отложения липидов в коже). Обнаруживают расчесы кожи. «Печеночные ладони», сосудистые звездочки нехарактерны для ХХГ: единичные внепеченочные знаки встречаются у небольшого числа больных. Печень увеличена незначительно, плотная, с гладким краем (в периоды ремиссии может пальпироваться у края реберной дуги). У части больных наблюдается незначительное увеличение селезенки (в фазе обострения). Обнаружение при пальпации живота «округлого образования» в правом подреберье (желчный пузырь?) делает предположение о первичном холестазе сомнительным. Необходимы данные инструментальных и лабораторных исследований. Наибольшее значение в диагностике имеет III этап диагностического поиска. При подозрении на вторичный холестаз основным в диагностике становятся инструментальные методы исследования, позволяющие отвергнуть (или установить) существование причин, приводящих к внепеченоч-ному холестазу. Биохимическое исследование крови выявляет: а) повышение активности щелочной фосфатазы, у-глутаматтранспептидазы; б) гиперхолесте-ринемию, повышение уровня фосфолипидов, р-липопротеидов, желчных кислот; в) гипербилирубинемию (в основном за счет связанного билирубина); в моче уменьшенное содержание уробилина, могут встретиться желчные пигменты; в крови как проявление поражения гепатоцитов — умеренное повышение уровня аминотрансфераз. Иммунологическое исследование крови позволяет обнаружить мито-хондриальные антитела, которые являются характерным серологическим маркером внутрипеченочного холестаза. В последние годы выделен ряд подтипов антимитохондриальных антител (АМА) и установлено, что холе- статическим гепатитам лекарственной природы свойственны АМА-6. При этой же форме гепатита выявляются антитела к микросомам печени и почек (ALKM, подтип 2), а также антитела к мембранам печеночных клеток (ALM). Трудности, связанные с постановкой реакции, не позволяют рекомендовать этот тест для широкой клинической практики. Биохимические и ферментативные тесты дифференциально-диагностического значения в разграничении внепеченочного и внутрипеченоч-ного холестаза не имеют. Основная роль принадлежит инструментальным методам. Всем больным с желтухой неясного происхождения прежде всего необходимо проводить эхографию желчного пузыря и поджелудочной железы для исключения патологических изменений в этих органах, которые могут послужить причиной внепеченочного холестаза. Обязательным исследованием является эхография печени. В зависимости от ее результатов применяют следующие методы обследования больных: а) при расширенных желчных протоках (подозрение на внепеченоч- б) при нерасширенных желчных протоках для уточнения характера К основным морфологическим признакам внутрипеченочного (гепато-цитарного) холестаза относятся: а) накопление зерен желчных пигментов в гепатоцитах у билиарного полюса клетки; б) укрупнение гранул пигмента и появление их в желчных капиллярах; в) концентрация желчи в расширенных желчных капиллярах в виде сгустков (желчные тромбы). Для внепеченочного холестаза характерно расширение междольковых желчных протоков, уплощение их эпителия, впоследствии — накопление компонентов желчи в желчных ходах, а затем и в гепатоцитах. Следует отметить, что прижизненное морфологическое исследование печени имеет для диагностики холестаза второстепенное значение, поскольку констатируемые при световой микроскопии изменения (накопление компонентов желчи в гепатоцитах и желчных ходах и т.д.) появляются значительно позже биохимических и клинических признаков. Кроме того, пункционная биопсия печени противопоказана при наклонности к кровоточивости, что нередко отмечается у больных с холестазом. Исключение причин внепеченочного холестаза является достаточным для диагностики первичного внутрипеченочного холестаза. Диагностика. Распознавание хронического гепатита основывается на данных морфологического исследования биоптата печени с учетом клинической картины заболевания, изменений лабораторных показателей, в том числе маркеров вирусов гепатита. Критерии диагноза хронического гепатита: 1. Дистрофические изменения и некроз гепатоцитов, гистиолимфоци- 2. Гепатомегалия. 3. Повышение в крови содержания билирубина, «печеночных» фер 4. Проявления болевого, диспепсического и астеновегетативного син Формулировка развернутого клинического диагнозахронического гепатита учитывает: 1) клинико-морфологическую форму болезни (активный, аутоиммунный, персистирующий, лобулярный, холестатический); 2) этиологическую характеристику (если это возможно); 3) фазу течения (обострение, стихающее обострение, ремиссия); 4) степень активности процесса (активный, неактивный); 5) функциональное состояние печени (компенсированный, декомпенсированный процесс); 6) сопутствующие заболеванию синдромы, являющиеся составной частью болезни (указываются при их резкой выраженности, например геморрагический, холестаз и пр.). Лечение.Лечение хронических гепатитов — сложная и до сих пор окончательно не решенная проблема. При подборе терапии необходимо принимать во внимание: • Активность патологического процесса, подтвержденную результата • Этиологию хронического гепатита — вирусную, алкогольную, ток • Характер течения заболевания и предшествующую терапию. • Сопутствующие заболевания. Поскольку в прогрессировании и исходе болезни большое значение имеют рецидивы, вызванные многими факторами, необходимо проводить комплекс мероприятий, включающих соблюдение диеты, режима и направленных на нормализацию процессов пищеварения и всасывания, устранение кишечного дисбактериоза, санацию хронических воспалительных очагов; предусматривается также исключение профессиональных и бытовых вредностей. Эта базисная терапия является ведущей при ХПГ и нередко дает эффект и при ХАГ. Диета должна быть полноценной, содержащей в сутки 100 — 120 г белка, 80— 100 г жиров, 400 — 500 г углеводов. Исключаются жирные, острые блюда, продукты, содержащие экстрактивные вещества. Режим — физические нагрузки определяются активностью процесса. Постельный режим показан при ХАГ с высокой активностью, гипербили-рубинемией и выраженными проявлениями болезни. Больным хроническим гепатитом противопоказаны вакцинации, солнечные инсоляции, активная гидротерапия, переохлаждения, тяжелая физическая нагрузка. При обострении болезни базисная терапия включает назначение антибактериальных препаратов, подавляющих размножение и рост кишечной микрофлоры, в первую очередь в верхних отделах кишечника — канами-цин по 0,5 г 4 раза в день или левомицетин по 1 г 3 раза в день, возможно назначение энтеросептола или интестопана по 1 таблетке 3 раза в день. Длительность каждого курса — 5 — 7 дней. После прекращения антибактериальной терапии назначают биологические препараты, содержащие высушенные живые культуры антагонистически активных штаммов эшерихий (колибактерин) или бифидобактерий (бифидумбактерин). Эти препараты принимают в течение 1 — 1,5 мес. Для улучшения процессов пищеварения назначают ферментные препараты (не содержащие желчных кислот) — панзинорм, полизим, мезим-форте. Длительность приема — до 3 нед, в дальнейшем эти препараты назначают при появлении или усилении диспепсических расстройств. Базисная терапия способствует быстрому купированию диспепсического и болевого синдромов, уменьшению астенизации больных, а в ряде случаев и снижению биохимических показателей цитолиза. Продолжительность базисной терапии —1—2 мес. При высокой активности патологического процесса (наличие при гистологическом исследовании некрозов гепатоцитов, тяжелых клинических проявлений болезни, сохраняющееся более 10 нед повышение ACT и АЛТ, а также отсутствие эффекта от базисной терапии) назначают иммуносу-прессивную терапию (кортикостероиды в виде монотерапии или в сочетании с цитостатическими препаратами). Монотерапию преднизолоном проводят при наличии противопоказаний к назначению цитостатиков (азатио-прина). Начальная доза преднизолона — 30 — 40 мг/сут, снижают ее постепенно по мере купирования основных проявлений болезни и уменьшения ACT, АЛТ и у-глобулинов, но не ранее чем через 2 нед от начала терапии. В дальнейшем за 4 —8 нед дозу преднизолона уменьшают до 15 мг/сут. Поддерживающая доза преднизолона 10—15 мг, принимают ее длительно, не менее 2 — 3 лет после наступления ремиссии. При недостаточной эффективности преднизолона, рецидивировании гепатита на фоне уменьшения дозы, а также при развитии осложнений кортикостероидной терапии проводят комбинированное лечение преднизолоном и азатиоприном. К преднизолону (в суточной дозе 30 мг) добавляют азатиоприн в дозе 50 мг/сут; длительность приема азатиоприна составляет от нескольких месяцев до 1 — 2 лет (в комбинации с преднизолоном). Монотерапия азатиоприном в настоящее время не используется. Начинать и отменять иммуносупрессивную терапию следует только в условиях стационара. Длительная иммуносупрессивная терапия способствует наступлению ремиссии у большинства больных с ХАГ. В некоторых случаях (при непереносимости азатиоприна) назначают в виде иммуносу-прессивной терапии препараты 4-аминохинолинового ряда: хингамин (делагил), гидроксихлорохин (плаквенил); преднизолон 10—15 мг/сут и делагил 0,25 — 0,5 г/сут в течение 1—2 мес, затем дозу преднизолона постепенно снижают, а делагил в дозе 0,25 r/сут принимают в течение 1,5 — 2 лет. Иммуносупрессивная терапия больных хроническим вирусным гепатитом оказывается неэффективной. Лечение хронических гепатитов, вызванных вирусами гепатита В, С и D (HBV, HCV и HDV), направлено на применение противовирусных препаратов, основной из которых — интерферон (ИФН). В настоящее время выделены а-, р- и у-ИФН. а- и р-ИФН обладают выраженной противовирусной активностью, а у-ИФН — универсальный эндогенный модулятор). Целью противовирусной терапии хронического вирусного гепатита является: а) элиминация или прекращение репликации вируса; б) купирование или уменьшение степени активности воспаления; в) предупреждение прогрессирования гепатита с развитием отдаленных его последствий, включая цирроз и печеночно-клеточный рак. В настоящее время единственным эффективным средством является ос-ИФН как в качестве монотерапии, так и в комбинации с другими средствами (например, с синтетическими нуклеозидами, антиоксидантами и ДР-Х Существует человеческий лейкоцитарный сс-ИФН — велферон, а также генно-инженерные (рекомбинантные) препараты а-ИФН — реафе-рон, роферон А, интрон А. Наиболее эффективно подкожное или внутримышечное введение а-ИФН в дозе 5 — 6 ME 3 раза в неделю в течение 6 мес или 10 ME 3 раза в неделю в течение 3 мес при гепатите, вызванном вирусом гепатита В. При хроническом гепатите, вызванном вирусами С, и при суперинфекции вирусом гепатита D сроки применения а-ИФН удлиняются до 12 мес. Эффективность велферона существенно выше эффективности реком-бинантных интерферонов при лечении хронических вирусных гепатитов. Вместе с тем следует помнить, что при назначении а-ИФН могут возникать побочные реакции (лихорадка, озноб, головная боль, артралгии, диспепсические расстройства, кожные высыпания, развитие или усиление аутоиммунных реакций). Противопоказания к назначению а-ИФН: печеночно-клеточная недостаточность; выраженная лейко- и тромбоцитопения; гиперчувствительность к препаратам. Основное условие успешного лечения противовирусными препаратами — длительное и непрерывное применение, что не всегда возможно осуществить . При хроническом гепатите с минимальной активностью вместо имму-носупрессивной терапии проводят лечение так называемыми гепатопротек-торами (средствами, влияющими на обменные процессы в гепатите, уменьшающими перекисное окисление липидов и стабилизирующими биологические мембраны). Используют эссенциале по б —8 капсул в день в течение 2-—3 мес или силибинин (легалон), а также карсил, флавобион по 6 — 9 таблеток в сутки в течение 2 — 3 мес, затем по 3-4 таблетки на протяжении года. Применяется также липоевая кислота или липамид по 0,025 — 0,05 г 3 раза в день в течение 1 мес. В последнее время в комплексной терапии хронического гепатита используется гипербарическая оксигенация (ГБО), на курс назначают 10 15 сеансов. При холестатическом гепатите, помимо препаратов, воздействующих на обмен печеночных клеток, и средств, оказывающих иммунодепрессив-ное и противовоспалительное действие (при высокой активности процесса), назначают вещества, непосредственно устраняющие синдром внутри-печеночного холестаза. Так, холестирамин (связывает желчные кислоты) назначают по 10 — 16 г в сутки в течение 1 — 2 мес с последующим снижением дозы до б —8 г, общая продолжительность курса лечения от нескольких месяцев до нескольких лет. Вместе с препаратами, улучшающими обмен печеночных клеток, парентерально вводят витамины A, D, Е и К, всасывание которых нарушается при холестазе. Глюкокортикоидная терапия (преднизолон в начальной дозе 25 — 30 мг/сут) проводится длительно — от 4 —б мес до года (до снижения уровня билирубина и холестерина). При неэффективности терапии глюко-кортикоидами назначают цитостатики (азатиоприн в дозе 50— 100 мг/сут) в течение 2 мес — 1 года и более. Возможно сочетание цитостатиков с небольшими дозами глюкокортикоидов (5— 10 мг преднизолона в сутки). Проводится гемо- и лимфосорбция (уменьшает кожный зуд и способствует связыванию патологических иммунных комплексов); эффект достигается не во всех случаях, бывает недлительный. Прогноз.Наименее благоприятный прогноз у больных ХАИГ, наилучший — при хроническом персистирующем лобулярном гепатите. Хронический активный и холестатическии гепатиты переходят в цирроз в 20 — 30 % случаев. Хронический персистирующий гепатит у большинства больных заканчивается стабилизацией процесса, переходит в цирроз крайне редко. Профилактика.Профилактика хронического гепатита состоит прежде всего в предупреждении распространения болезни Боткина и активном диспансерном наблюдении лиц, перенесших эту болезнь. Должное внимание обращают на ликвидацию промышленных, бытовых интоксикаций, ограничивают прием лекарственных препаратов, способствующих развитию холестаза. ЦИРРОЗ ПЕЧЕНИ Цирроз печени (ЦП) — хроническое прогрессирующее диффузное заболевание разнообразной этиологии с поражением гепатоцитов, выраженными в различной степени признаками их функциональной недостаточности, фиброзом и перестройкой нормальной архитектоники печени, приводящей к образованию структурно-аномальных регенераторных узлов и портальной гипертензии, а в ряде случаев — к развитию печеночной недостаточности. Смертность от ЦП занимает не последнее место в структуре общей смертности населения, и ее показатели в разных странах составляют 15 — 30 на 100 000 населения. Классификация.В настоящее время Всемирной ассоциацией по изучению заболеваний печени (г. Акапулько, 1974) и ВОЗ (1978) рекомендовано использовать классификацию, основанную на этиологическом и морфологическом принципах. • По этиологии различают циррозы: а) вследствие вирусного поражения печени; б) вследствие недостаточности питания; в) вследствие хронического алкоголизма; г) холестатические; д) как исход токсических или токсико-аллергических гепатитов; е) конституционально-семейные; ж) вследствие хронических инфильтраций печени некоторыми веществами с последующей воспалительной реакцией (ге-мохроматоз, гепатоцеребральная дистрофия, или болезнь Вильсона-Коновалова); з) развивающиеся на фоне хронических инфекций (туберкулез, сифилис, бруцеллез); и) прочей этиологии, в том числе возникающие вследствие невыясненных причин (криптоген-ные). • По морфологическим и отчасти клиническим признакам выделяют Для микронодулярного цирроза характерны узлы регенерации преимущественно одинакового размера диаметром менее 3 мм и перегородки (септы) одинаковой ширины. При макронодулярном циррозе узлы регенерации крупные, намного больше 3 мм (некоторые из них достигают 5 см), перегородки имеют неправильную форму и разную ширину. • По активности процесса различают циррозы: а) активные, прогрес • По степени функциональных нарушений различают циррозы: а) ком Этиология.Из представленной классификации следует, что ЦП является полиэтиологическим заболеванием, однако частота выявления той или иной причины болезни весьма различна. Так, примерно 75 — 80 % ЦП имеют вирусную и алкогольную природу, остальные этиологические факторы встречаются гораздо реже. Частота ЦП невыясненной этиологии составляет, по данным некоторых авторов, до 26 % и более. Патогенез.Пусковым моментом патологического процесса при ЦП является повреждение гепатоцита, обусловленное воздействием различных этиологических факторов. Гибель паренхимы вызывает активную реакцию соединительной ткани (мезенхимы), что в свою очередь оказывает вторичное повреждающее воздействие на интактные гепатоциты и приводит к формированию ступенчатых некрозов — признаки перехода хронического гепатита в цирроз печени. Гибель гепатоцитов является также основным стимулом регенерации клеток печени, которая протекает в виде концентрического увеличения сохранившегося участка паренхимы; это ведет к образованию псевдодолек. Некроз гепатоцитов является также одной из основных причин воспалительной реакции (действие продуктов распада клеток). Значительную роль играют воспалительные инфильтраты, распространяющиеся из портальных полей до центральных отделов долек и приводящие к развитию постсинусоидального блока. Особенностью воспалительного процесса при ЦП является высокая фибропластическая активность, способствующая новообразованию колла-геновых волокон. Важным следствием этих процессов является нарушение кровоснабжения печеночных клеток: формирующиеся соединительнотканные септы, соединяющие центральные вены с портальными трактами, содержат сосудистые анастомозы, по которым происходит сброс крови из центральных вен в систему печеночной вены, минуя паренхиму долек. Кроме того, развивающаяся фиброзная ткань механически сдавливает венозные сосуды в ткани печени; такая перестройка сосудистого русла печени обусловливает развитие портальной гипертензии. Вышеописанные процессы, способствуя нарушению печеночной гемодинамики и развитию портальной гипертензии, приводят к повторным некрозам, замыкая порочный круг: некроз — воспаление — неофиб рил логе- нез — нарушение кровоснабжения гепатоцитов — некроз. В развитии портальной гипертензии наибольшее значение имеет сдавление разветвлений воротной вены узлами регенерирующих гепатоцитов или разросшейся фиброзной тканью. Портальная гипертензия является причиной развития портокавально-го шунтирования, асцита и спленомегалии. Коллатерали развиваются между бассейном воротной вены и системным венозным кровотоком (портокавальные анастомозы). Из них наибольшее клиническое значение имеют анастомозы в области кардиальной части желудка и пищевода, поскольку кровотечение из варикозно-расши-ренных вен этой области является одним из самых тяжелых осложнений портальной гипертензии, приводящих к летальному исходу. В развитии асцита, помимо собственно портальной гипертензии, играют роль и другие факторы: 1) падение коллоидно-осмотического давления плазмы в результате снижения синтеза альбумина в печени; 2) гиперальдо-стеронизм, развивающийся как за счет пониженной инактивации альдосте-рона в печени, так и за счет повышенной его выработки в ответ на гиповоле-мию; 3) нарушение функции почек вследствие сниженного почечного кровотока; 4) повышенная лимфопродукция в печени; 5) повышенная секреция вазопрессина, АДГ в ответ на повышение внеклеточной осмолярности. Спленомегалия также развивается вследствие портальной гипертензии. Помимо застойных явлений, увеличению селезенки способствуют разрастание соединительной ткани и гиперплазия ретикулогистиолимфоци-тарных элементов. Спленомегалия на этом этапе сочетается с гиперспле-низмом: анемией, лейкопенией и тромбоцитопенией, обусловленными повышенным разрушением и частичным депонированием форменных элементов крови в селезенке. Портальная гипертензия ведет также к значительному отеку слизистой оболочки кишечника (нарушение всасывания и экссудативная энтеро-патия). Шунтирование в обход паренхимы печени приводит к частичному функциональному отключению ее и развитию бактериемии, эндотоксине-мии, гиперантигенемии, недостаточной инактивации в печени ряда биологически активных веществ (в частности, гормонов альдостерона, эстрогенов, гистамина и др.), недостаточному поступлению в печень гепатотроф-ных веществ (глюкагон, инсулин и пр.). Серьезным осложнением шунтирования является портокавальная «шунтовая» энцефалопатия, которая может закончиться развитием комы. Помимо шунтовой (портокавальной, или экзогенной) комы, при ЦП возможно развитие так называемой печеночно-клеточной (собственно печеночной, или эндогенной) комы. Этот вид комы является проявлением гепатоцеллюлярной (печеночно-клеточной) недостаточности. При ЦП может развиться и смешанная кома вследствие обеих названных причин. Клиническая картина.Проявления ЦП варьируют в зависимости от этиологии, выраженности развития цирротического процесса, степени нарушения функции печени, выраженности портальной гипертензии и активности воспалительного процесса. При ЦП, как и при гепатитах, отмечаются синдромы: астеновегета-тивный, диспепсический, цитолитический, мезенхимально-воспалитель-ный, или синдром иммунного воспаления, холестатический, геморрагический, синдром гиперспленизма. Наличие и выраженность всех этих синдромов при различных циррозах печени колеблются в больших пределах, что будет показано при описании клинической картины различных форм цирроза. Общим признаком, с той или иной частотой встречающимся при различных формах ЦП на определенной стадии его развития, является портальная гипертензия. Из ранних симптомов портальной гипертензии наблюдаются: 1) метеоризм; 2) диспепсические расстройства (снижение аппетита, тошнота); 3) расширение вен брюшной стенки в боковых отделах живота, а в последующем и в области пупка (вплоть до развития «головы медузы»). Другие клинические проявления выражены при отчетливых проявлениях портальной гипертензии: спленомегалия, асцит, варикозное расширение вен пищевода, желудка, геморроидальных вен, кровотечения из них (ректальные кровотечения нечасты). При ЦП в большей степени, чем при ХГ, выражен синдром печеноч-но-клеточной недостаточности, проявляющийся геморрагическим диатезом, желтухой, печеночной энцефалопатией. Заболевание в своем развитии проходят ряд определенных стадий. В начальной стадии (компенсированной), нередко протекающей латентно, без признаков печеночной недостаточности, портальная гипертензия не выражена. Внепеченочные признаки болезни выражены слабо или отсутствуют, лабораторные показатели изменены незначительно или находятся в пределах нормы. Вместе с тем при морфологическом исследовании биоптатов печени обнаруживается характерная картина. В стадии выраженных клинических проявлений (субкомпенсированной) внепеченочные признаки выражены отчетливо, что сочетается с отчетливыми изменениями лабораторных исследований и явными признаками портальной гипертензии. В терминальной стадии (декомпенсированной) наряду с портальной гипертензией, выраженными внепеченочными признаками имеются клини-ко-лабораторные проявления печеночной недостаточности. В клинической картине ЦП (вне зависимости от его этиологии и формы) принято выделять активность цирротического процесса, что морфологически выражается в лимфогистиоцитарной инфильтрации портальных трактов, увеличении количества некрозов гепатоцитов, усилении ци-толитического и иммуновоспалительного синдромов, появлении признаков печеночной недостаточности. Клиническая картина ЦП эволюционирует в зависимости от развития осложнений: кровотечения из верхних отделов пищеварительного тракта; печеночные прекома и кома; вторичная инфекция (главным образом пневмонии); гепаторенальный синдром; трансформация в цирроз-рак; тромбоз воротной вены; образование конкрементов в желчных путях (при первичном били- арном циррозе). наиболее часто встречающаяся форма цирроза печени (до 40 % всех случаев ЦП). Объем получаемой информации на каждом этапе диагностического поиска различен в зависимости от состояния компенсации (или декомпенсации) процесса. На I этапе диагностического поиска в состоянии компенсации жалоб может не быть. При субкомпенсации ведущими являются симптомы диспепсического (потеря аппетита, плохая переносимость жирной пищи, тошнота, рвота, диарея) и астеновегетативного (слабость, повышенная утомляемость, снижение работоспособности) синдромов. Частый и стойкий симптом — чувство тяжести и боли в правом подреберье. При декомпенсации цирроза больной как первые проявления может отмечать увеличение живота и отеки ног, кровотечения из верхних отделов пищеварительного тракта, носовые кровотечения, редко — желтуху. Возможны нарушения сна, резкая раздражительность — проявления «печеночной» энцефалопатии. Этиологический фактор (если цирроз алкогольный) на I этапе на основании анамнестических данных уточнить бывает трудно, так как больные часто скрывают злоупотребление алкоголем. У части больных отмечается перенесенный ранее острый вирусный гепатит; выясняется бывшая ранее белково-витаминная недостаточность и т.п. На II этапе диагностического поиска уже в стадии компенсации могут обнаруживаться «печеночные» знаки: сосудистые звездочки, паль-марная эритема, гинекомастия, отсутствие или снижение оволосения в подмышечных впадинах, у мужчин — на груди, лице. Ногти часто белые и ровные. Отмечается темная пигментация кожи (отложение меланина вследствие повышенного содержания эстрогенов и стероидных гормонов в крови), иктеричность склер. При обследовании больного (особенно при подозрении на алкогольный генез ЦП) следует обращать внимание на возможные соматические и неврологические проявления алкоголизма; контрактуру Дюпюитрена, атрофию яичек, увеличение околоушных желез, атрофию мышц, миопатию и полиневриты. Возможны проявления алкогольного панкреатита, болезненность в характерных зонах (подробнее см. «Хронический панкреатит»). Обнаружение перечисленных признаков делает диагноз алкогольного цирроза очень вероятным. Одним из наиболее частых объективных симптомов является небольшое увеличение печени; край ее заостренный, консистенция плотная. Увеличенная селезенка на этой стадии пальпируется у половины больных. В стадии суб- или декомпенсации при физикальном обследовании выявляются желтуха (степень выраженности различна), значительное похудание, развитые венозные коллатерали на груди и передней брюшной стенке, нередко — пупочная грыжа, отеки нижних конечностей, спленоме-галия, асцит. Селезенка увеличена больше, чем печень. На III этапе диагностического поиска клинический анализ крови выявляет анемию, чаще гипохромную. Микроцитарная анемия — результат возможных кровотечений и(или) синдрома гиперспленизма (возможно сочетание с лейкопенией и тромбоцитопенией на стадии суб- или декомпенсации). При биохимическом исследовании крови в стадии компенсации обнаруживаются незначительные отклонения в функциональных пробах печени: гиперпротеинемия, небольшое повышение билирубина (у части больных). В стадии декомпенсации — выраженная диспротеинемия (гипоаль-буминемия, гипергаммаглобулинемия, положительные осадочные реакции), снижение содержания протромбина и холестерина, повышение билирубина, умеренное повышение активности аминотрансфераз. Иммунологические нарушения выражены незначительно. У отдельных больных отчетливо повышено содержание IgA (встречается при хроническом алкоголизме). Для выявления варикозно-расширенных вен пищевода производят рентгенологическое исследование, при подозрении на расширение вен желудка и пищевода — эзофагогастроскопию. Ректоскопия выявляет вари-козно-расширенные геморроидальные вены. Радионуклидное сканирование печени — метод изучения распределения радионуклидов (предпочтительно коллоидное золото — 198Аи), селективно поглощаемых печенью, с целью оценки ее структуры. При портальном циррозе снижена контрастность сканограмм, неравномерно распределен радиоактивный препарат: почти полностью отсутствует в периферических отделах органа, повышено накопление его в селезенке. Лапароскопия и прицельная биопсия печени не только выявляют цирроз, но позволяют установить его морфологический тип и признаки активности процесса. На ранних стадиях при лапароскопии можно обнаружить увеличенную печень с картиной мелкоузлового цирроза, симптомы портальной гипертензии, на поздних стадиях — картину крупно- и мелкоузлового цирроза. Морфологическое изучение биоптата печени при циррозе алкогольного генеза выявляет: а) жировую дистрофию гепатоцитов; б) образование ложных долек; в) обширное развитие фиброза. Признаками алкогольной этиологии ЦП являются тельца Маллори (скопления гиалина в центре долек) и очаговая инфильтрация нейтрофилами портальных трактов. Крупноузловой (постнекротический) цирроз печенисоставляет до трети всех ЦП и бывает, как правило, вирусной этиологии. Заболевание значительно чаще встречается у лиц молодого и среднего возраста. Для этой формы цирроза характерно быстрое, клинически выраженное прогрессирование. В клинической картине на первый план выступают проявления печеночной недостаточности, предшествующие выраженным признакам портальной гипертензии. Симптоматика в период обострения заболевания напоминает острую фазу вирусного гепатита или обострения ХАГ. Характерны желтуха, лихорадка, астеновегетативный, диспепсический и цитолитический синдромы (последние два резко выражены). На I этапе диагностического поиска главными признаками являются желтуха, боли в животе (в правом подреберье и подложечной области), повышение температуры тела, диспепсические расстройства, слабость. Степень выраженности жалоб усиливается в период обострения; в период ремиссии они ослабевают (но не исчезают). Это позволяет уже на данном этапе обследования больного судить об активности процесса. В случае развития постнекротического цирроза как исхода ХАГ остается полиорганность поражения (у ряда больных сохраняется сходство с СКВ); с этим связано и разнообразие жалоб (артралгии, геморрагические высыпания и др.). На этом же этапе уточняют этиологию цирроза: у подавляющего большинства больных устанавливается связь с перенесенной ранее болезнью Боткина; у некоторых выявляется интоксикация гепатотропными ядами, отмечается лекарственная непереносимость (возможный этиологический фактор). Выявляются характерные особенности развития цирроза: 1) прогрессирующее течение; 2) печеночная недостаточность развивается при отсутствии признаков предшествовавшей портальной гипертензии. На IIэтапе диагностического поиска даже в стадии компенсации внепеченочные признаки выражены в большей степени, нежели у больных портальным ЦП. В стадии субкомпенсации, особенно при декомпенсации ЦП, отмечаются выраженные желтуха и другие «печеночные» знаки. При высокой активности процесса возможны полисерозиты, чаще — преходящий асцит. На поздних стадиях асцит является постоянным признаком болезни. Печень и селезенка увеличены значительно. Печень имеет острый и болезненный край. Болезненность при пальпации печени и селезенки усиливается в период обострения. Данные IIIэтапа диагностического поиска по результатам клинического и биохимического анализа крови выявляют признаки функциональной недостаточности гепатоцитов: повышение уровня билирубина (преимущественно за счет связанного), снижение содержания холестерина и протромбина, диспротеинемию (резкое увеличение количества у-глобу-линов и значительное понижение альбуминов, изменение осадочных проб, особенно тимоловой), повышение уровня аминотрансфераз, ЛДГ и ее 4 — 5-й фракции. Отмечается выраженное изменение бромсульфалеиновой пробы. Задержка бромсульфалеина в плазме соответствует тяжести поражения печени. Как правило, выражены явления гиперспленизма: анемия, тромбоцитопения, лейкопения. Вирусную природу ЦП подтверждает или выявляет обнаружение при серологическом исследовании крови маркеров вирусной инфекции (HBsAg, антител к HBsAg и др.). Симптом портальной гипертензии — варикозное расширение вен пищевода, желудка и геморроидальных вен — выявляется при рентгенологическом исследовании пищеварительного тракта, эзофагогастроскопии и ректороманоскопии. Радионуклидное сканирование печени с коллоидным золотом или технецием играет существенную роль в диагностике, выявляя диффузное снижение поглощения изотопа с очаговой неравномерностью ее распределения в селезенке, активно накапливающей изотоп. Лапароскопия и прицельная биопсия помогают обнаружить крупноузловое поражение печени. Морфологические признаки активности цирроза выражаются в преобладании деструктивных процессов: появление большого количества ступенчатых некрозов, резко выраженная гидропическая дистрофия, большое количество очаговых скоплений гистиолимфоидных инфильтратов в различных участках узлов-регенератов. Вирусную природу ЦП подтверждает также обнаружение в биоптатах печени маркеров вирусного поражения при специальной окраске орсеином. Билиарные циррозы (БЦ)встречаются у 5 —10 % больных циррозами печени. Различают первичный (истинный) билиарный цирроз (ПБЦ) и вторичный билиарный цирроз (ВБЦ). ПБЦ поражает почти исключительно женщин. ВБЦвстречается и у мужчин. Возникает ПБЦкак следствие хронического холестатического гепатита (ХХГ) и формируется на поздних этапах этого заболевания. Этиология его идентична таковой ХХГ (вирус, лекарственные препараты, эндокрин- ные нарушения). У части больных, как и при ХХГ, этиология заболевания остается неизвестной. В основе ПБЦ лежит внутрипеченочный холестаз, а в основе ВБЦ — внепеченочный холестаз (редко — длительное нарушение оттока желчи на уровне крупных внутрипеченочных желчных протоков). Чаще всего ВБЦ развивается при «доброкачественной» обструкции, так как «злокачественная» обструкция приводит к смерти раньше, чем успевает развиться цирроз. Наиболее благоприятным фоном для развития цирроза является полная обструкция желчных путей. Приблизительные сроки формирования цирроза — от 3 мес до 1V2 лет. Клинические особенности БЦ состоят в доминировании холестатичес-кого синдрома, позднем проявлении и небольшой выраженности синдромов портальной гипертензии и печеночно-клеточной недостаточности. На I этапе диагностического поиска выявляют основные жалобы, характерные для длительного холестаза: желтуху, кожный зуд, кровоточивость, боли в костях (особенно в спине и ребрах), диарею. Асцит беспокоит больных лишь в поздней стадии болезни. Уже на этапе анализа анамнестических данных создается впечатление о первичном или вторичном БЦ. Для первичного БЦ характерным является предшествующий хронический холестатический гепатит, для вторичного — указания на имевшуюся ранее патологию желчевыводящих путей или перенесенные операции по поводу опухолей других органов (возможность метастатических опухолей гепатопанкреатодуоденальной зоны). При вторичном БЦ наряду с симптомами холестаза отмечаются приступы желчной колики, лихорадка. На II этапе диагностического поиска отчетливо проявляются симптомы длительного холестаза: желтуха, диффузная гиперпигментация кожи, ее утолщение, огрубение, сухость, множественные следы расчесов, ксантомы и ксантелазмы на веках, локтях, подошвах, ягодицах; геморрагии разной стадии. Болезненность при поколачивании по костям, пальцы в виде барабанных палочек — результат остеомаляции и субпериосталь-ных новообразований костной ткани при длительном холестазе. Сосудистые звездочки встречаются реже, чем при других видах ЦП, выражены слабо. Печень всегда увеличена, плотная, может достигать огромных размеров. Селезенка также увеличена, но незначительно. Портокавальные анастомозы поверхностных вен на груди и животе, как и асцит (проявление портальной гипертензии), выявляются на поздних стадиях болезни. Кроме того, асцит может возникать как проявление активности цирроза, а по мере снижения активности процесса исчезать. На III этапе диагностического поиска выявляют: а) лабораторные признаки холестаза; б) иммунные нарушения при первичном холестазе; в) проявления портальной гипертензии; г) осложнения; д) причины вне-печеночного холестаза; е) морфологические признаки цирроза. Лабораторные признаки холестаза выражены резко: 1) гипербилирубинемия достигает высоких цифр (более 342 мкмоль/л), 2) значительно возрастает уровень общих липидов, фосфолипидов и 3) повышается активность щелочной фосфатазы, у-глутаматтранспеп- Биохимические признаки цитолиза гепатоцитов с печеночно-клеточ-ной недостаточностью появляются (и прогрессируют) лишь на поздних стадиях процесса. В начальном периоде БЦ подъем активности амино-трансфераз выражен слабо. При первичном БЦ закономерно выявляется изменение иммунологических показателей: повышение титра IgG и IgM (больше IgM), резкая гипергаммаглобулинемия, повышение СОЭ (при вторичном БЦ СОЭ также повышена, но как результат воспаления); выявляются антимито-хондриальные антитела в высоком титре. С помощью иммуноферментного анализа выделены подтипы антими-тохондриальных антител: анти-М-8 характерны для наиболее прогрессирующих форм заболевания, а анти-М-9 — для наиболее доброкачественных форм заболевания. Рентгеноскопия пищеварительного тракта помогает выявить варикозное расширение вен пищевода, эзофагогастроскопия — расширение вен желудка (проявления портальной гипертензии). Эти методы исследования помогают обнаружить язвы желудка и двенадцатиперстной кишки как проявление осложнений БЦ. Такое осложнение, как остеомаляция, выявляется при рентгенологическом исследовании костей (деминерализация костей, полосы просветления, выявляемые особенно часто в костях таза и лопаток, сдавление и деформация позвонков). Инструментальные методы исследования (гастродуоденоскопия, ретроградная дуоденопанкреатохолангиография, УЗИ, лапароскопия, сканирование печени и пр.) позволяют в большинстве случаев выявить причины внепеченочного холестаза. Последовательность проведения исследований, их информативность и значимость для диагностики — см. «Хронические гепатиты». В случае подозрения на опухолевый процесс производят ангиографию печени и целиакографию. Методы позволяют оценить артериальное кровоснабжение печени, селезенки, поджелудочной железы и исключить или подтвердить наличие опухоли. Сканограмма при билиарном циррозе в отличие от портального и постнекротического цирроза отличается минимальными изменениями. Гистологические признаки цирроза определяются по данным биопта-та печени, полученного при лапароскопии или чрескожной пункции. Диагноз ПБЦ подтверждают следующие признаки (учитывать их сочетание): 1) деструктивные изменения междольковых желчных протоков; 2) отсутствие междольковых протоков более чем в половине порталь 3) холестаз преимущественно на периферии дольки; 4) расширение, инфильтрация и фиброз портальных полей. При вторичном БЦ морфологическими критериями являются: 1) расширение внутрипеченочных желчных ходов; 2) некрозы в периферических частях печеночных долек с образовани 3) нормальное дольковое строение в отдельных участках печени. Диагностика ЦП. Распознавание цирроза печени основывается на выявлении: 1) клинических проявлений цитолитического (сочетающегося с пече- 2) лабораторно-инструментального подтверждения наличия указан 3) морфологических признаков цирроза печени (наиболее достовер Дифференциальная диагностика.Трудности в диагностике цирроза печени обусловлены сходством клинической картины болезни с проявлениями хронического гепатита, а также ряда других заболеваний. От хронического гепатита цирроз печени отличают следующие клинические симптомы: а) резкое нарушение архитектоники органа (по данным морфологи б) глубокие дистрофические и некробиотические изменения паренхи Среди заболеваний, требующих дифференциальной диагностики с циррозом печени (преимущественно портальным), следует выделить: • цирроз-рак и первичный рак печени (асцит развивается вследствие • констриктивный перикардит, сопровождающийся увеличением пе • доброкачественный сублейкемический миелоз (миелофиброз, остео- • альвеолярный эхинококкоз, проявляющийся не только увеличением • амилоидоз и гемохроматоз, сопровождающиеся гепатолиенальным Формулировка развернутого клинического диагнозаучитывает следующие пункты: 1) этиология; 2) морфология: микронодулярный (мелкоузловой), макронодуляр- 3) морфогенез: постнекротический, портальный, билиарный, смешан 4) клинико-функциональная характеристика: а) компенсированный; б) субкомпенсированный; в) декомпенсированный (указывают выраженность портальной ги- 5) другие синдромы (указывают при их резкой выраженности: холе- 6) активность цирроза (активная или неактивная фаза: обострение 7) течение: прогрессирующее, стабильное, регрессирующее. Примечания. П. 1 указывается при четких данных анамнеза и результатах серологического исследования (для выявления или подтверждения вирусной этиологии цирроза). Следует помнить о большой частоте криптогенных форм; п. 2 указывается при наличии биопсии или лапароскопии; п. 3 в настоящее время указывается не всеми. Лечение.Тактика лечения ЦП определяется активностью и характером патологического процесса, основными клиническими проявлениями и степенью функциональных расстройств. Для подбора адекватной терапии важно учесть стадию течения и степень активности процесса. Так как признаки активности при ЦЕ (некрозы гепатоцитов, мезенхимально-воспали-тельная реакция, цитолитический синдром) аналогичны таковым при хроническом гепатите, то лечение активного ЦП полностью совпадает с лечением ХАГ. Основа терапевтических мероприятий — иммуносупрессивная терапия (применение кортикостероидов изолированно или в сочетании с цитостатическими препаратами). Начальная стадия ЦП с выраженной активностью процесса хорошо поддается соответствующей терапии, тогда как при далеко зашедшей стадии эффективность кортикостероидов и цитостатиков низка. Всем больным ЦП показана базисная терапия, включающая, как и при хроническом гепатите, ряд правил. • Соблюдение режима общегигиенических мероприятий; исключение профессиональных и бытовых вредностей, в том числе алкоголя; соблюдение режима труда, отдыха и питания. В компенсированной стадии ЦП больные могут выполнять работы, не связанные с вынужденным положением тела, длительной ходьбой или стоянием, воздействием высокой или низкой температуры, значительными ее колебаниями. При портальной гипертензии следует избегать любых физических усилий, вызывающих повышение внутрибрюшного давления. При выраженной активности и декомпенсации процесса показаны постельный режим и стационарное лечение. • Всем больным показано соблюдение диеты (стол № 5), но следует • Лечебные мероприятия, направленные на нормализацию процессов • Запрещение проведения физиотерапевтических процедур, инсоля • Устранение диспепсических расстройств, недостаточности питания Такое подробное описание мероприятий базисной терапии объясняется тем, что строгое ее соблюдение играет решающую роль в лечении ряда больных ЦП. Так, больные компенсированным неактивным или с минимальной активностью ЦП в специальной лекарственной терапии не нуждаются. Им показана лишь базисная терапия. Больные субкомпенсированным неактивным или с минимальной активностью ЦП нуждаются в строгом соблюдении базисной терапии (корти-костероиды и иммунодепрессанты им не показаны), лекарственную терапию проводят патогенетическими и симптоматическими средствами. К ним относятся дезинтоксикационные средства (внутривенное капельное введение гемодеза или 200 — 300 мл 5 % раствора глюкозы), эссенциале (по 2 капсулы 3 раза в день) или карсил (легалон) по 2 — 3 таблетки 3 раза в день на протяжении 3 мес и более. На фоне этого лечения или после окончания приема указанных лекарственных средств назначают липоевую кислоту или липамид (внутрь). При гипоальбуминемии назначают анаболические стероиды (ретаболил в инъекциях или неробол внутрь). Декомпенсированный ЦП с признаками портальной гипертензии (кроме вышеперечисленных мероприятий) нуждается в лечении отечно-асцити-ческого синдрома: назначают спиронолактон, или верошпирон (200 мг/сут, через неделю дозу снижают до 150 мг; на поддерживающей дозе в 75 — 100 мг/сут больной находится несколько месяцев). На фоне приема верошпирона показано назначение диуретиков, если диурез ниже оптимального. Диуретики назначают в небольших дозах (фу-росемид 40 мг/сут 3 —4-дневными курсами), так как избыточное выведение калия и других жизненно важных метаболитов может вызвать грозные осложнения (печеночная кома и пр.). Консервативное лечение портальной гипертензии предусматривает также прием лекарственных препаратов, снижающих портальное давление. Для этого используют пролонгированные нитраты в обычных терапевтических дозах и пропранолол в дозах, снижающих частоту сердечных сокращений в покое на 25 %. Такая терапия проводится в течение длительного времени (месяцы, годы). Это лечение является обязательным для больных с наличием в анамнезе кровотечения из расширенных вен пищевода. Терапия асцита включает, помимо вышеописанного, введение белковых препаратов: нативную концентрированную плазму и 20 % раствор альбумина. Они способствуют повышению коллоидно-осмотического давления плазмы и содержания альбумина. Стойкий асцит, не поддающийся адекватной терапии, является показанием к проведению абдоминального парацентеза. Для декомпрессии портальной системы показаны операции: наложение портокавальных сосудистых анастомозов; перевязка ветвей чревной артерии; органопексия, спленэктомия. Показаниями к операции являются варикозно-расширенные вены пищевода у больных, перенесших кровотечение, а также высокая портальная гипертензия. Оперативное лечение производят также больным с наличием синдрома гиперспленизма и указанием на перенесенное кровотечение или его угрозу. При гиперспленизме и низком содержании лейкоцитов (менее 2,0109/л) и тромбоцитов (при наклонности к кровоточивости) вводят лейкоцитную и тромбоцитную массу. При билиарном ЦП лечение холестаза проводится аналогично таковому при ХХГ (см. «Лечение хронического холестатического гепатита»). Борьба с осложнениями • Остановка пищеводно-желудочного кровотечения включает: а) прямое переливание крови от донора свежезаготовленной крови б) внутривенное введение питуитрина или вазопрессина в 100 — в) обтурационное тампонирование пищевода зондом с баллоном, г) для предупреждения постгеморрагической комы показаны удале Борьба с пищеводно-желудочным кровотечением не всегда заканчивается успешно, несмотря на весь комплекс мероприятий; в 20 —40 % случаев наступает смертельный исход. • Лечение печеночной комы требует введения всех препаратов внут 6) для улучшения обмена печеночных клеток — эссенциале, витаминов группы В и С, липоевой кислоты, препаратов калия, которые вводят в 5 % растворе глюкозы внутривенно капельно (за сутки — до 2 — 3 л); в) постоянно контролируют электролитный баланс, кислотно-основное состояние и своевременно регулируют его введением электролитов и буферных смесей; при развитии метаболического ацидоза вводят 200 — 600 мл 4 % раствора гидрокарбоната натрия, а при выраженном метаболическом алкалозе вводят препараты калия до 10 г/сут; г) антибиотики широкого спектра (тетрациклин или канамицин, ампициллин) вводят через желудочный зонд для подавления жизнедеятельности кишечной микрофлоры и профилактики бактериальных осложнений; д) при печеночно-кле-точной коме вводят большие дозы глюкокортикоидных гормонов (преднизолон 150 мг струйно и далее каждые 4 ч по 90 мг). Рекомендуется через носовой катетер вводить кислород со скоростью 2-4 л в минуту; при возможности — обменные переливания крови по 5 — 6 л ежедневно (7 10 дней). Однако, несмотря на интенсивное лечение, печеночная кома при ЦП чаще всего заканчивается летальным исходом, хотя в последние годы появились сообщения об успешном ее лечении. Профилактика комы сводится к проведению лечебных мероприятий, предотвращающих развитие желудочно-кишечных кровотечений, инфекций, интоксикации; требуется осторожность в назначении диуретиков, седативных и снотворных препаратов. Прогноз.Сформировавшийся ЦП является необратимым состоянием, однако успешная борьба с активностью процесса, проведение всего комплекса лечебных мероприятий могут способствовать тому, что ЦП длительное время остается компенсированным. Профилактика.Мероприятиями профилактики являются устранение или ограничение действия этиологических факторов, своевременное распознавание и лечение хронического гепатита и жировой дистрофии печени. При наличии цирроза необходимо проводить мероприятия, направленные на прекращение прогрессирования процесса и профилактику осложнений.
|
||||
|
Последнее изменение этой страницы: 2024-06-27; просмотров: 5; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.218.250.241 (0.04 с.) |

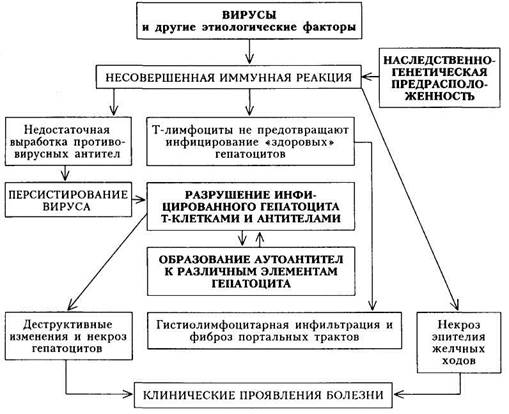


 Признак
Признак


