
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Сила внутреннего трения пропорциональна градиенту скорости и площади трущихся слоев и направлена против движения слоевСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Градиентом скорости называется изменение скорости на каждой единице длины в направлении, перпендикулярном скорости
h – коэффициент внутреннего трения, равный силе внутреннего трения между слоями единичной площади при градиенте скорости, равном единице. 4. Из молекулярно–кинетического рассмотрения явления внутреннего трения вытекает, что коэффициент внутреннего трения в газе равен
где r – плотность газа. Именно эта формула позволяет определить среднюю длину свободного пробега <l>:
Выразим h,r, < υ > через известные параметры и величины, которые можно измерить, и рассчитаем <l>: а) для нахождения h воспользуемся формулой Пуазейля, определяющей объем газа V, протекающего через трубку длинной ℓ, радиусом r, за время t, при перепаде давления на ее концах, равном D p:
б) средняя скорость молекул газа из молекулярно–кинетической теории выражается:
в) плотность газа r найдем из уравнения состояния идеального газа (Менделеева–Клапейрона)
Подставляя (6,7,8,) в (5) получим:
Соберем все постоянные в одну и вычислим ее:
Окончательно получим:
const 1 – табличное значение. Как видно из (10), задача свелась к определению величин V, t, T, D p. D p –перепад давления на концах трубки. Перепад давления можно создать за счет выливания жидкости из баллона, который соединен с одним из концов трубки (капилляра) (рис.4). Когда кран закрыт, давление воздуха внутри баллона и снаружи одинаковое, перепад давления на концах трубки капилляра равен нулю. Если кран открыть полностью, то вода начнет вытекать, давление газа внутри баллона начнет уменьшаться из–за увеличения объема газа, на концах трубки появится перепад давления. Признаком установившегося перепада давления является капание воды с полностью открытого крана. В этом случае можно считать, что количество прошедшего воздуха через трубку равно количеству воды, вытекшей из баллона.
Выполнение работы
2. Подставьте под капающую воду мензурку (при полностью открытом кране), одновременно включите секундомер. 3. Измерьте объем вытекшей воды и время, все данные занесите в таблицу. 4. После того как найдете среднюю длину свободного пробега, определите эффективный диаметр по формуле (3):
Концентрацию молекул воздуха определим из выражения
где Р 0, T 0 – давление и температура при нормальных условиях, T 0 = 273,15 К, Р 0=1,0132×105 Па = 760 мм рт.ст.; n 0 – число Лошмидта – число молекул, находящихся в 1 см3 идеального газа при нормальных условиях, оно равно: n0 = 2,687 1019 см–3, P,T –давление и температура, при которых протекает опыт.
Окончательно формула для расчета эффективного диаметра:
Занесите данные в таблицу
Расчет погрешности Относительная ошибка длины свободного пробега: Относительная ошибка эффективного диаметра
Δτ = 0,01 с; Δ Т = 0,50; Δ Р = 20 ед.давл; Δ V =10–6 м3
Задачи
1. Определите среднюю длину свободного пробега <λ> молекул кислорода, находящегося при температуре 00С, если среднее число столкновений, испытываемых молекулой в 1 с, равно 3,7.109. Ответы: 1) 6,5.10–8 м; 2) 4,52.10–8 м; 3) 11,5.10–8 м; 4) 15.10–8 м; 5) 3.10–8 м. 2. При каком давлении средняя длина свободного пробега молекул водорода равна 2,5 см, если температура газа равна 670 С? Диаметр молекул водорода 0,28 нм. Ответы: 1) 1,32 Па; 2) 0,77 Па; 3) 0,539 Па; 4) 2,37 па; 5) 0,428 Па. 3. Определите длину свободного пробега молекул углекислого газа при нормальных условиях, если при этих условиях его плотность ρ=2 кг/м3, а коэффициент внутреннего трения 14,9.10–6кгм/с. Ответы: 1) 8,32.10–8м; 2) 3,52.10–10м; 3) 7,42.10–8м; 4) 6,20.10–8м; 5) 3,90.10–8м. 4. Как связаны давление идеального газа Р, концентрация его молекул и его температура? Ответы: 1) Р= 5. Средняя длина свободного пробега <λ1> молекул водорода при нормальных условиях составляет 0,1 мкм. Определите среднюю длину свободного пробега при давлении 0,1 мПа, если температура остается постоянной. Ответы: 1) 52 м; 2) 15,3.10–2 м; 3) 101 м; 4) 1,34 м; 5) 7,2.10–4 м. 6. Средняя длина свободного пробега <λ> молекулы углекислого газа при нормальных условиях равна 40 нм. Определить среднее число соударений <z>, которые испытывает молекула в 1 с. Ответы: 1) 1010 с–1; 2) 3,1.109 с–1; 3) 7,52.109 с–1; 4) 9,05.109 с–1; 5) 8,33.109 с–1. Контрольные вопросы 1. Дать определение средней длины свободного пробега и эффективного диаметра молекул. 2. Какое физическое явление положено в основу работы? Запишите уравнение Ньютона. 3. Каков физический смысл коэффициента внутреннего трения.? 4. Что такое градиент скорости и куда он направлен? 5. Почему вода из баллона сначала вытекает, а затем капает? 6. Объяснить формулу Пуазейля. 7. Подробно вывести рабочую формулу.
Литература 1. Савельев И. В. Курс общей физики, т. 1. М.: Наука, 1989. с.269–274, 285–287. 2. Трофимова Т. И. Курс физики. М.: Высшая школа, 2002, с.91–96 3. Детлаф А. А., Яворский Б. М. Курс физики, М.: Высшая школа, 1989, с.114–119. Лабораторная работа 1.11
|
||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-08; просмотров: 696; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.220 (0.008 с.) |

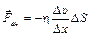 . (4)
. (4)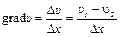 .
.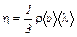 ,
,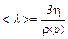 . (5)
. (5)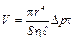 ;
;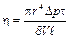 . (6)
. (6)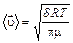 . (7)
. (7)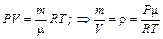 . (8)
. (8)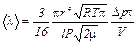 . (9)
. (9)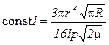 .
.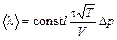 . (10)
. (10)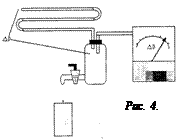 1. Откройте кран, подождите пока вода не начнет капать и не установится перепад давления D p (по манометру).
1. Откройте кран, подождите пока вода не начнет капать и не установится перепад давления D p (по манометру).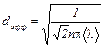 .
.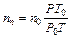 ,
,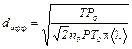 . (11)
. (11)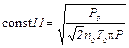 ;
;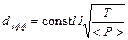 . (12)
. (12)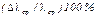
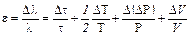 Абсолютная ошибка:
Δλ = ε λ,
Абсолютная ошибка:
Δλ = ε λ,
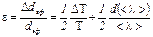 Абсолютная ошибка:
Δ dэф = ε dэф
Абсолютная ошибка:
Δ dэф = ε dэф
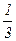 nкТ; 2) Р=
nкТ; 2) Р= 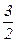 nкТ; 3) Р=nкТ; 4) Р=
nкТ; 3) Р=nкТ; 4) Р= 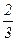 nкТ; 5) Р=кТ.
nкТ; 5) Р=кТ.


