Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Общие представления и понятия титриметрического анализа. Способы фиксации точки эквивалентностиСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
К основным понятиям титриметрии относятся: аликвота, рабочий раствор, стандартный раствор, титрование, титрованный раствор, титрант; кривая титрования, конец титрования и точка эквивалентности. Приведем определение этих понятий. Ø Аликвота (аликвотная часть) (Va ) – точно отмеренный объем раствора (мл) взятый для титрования. Обычно это раствор, содержащий определяемый компонент, который помещают в колбу для титрования. Ø Рабочий раствор – раствор реагента точно известной концентрации, используемый непосредственно при выполнении анализа вещества. Ø Стандартный раствор – это раствор точно известной концентрации применяемый для стандартизации других растворов; может выполнять функции рабочего раствора. Ø Титрованный раствор (стандартный титрованный раствор) – любой раствор, концентрация которого точноустановлена тем или иным способом. Ø Титрант – раствор реагента или определяемого вещества, объем которого изменяется в процессе титрования и точно фиксируется в точке эквивалентности. Ø Кривая титрования – график зависимости изменения параметров титруемого раствора от объема израсходованного титранта(Vт-та), например, при измерении кислотности среды: рН = f(Vт-та); потенциала системы: Е = f(Vт-та), где f - знак функциональной зависимости измеряемого параметра. Ø Конец титрования – это реально фиксируемый каким-либо методом момент окончания реакции. Он близок, но не точно совпадает с точкой эквивалентности. Чем ближе фиксируемый конец титрования к точке эквивалентности, тем точнее титрование (меньше погрешность). Ø Точка эквивалентности (стехоиметричности), обозначаемая Т.Э. или Е – это теоретически рассчитанный момент титрования, когда реагент и определяемый компонент взяты в стехиометрических количествах. Ø Титрование - это такой процесс, когда раствор титранта добавляют в титруемую пробу малыми порциями до момента фиксации окончания реакции (точке эквивалентности). Ø Показатель титровании (рТ) – это значение, при котором заканчивается титрование с данным индикатором при правильном его подборе. При этом показатель титрования должен быть как можно ближе к середине интервала перехода индикатора, т.е. к значению рК. Вид параметра рТ определяется типом индикатора (рТ = рН; рЕ). Ø Показатель индикатора (рК) – это значение, которое соответствует середине интервала перехода индикатора и рассчитывается через его константу (диссоциации, устойчивости и т.д.). Все расчеты в титриметрии основываются на законе эквивалентов и выполняются, исходя из объема титранта, измеренного в точке конца реакции, хотя на практике вместо «конец реакции» обычно употребляют термин «точка эквивалентности». Это удобнее, однако, смешивать по сути понятия «конец реакции» и «точка эквивалентности» нельзя. Одина из главных причин погрешности титриметрического метода заключается в несовпадении фиксируемого конца реакции и реальной точки эквивалентности. В основе титриметрических определений лежит химическая реакция между титруемым раствором и титрантом, но далеко не любая химическая реакция пригодна для ее использования в титриметрии. Их выбор обусловлен следующими требованиями: Ø реакция должна идти количественно, т.е. быть необратимой (Креак.>>1); Ø остаточная концентрация титруемого вещества в Т.Э. не может превышать 10-6 моль/л; Ø должен существовать способ точной фиксации точки эквивалентности (конца реакции) - визуальный или инструментальный; Ø скачок и Т.Э. - четко фиксируются и находятся в узком интервале расхода титранта (обычно 1- 2 капли); Ø отсутствуют сопряженные реакции, влияющие на ход кривой титрования и положение Т.Э.; Ø скорость реакции достаточно высока, чтобы исключить перетитровывания раствора. Отбор пробы для титрования (аликвоты) осуществляют пипеткой Мора, а расход титранта фиксируют по шкале бюретки в момент окончания реакции. Точность выполненных определений во многом зависит от правильности обращения с пипеткой Мора (рис. 4.5) и бюреткой (рис. 4.6). Особенно это касается измерения объемов. Объем будет определен правильно, если отсчет проводится по центральной части нижнего края мениска, расположенного на уровне глаз (рис. 4.5 и 4.6)
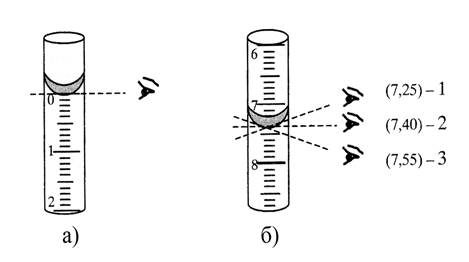
Рисунок 4.5 – Определение объема раствора при работе с пипеткой Мора (а) и перенос аликвоты (снятие последней капли) в колбу для титрования (б).
Рисунок 4.6 – Положение глаз при отсчете объема по бюретке: а – определение нулевого положения перед началом титрования; б – определение объема израсходованного титранта: 1 и 3 – неправильное положение глаз: объем раствора или занижен (1), или завышен (3); 2 – правильное положение глаз при отсчете.
Титрование в лаборатории при визуальной фиксации точки эквивалентности выполняют на установке, показанной ниже на рисунке 4.6. Существуют два варианта проведения титриметрического анализа, обусловленные методикой отбора титруемой пробы: метод пипетирования и метод отдельных навесок. Они отличаются точностью и трудоемкостью. Метод пипетирования (рис. 4.5) заключается в отборе аликвотных частей (аликвот) титруемого раствора из мерной колбы с помощью пипеток Мора. Обычно отбирают и титруют аликвоты до получения не менее 3-хсходящихся результатов. Метод прост, экспрессен, но уступает в точности методу отдельных навесок. Метод отдельных навесок состоит во взвешивании на аналитическихвесах рассчитанной массы навески вещества, необходимой для каждого титрования, которые не должны значительно отличаться. Навески количественно переносят в колбы для титрования, растворяют примерно равными объемами воды и титруют. Титрование выполняю до получения не менее 3-х сходящихся значений по содержанию вещества.
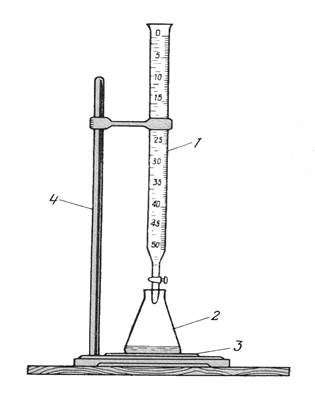
Рисунок 4.6 – установка для титрования: 1 – бюретка с раствором титранта; 2 – колба с титруемым раствором; 3 – белая плитка или лист белой бумаги; 4 – штатив с лапками.
|
||||
|
Последнее изменение этой страницы: 2017-01-19; просмотров: 1592; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.119 (0.007 с.) |