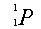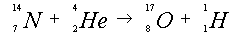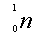Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Метод толстослойных фотоэмульсийСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
В России был создан еще один метод наблюдения за радиоактивными различными частицами, распадами, реакциями. Это метод толстослойных фотоэмульсий. Частицы попадают в эмульсии, приготовленные определенным образом. Взаимодействуя с частицами эмульсий, они не просто создают треки, но треки, которые уже сами по себе представляют фотографию, которую мы получаем, когда фотографируем треки в камере Вильсона или в пузырьковой камере. Это гораздо удобнее. Но и здесь есть один важный недостаток. Чтобы фотоэмульсионный метод работал довольно долгое время, должно происходить постоянное проникновение, попадание образовавшихся новых частиц или излучений, т.е. регистрировать кратковременные импульсы таким способом проблематично. Другие методы регистрации частиц Можно говорить и о других методах: например, есть такой метод, как искровая камера. Там в результате протекания радиоактивных реакций по следу движения частицы образуются искры. Их тоже хорошо видно и легко регистрировать. На сегодняшний день чаще всего используют полупроводниковые датчики, которые и компактны, и удобны, и дают достаточно хороший результат. Заключение О том, какие же открытия удалось сделать при помощи описанных выше методов, мы поговорим на следующем уроке. Список дополнительной литературы 1. Боровой А.А. Как регистрируют частицы (по следам нейтрино). «Библиотечка “Квант”». Вып. 15. М.: Наука, 1981 2. Бронштейн М.П. Атомы и электроны. «Библиотечка “Квант”». Вып. 1. М.: Наука, 1980 3. Кикоин И.К., Кикоин А.К. Физика: Учебник для 9 класса средней школы. М.: «Просвещение» 4. Китайгородский А.И. Физика для всех. Фотоны и ядра. Книга 4. М.: Наука 5. Мякишев Г.Я., Синякова А.З. Физика. Оптика Квантовая физика. 11 класс: учебник для углубленного изучения физики. М.: Дрофа
Тема: Строение атома и атомного ядра. Использование энергии атомных ядер Урок 55. Открытие протона. Открытие нейтрона Ерюткин Евгений Сергеевич Открытие протона Удивительная история случилась в самом начале ХХ века. Именно тогда были открыты две важнейшие частицы, из которых состоят все ядра химических элементов – протон и нейтрон. Протон Начнем по порядку – с протона. Как известно, протон был открыт в 1919 г. Э. Резерфордом. Мы знаем, что в 1911 г. уже состоялся опыт Резерфорда по определению строения атома. А в 1913 г., т.е. через 2 года после своего знаменитого эксперимента, Резерфорд выдвинул очень важную идею. Он предложил считать, что в состав любого ядра, т.е. всех химических элементов, в ядре любого химического элемента находится водород. На чем основывались его такие размышления? Уже был определены характеристики ядер водорода. Была известна масса, был известен заряд ядра водорода. Оказалось, что массы химических элементов делятся на массу водорода без остатка. Таким образом, Резерфорд сделал заявление, что, по всей вероятности, внутри любого ядра находится то или иное количество атомов водорода. Но любая теория должна подтверждаться обязательно экспериментом. Такой эксперимент состоялся в 1919 г., именно тогда и был открыт протон. В своем эксперименте Резерфорд использовал a-частицы. Их Резерфорд направил на ядра азота. В результате этого эксперимента были получены два каких-то химических элемента. Один из них был отождествлен – кислород, а второй, по всей вероятности, являлся водородом. Обращаю ваше внимание: уверенности здесь не было. Почему? Резерфорд использовал в своем эксперименте метод, о котором мы уже говорили на предыдущем уроке, – метод сцинтилляций, когда попадающая частица дает вспышку. По результатам таких экспериментов он судил о том, что там есть какая-то частица, соответствующая атому ядра водорода.
Рис.1. Результат бомбардировки a-частицами ядер азота: образовались кислород и частица, тождественная ядру водорода
Эту частицу, ядро водорода, он назвал протоном (от греч. «протос» – «первый»). Когда этот эксперимент повторили, но уже в камере Вильсона, причем эта камера находилась в магнитном поле, то уже не было никаких сомнений: открыта новая частица – протон. Итак, протон является ядром атома водорода. Давайте посмотрим на эту первую искусственную ядерную реакцию. Ставится буква Р, внизу отмечается порядковый номер 1, как у водорода. И массовое число ставится 1, т.е. по оценке уже тогда, когда были проведены исследования в камере Вильсона, ясно стало, что масса протона приблизительно соответствует 1 атомной массе. Обратите внимание на реакцию. Реакция происходила следующим образом: Азот, порядковый номер 7 и массовое число 14, обстреливался a-частицами. Мы знаем, что a-частицы – это ядра атома гелия с порядковым номером 2 и с массовым числом 4. В результате такой реакции образовались два новых ядра. Два совершенно новых элемента. Первое ядро – это ядро, соответствующее атому кислорода, с порядковым номером 8 и массовым числом 17. И та частица, ядро атома водорода, которое мы теперь можем смело назвать протоном. Итак, ядро атома водорода и протон – это одно и то же, были открыты в 1919 г. по сути своей в опытах Резерфорда. Открытие нейтрона Нейтрон Следующий этап в развитии строения ядра атома был связан с именем Чедвика. Это ученик Резерфорда. Именно ему удалось в 1932 г. открыть нейтрон. Обнаружить нейтрон было гораздо сложнее, ведь нейтрон – электрически нейтральная частица, как мы уже знаем. В 1930 г. двое немецких ученых, Боте и Беккер, в результате опытов обнаружили, что при облучении a-частицами бериллия образуется какое-то неизвестное излучение. После открытия Резерфордом протона, многие ученые направили свои помыслы и силы на то, чтобы провести ядерные реакции, искусственные ядерные реакции. При помощи a-лучей стали облучать многие элементы, наблюдая за реакцией. Вот и немецкие ученые в 1930 г., облучая бериллий, получили неизвестное излучение. Вначале это излучение решили отождествить с g-лучами. Они распространялись вдоль прямой, не отклонялись в электрическом и магнитном полях, обладали большой энергией и высокой проникающей способностью. В дальнейшем при изучении других реакций стало ясно, что такие же лучи образуются, когда a-лучами обстреливают бор и некоторые другие химические элементы. Сравнивая химические элементы, полученные в результате такого рода реакций, поняли, что данные лучи не являются никакими лучами (g-лучами уж точно не являются, поскольку обладают более высокой проникающей способностью энергией по сравнению с g-лучами).
Рис. 2. Джеймс Чедвик
Свойства нейтрона В 1932 г. Чедвик предположил, что это какая-то новая частица, которая не обладает электрическим зарядом. Именно этим объясняются все ее свойства: она хорошо проникает через преграды, потому что не взаимодействует с ядрами. Такую новую частицу назвали нейтрон (т.к. он электрически нейтрален). Давайте посмотрим на обозначения этой частицы и обсудим ее свойства. Обозначение нейтрона следующее: Поскольку у нейтрона нет заряда, то 0 ставится внизу, где пишется зарядовое число, а вот массовое число у него равно 1. Масса нейтрона почти равна, но чуть больше массы протона. Поэтому тоже было решено ставить в массовом обозначении число, равное 1. Заключение Теперь можно смело говорить о том, что нейтрон и протон составляют ядро атома. Но о том, какова модель ядра атома, что она собой представляет, мы поговорим на следующем уроке.
|
||||
|
Последнее изменение этой страницы: 2016-12-12; просмотров: 2004; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.21.244.240 (0.006 с.) |