Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Методы получения сопряженных диеновСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Основной метод получения сопряженных диенов – дегидрирование алканов и алкенов, выделяемых их нефти путем фракционной перегонки:
Химические свойства сопряженных диенов Для сопряженных диенов известны все реакции, характерные для алкенов. Однако их поведение отличает ряд особенностей. В реакциях электрофильного присоединения сопряженные диены более активны, чем алкены, так как реакции присоединения к ним электрофилов протекают через образование термодинамически стабильных карбокатионов аллильного типа. 1,3-Бутадиен взаимодействует с бромом, давая смесь продуктов 1,2- и 1,4-присоединения:
Образование двух разных продуктов присоединения объясняет механизм реакции:
Аналогично протекает присоединение галогеноводородов к сопряженным диенам. При этом соблюдается правило Марковникова:
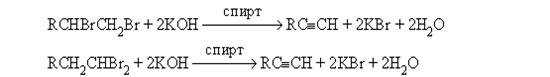
А л к и н ы Алкины – углеводороды состава CnH2n-2, содержащие одну тройную связь углерод – углерод. Методы получения
Химические свойства Химические свойства алкинов определяются наличием связи С≡С, для которой характерны реакции присоединения электрофильных и нуклеофильных реагентов. Алкины с концевой тройной связью вступают в реакции замещения водорода при тройной связи, который обладает слабыми кислотными свойствами. Таким образом, молекулы алкинов содержат два основных реакционных центра – связь С≡С и подвижный водород:
Реакции присоединения по С≡С связи В реакциях электрофильного присоединения алкины менее реакционноспособны, чем алкены. Присоединение галогенов Ацетилен в присутствии катализатора FeCl3 присоединяет 2 моля хлора. Реакция протекает в две стадии:
Присоединение галогеноводородов Ацетилен присоединяет HCl только в присутствии катализаторов, содержащих соли ртути(II):
Присоединение второй молекулы HCl происходит без катализатора по правилу Марковникова: CH2=CHCl + HCl →CH3CHCl2 Замещенные ацетилены более реакционноспособны и присоединяют галогеноводороды согласно правилу Марковникова:
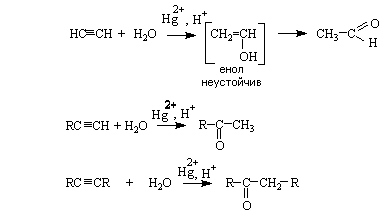
Присоединение воды В кислой среде в присутствии солей ртути(II) алкины взаимодействуют с водой с образованием карбонильных соединений. На первой стадии алкины присоединяют воду в соответствии с правилом Марковникова. Образующиеся при этом ненасыщенные спирты (енолы) неустойчивы, и в условиях реакции быстро изомеризуются в карбонильные соединения. При этом только в случае ацетилена образуется альдегид, а его гомологи дают кетоны:
Реакции с участием подвижного водорода Атом водорода, связанный с атомом углерода, находящемся в состоянии sp-гибридизации, обладает кислотными свойствами и может отщепляться в виде протона под действием сильных оснований:
Равновесие реакции смещено в сторону более слабой кислоты – аммиака Алкены с концевой тройной связью реагируют с солями тяжелых металлов, давая нерастворимые ацетилениды: RC≡ CH + [Ag(NH3)2]OH →RC≡ CAg ↓ + 2 NH3 + H2O RC≡ CH + [Сu(NH3)2]Сl → RC≡ CCu ↓ + NH4Cl + NH3 Реакции используются как качественные на концевую тройную связь. Лекция 8 АРЕНЫ
Арены – это углеводороды, содержащие одно или несколько бензольных ядер. К ним относятся: бензол и его гомологи:
Методы получения
В реакцию вступают алканы, содержащие в цепи не менее шести атомов углерода.
Гомологи бензола могут быть получены также из бензола и его производных (см. алкилирование бензола, реакция Вюрца). Химические свойства Химические свойства ароматических соединений определяются наличием системы делокализованных π -связей. Присутствие π -электронной системы обусловливает основные свойства аренов и их взаимодействие с электрофильными реагентами. Повышенная термодинамическая стабильность ароматического кольца делает предпочтительными реакции замещения, в которых ароматическая система сохраняется. Как следствие этого, наиболее характерными для ароматических соединений являются реакции электрофильного замещения. Известны также реакции радикального галогенирования и окисления боковых цепей алкилбензолов, которые протекают по наиболее реакционноспособному бензильному положению. Процессы, в которых разрушается стабильная ароматическая система, мало характерны и протекают в жестких условиях.
|
||||||
|
Последнее изменение этой страницы: 2016-09-18; просмотров: 496; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.190.153.90 (0.011 с.) |