Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Свойства кристаллических решетокСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Продолжение табл. З4
Кристаллы по величине электропроводности делятся на три класса: Проводники I рода – электропроводность 104 - 106 (Ом×см)-1–вещества с металлической кристаллической решеткой, характеризующиеся наличием «переносчиков тока» - свободно перемещающихся электронов (металлы, сплавы). Диэлектрики (изоляторы) – электропроводность 10-10-10-22 (Ом×см)-1 – вещества с атомной, молекулярной и реже ионной решеткой, обладающие большой энергией связи между частицами (алмаз, слюда, органические полимеры и др.). Полупроводники – электропроводность 104-10-10 (Ом×см)-1 – вещества с атомной или ионной кристаллической решеткой, обладающие более слабой энергией связи между частицами, чем изоляторы. С ростом температуры электропроводность у полупроводников возрастает (серое олово, бор, кремний и др.)
5.2. Контрольные вопросы и задания
1. Охарактеризуйте двойственную природу электрона, уравнение де Бройля, принцип неопределенности Гейзенберга, волновое уравнение Шредингера. 2. Спектры атомов, как источник информации об их строении. Квантовые числа. 3. Основные принципы заполнения электронами орбиталей (принцип Паули, принцип наименьшей энергии, правило Гунда). 4. Электронные формулы и электронно-структурные схемы атомов. 5. Определение валентных возможностей элемента, исходя из строения электронных оболочек атома. 6. Охарактеризовать свойства элемента по его положению в ПСЭ. 7. Физическая сущность химической связи. Типы химической связи, ее характеристика: энергия, длина направленность. 8. Основные положения МВС и ММО. Связывающие и разрыхляющие МО. Кратность связи в ММО. 9. Типы ковалентной связи. Свойства ковалентной связи: насыщаемость, полярность, поляризуемость, направленность, гибридизация. Пространственное расположение атомов в молекуле. Кратность и делокализация связи. 10. Ионная связь, ее характеристики. Общая характеристика металлической связи, водородной связи, межмолекулярных взаимодействий. 11. Характеристика агрегатного состояния веществ.
Примеры решения задач Пример 1. Запишите полный набор квантовых чисел для электрона, который находится последним в орбитальной диаграмме атома азота. Решение. Этот электрон характеризуется набором квантовых чисел: n = 2 (находится на 2-м уровне), l = 1(находится на p-подуровне), m = +1 (находится на последней из трех одинаковых p-орбиталей, s = +1/2 (этот электрон заселился первым на данную p-орбиталь).
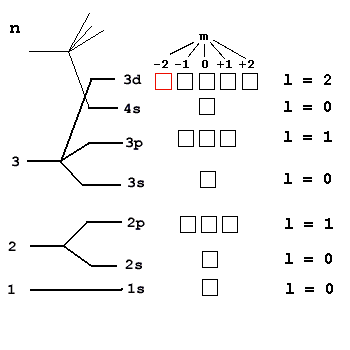
Пример 2. Последним электронную оболочку некоего элемента заселяет электрон с набором квантовых чисел: n = 3, l = 2, m = -2, s = +1/2. Какой это элемент? Какова его полная электронная формула? Решение. Данный электрон находится на 3-м уровне (n = 3), причем на d-подуровне (l = 2). На рис. 20 изображены все пять d-орбиталей и расположены над ними значения магнитного квантового числа m от -2 до +2, нужная орбиталь (m = -2). Расположив на ней единственный электрон (стрелка вверх, т.к. s = +1/2) и зная, что он последний, мы приходим к выводу, что остальные d-орбитали пусты. Теперь мы уже можем записать сокращенную электронную формулу элемента: …3d1. Этот элемент легко найти в периодической таблице - это скандий 21Sc. Всего на орбитальной диаграмме элемента поместится ровно 21 электрон, следовательно, в его ядре 21 протон и его порядковый номер в таблице Менделеева тоже 21 (Sc). Орбитальная диаграмма помогает записать и полную электронную формулу для скандия: 1s2 2s2 2p6 3s2 3p6 4s2 3d1.
Рис. 20. Графическое изображение орбиталей
Пример 3. Элемент имеет порядковый номер 18. Напишите полную электронную формулу, указав, на каких энергетических уровнях и подуровнях находятся электроны в атомах этого элемента. Решение. Заполнение электронами энергетических уровней и подуровней происходит в порядке возрастания энергии 1 s <2 s <2 p <3 s <3 p <4 s ≈3 d <4 p <5 s ≈4 d <5 p <6 s ≈4 f ≈5 d <6 p <7 s ≈5 f ≈6 d <7 p. Порядковый номер 18, т.е. атом содержит 18 электронов, его электронная формула имеет вид: 1s22s22p63s23p6, это аргон. Пример 4. Сокращенная электронная формула элемента изображена в виде … 3d34s2. Какой это элемент? Напишите полную электронную формулу. Решение. Исходя из строения электронной оболочки, элемент находится в 4-м периоде, общее число валентных электронов (3d34s2) – пять, следовательно, в V группе, d-орбиталь незавершенна, это d-элемент V группы побочной подгруппы. Это ванадий 23V. Электронная формула этого элемента: 1s22s22p63s23p64s23d3. Пример 5. На основании ПСЭ охарактеризуйте химические свойства атома с порядковым номером 21 по плану.
План характеристики элемента по положению
|
||||||||||||||||
|
Последнее изменение этой страницы: 2016-08-26; просмотров: 439; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.14.86.70 (0.01 с.) |