
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Теория электролитической ионизации (диссоциации).Содержание книги
Поиск на нашем сайте
Электролитическая ионизация в растворе – это распад вещества на сольватиованные (гидратированные) ионы под действием молекул растворителя. Данная теория была разработана шведским ученым Сванте Аррениусом в 1887 г. Основные ее положения: 1. Вещества распадаются на положительные и отрицательно заряженные ионы под действием растворителя. 2. Под дейсвием электрического тока положительно заряженные ионы двигаются к катоду (-) и называются катионами, а отрицательно заряженные двигаются к аноду (+) и называются анионами. 3. Диссоциация – процесс обратимый, наряду с распадом молекул протекает процесс соединения ионов в молекулу (молязация).
В своих работах Аррениус доказал, что распад молекул на ионы происходит уже в самом процессе растворения независимо от того, пропускают электрический ток через раствор или нет. Благодаря ионизации увеличивается число частиц в расторе, что ведет к повышению осмотического давления, однако он не учитывал взаимодействие растворенного вещества с растворителем (сольватационные процессы), данный процесс рассматривал как физический. Основоположником современной теории электролитической ионизации как процесса, вызываемого сольватацией молекул, являются И.А. Каблуков и В.А. Кистяковский. Они расширили теорию Аррениуса с позиции химической теории растворов Д.И. Менделеева. Основная причина электролитической ионизации – гидратация (сольватация) ионов, затрудняющая обратное соединение ионов (ассоциацию). Дипольные молекулы воды взаимодействуют с ионами или полярными молекулами в растворе как за счет неподеленных электронных пар атома кислорода, так и за счет образования водородных связей:
Таким образом, катионы связаны с молекулами воды по типу донорно-акцепторного взаимодействия. Доморами являются атомы кислорода молекулы воды, имеющие свободные электронные пары, акцепторами - катионы, имеющие свободные орбитали. Анионы связаны с водой водородной связью. Число координированных молекул воды называется координационным числом. Оно может бытьравно 4,6 и т.д. В общем виде растворение электролита в воде описывает уравнение: КА + (x + у) Н2О ↔ [К(Н2О)х]+ + [А(Н2О)у]- На практике пользуются упрощенным уравнением: КА ↔ К+ + А- Таков механизм ионизации вещества ионного характера, кристаллическая решетка которых состоит из ионов. При растворении в воде или других полярных растворителях соединений с ковалентной полярной связью происходит ионизация по типу:
Аналогично идет растворение галогенидов кобальта, алюминия, хрома, марганца,железа, меди и др.: СоCl2 + 6H2O = [Co(H2O)6]2+ + 2Cl- Элементарных ионов кобальта в растворе нет. Часто аквакомплексы оказываются настолько прочными, что выделяются из растворов в составе кристаллогидратов, например: CuSO4·5H2O, AlCl3·6H2O, BeCl2·4H2O. Количественной характеристикой электролитической ионизации является
По степени ионизации условно электролиты делятся на сильные (α>30%), средние (30% >α > 3%) и слабые (α<3%). Степень ионизации можно вычислить, если найти опытным путем изотонический коэффициент Вант-Гоффа:
n- общее количество ионов на которые распадается электролит Из сказанного выше следует, что растворы будут изотоничны, если при одинаковой температуре содержат одинаковое число частиц в еденице объема. У растворов с одинаковой молярной концентрацией осмотической давление выше в растворе электролита, с более высоким значением α. У растворов электролитов с одинаковыми СМ и α осмотическое давление выше у раствора электролита, диссоциирующего на болшее число частиц. Факторы, влияющие на степень ионизации: 1. Природа растворителя 2. Природа растворенного вещества 3. Температура (ионизация – это эндотермический процесс, поэтому с повышением температуры ионизация увеличивается). 4. Концентрация (с увеличением концентрации уменьшается степень ионизации и наоборот). 5. Наличие одноименных ионов уменьшает степень ионизации. К равновесиям в растворе слабого электролита применимы законы химического равновесия:
Киониз. - константа ионизации зависит от природы электролита и растворителя, от температуры и не зависти от концентрации. Это постоянная величина (прилож. 7) характеризует способность электролита распадаться на ионы. Чем больше Киониз., тем лучше вещество распадается на ионы. Для сильных электролитов Киониз >1 рКиониз = -lgКиониз (67) Взаимосвязь константы ионизации и степенью ионизации выражает закон разбавления Оствальда:
Для слабых электролитов, в очень разбавленных растворах:
Степень ионизации слабого электролита возрастает с разведением раствора. Ионизации подвергаются не только молекулы, но и сложные ионы. При ступенчатой ионизации кислот и оснований каждая ступень характеризуется собственной константой: Н3РО4 ↔Н+ + Н2РО4- Н2РО4- ↔ Н+ + НРО42- НРО42- ↔ Н+ + РО43- Общая Киониз = К/ион. · К//ион· К///ион. Поскольку К/ион. > К//ион > К///ион, в наибольшей степени идет ионизация по первой ступени. Электролиты – вещества, расплавы и растворы которых содержат подвижные ионы и проводят электрический ток. К сильным электролитам, если растворителем является вода относятся: все соли, сильные кислоты (соляная, бромоводородная, йодоводородная, хлорная, серная, азотная), основания (гидроксиды лития, натрия, калия, рубидия, цезия, кальция, бария). Данные вещества в растворах полностью диссоциируют на ионы. Однако экспериментально было доказано, что не все ионы, образовавшиеся в результате полной диссоциации электролита, являются свободными (электрическая проводимость растворов электролитов, которая связана с движением ионов, в концентрированных растворах оказалась незначительной). Это говорит о том, что в них ионы движутся медленнее, чем в разбавленных. Это обусловлено электростатическим взаимодействием между ионами и зависит от концентрации раствора, природы электролита и среды. Наличие этих сил приводит к тому, что каждый ион окружен «ионной атмосферой», состоящей из ионов с противоположным знаком (сложные агрегаты – ассоциаты). Движение положительных ионов в сторону отрицательного электрода тормозится силами притяжения отрицательно заряженной «ионной атмосферы» к положительному электроду (рис. 30). При разбавлении это взаимодействие ослабевает, подвижность ионов возрастает (максимальна при бесконечном разбавлении раствора).
Активность – это условная
Для сильно разбавленных растворов она равна концентрации. F – коэффициент активности, характеризует межионные взаимодействия. Чем они сильнее, тем меньше коэффициент, тем больше отличаются активность и концентрация. Это безмерная величина, характеризует степень отклонения свойств данного раствора от свойств идеального (если раствор разбавлять, то Сила взаимодействия между ионами – F- зависят от: концентрации ионов и заряда. Эти факторы учитываются величиной – ионной силой раствора (I) – полусумма произведений концентраций всех ионов в растворах на квадрат их заряда:
Для сильно разбавленных растворов коэффициент активности (в приложении 7.) зависит только от ионной силы. Согласно теории сильных электролитов Дебая-Гюккеля (1923 г), коэффициент активности электролита связан с ионной силой раствора следующим соотношением:
А – коэффициент, зависит от заряда иона, диэлектрической проницаемости среды и температуры. Согласно теории электролитической диссоциации Аррениуса кислота – это соединение, распадающееся в водном растворе с образованием ионов Н+, а основание – вещество, при диссоциации которого образуются ионы ОН-. Эти определения являются весьма упрощенными, поскольку относятся только к водным растворам (кислотно-основные свойства проявляются в разных растворителях и даже при их отсутствии). Многие вещества не содержат в своем составе гидроксильных групп, и тем не менее являются основаниями. В данном процессе диссоциации не учитываются молекулы растворителя. В развитии представлений о кислотах и основаниях появляется протеолитическая теория Бренстеда –Лоури (1923г). Согласно этой теории кислота – вещество, которое может отщеплять протоны, а основание – вещество, присоединяющее протоны.
ацетет ион – основание хлорид ион – основание, более слабое. Следовательно, хлороводород – сильный электролит. В каждом примере есть кислота и основание, которые называются сопряженными.
Протолитическое, или кислотно-основное, равновесие устанавливается в результате конкуренции за протон между основаниями взаимодействующих сопряженных кислотно-основных пар (НА, А- и ВН+, В). Протолитическое равновесие всегда смещается в сторону образования более слабой кислоты: НА + В ↔ А- + ВН+
pKa(HA) + pKb(А-)= 14 pKa(ВH+) + pKb(B) = 14 Согласно протеолитической теории сила кислот и оснований зависят от природы растворителя. Так, если в качестве растворителя хлороводорода вместо воды взять безводную уксусную кислоту (более слабое основание, чем вода), то равновесие не будет полностью смещено вправо, т.е. хлороводород - слабая кислота.
Наоборот, если уксусную кислоту растворить не в воде, а в жидком аммиаке (более сильное основание чем вода) диссоциация уксусной кислоты существенно увеличится.
По Льюису кислотами являются: Н+, Аl3+, BF3, основаниями – Н2О, NH3, Cl- (рис. 31).
Рис. 31. Кислоты и основания Льюиса. 8.2. Контрольные вопросы и задания 1. Учение о растворах. Раствор, растворитель, растворенное вещество, растворимость. 2. Гидратная теория растворов Д.И. Менделеева. 3. Сущность явления осмоса. Осмотическое давление. Закон Вант-Гоффа. 4. Изо-, гипо-, гипертонические растворы. Плазмолиз, тургор, гемолиз. 5. Роль осмотического давления в биологических системах. 6. Основные положения теории электролитической диссоциации С. Аррениуса и ее развитие И.А. Каблуковым. 7. Состояние ионов в водных растворах. Гидратация ионов, образование аквакатионов, сольватация. 8. Степень ионизации. Факторы, влияющие на степень ионизации. 9. Изотонический коэффициент. Константа ионизации. 10. Взаимосвязь степени и константы ионизации.Закон разбавления Оствальда. 11. Понятие об активности. Кислоты и основания по Бренстеду-Лоури и Льюису.
Примеры решения задач Пример 1. Вычислите осмотическое давление раствора, содержащего 16 г сахарозы С12Н22О11 в 350 г воды при 293 К. Плотность раствора считать равной 1. Решение. Находим массу раствора: 16 + 350 = 366 г Поскольку плотность равна 1 г/см3, то объем раствора равен 366 см3 = 0,366 дм3. Находимо осмотическое давление раствора:
Пример 2. В 250 см3 раствора содержится 2,3 г растворенного вещества. Осмотическое давление при 27 0С равно 249 кПа. Вычислите молярную массу вещества. Решение. V = 0,25 дм3; Т = 27+273 = 300 К
Пример 3. При 0 0С осмотическое давление 0,1 н раствора карбоната калия равно 272,6 кПа. Определите кажущуюся степень ионизации соли. Решение. Находим молярную концентрацию 0,1 н раствора К2СО3 (fЭ = ½): 0,1 · ½ = 0,05 моль/л. Находим изотонический коэффициент для раствора соли (сильный электролит): К2СО3 ↔ 2К+ + СО32-, следовательно n = 3 Кажущуюся степень ионизации находим из соотношения: Пример 4. При 20 0С осмотическое давление раствора, в 100 мл которого содержится 6,33 г красящего вещества крови – гематина, равно 243,4 кПа. Определите молекулярную формулу, если известен элементарный состав (в %) гематина: С – 64,6; Н – 5,2; N – 8,8; О – 12,6; Fe – 8,8. Решение. Находим молярность раствора: Определяем молекулярную массу гематина: в 1 л раствора содержится 63,3 г гематина, это 0,1 моль. Таким образом, молярная масса гематина равна 63,3/0,1 = 633 г/моль. Находим простейшую формулу гематина: С:Н:N:О:Fe = Простейшая формула гематина: С34Н33N4O5Fe. Этой формуле соответствует молекулярная масса 633 г/моль, что совпадает с найденным выше значением. Таким образом, искомая молекулярная формула гематина С34Н33N4O5Fe. Пример 5. Вычислите [H+], [HS-], [S2-] в 0,1 М растворе H2S. Решение. Поскольку диссоциация сероводорода протекает преимущественно по первой ступени, то концентрацией [H+], образующихся при диссоциации по второй ступени, можно пренебречь и считать, что [H+] = [HS-] = К2 – константа диссоциации по второй ступени – табл. величина).
Пример 6. Вычислите концентрацию ионов водорода в 0,1 М растворе хлорноватистой кислоты (Ка = 5 · 10-8). Решение. Находим степень диссоциации хлорноватистой кислоты: Пример 7. Степень диссоциации уксусной кислоты в 0,1 М растворе равна 1,32 · 10-2. найдите константу диссоциации кислоты и значение рКа. Решение. Подставляем данные задачи в уравнение закона разбавления Оствальда: Пример 8. Вычислите ионную силу и активность ионов в растворе, содержащем 0,01 моль/л MgSO4 и 0,01 моль/л MgCl2. Решение. Определяем ионную силу раствора:
Находим коэффициенты активности ионов по формуле:
Находим активность каждого иона по формуле, а = f · См: a(Mg2+) = 0,02 · 0,3 = 0,006 моль/л; a(SO42-) = 0,01 · 0,3 = 0,003 моль/л; a(Cl-) = 0,02 · 0,74 = 0,0148 моль/л. 8.4. Индивидуальные задания Задание. Решите задачи своего варианта (табл. 48). Таблица 48 Варианты контрольного задания
Продолжение табл. 48
Продолжение табл. 48
Продолжение табл. 48
Окончание табл. 48
8.5. Тестовые задания 1. Название растворов, имеющих одинаковое осмотическое давление: а) гипертонические в) изотонические б) гипотонические г) пропорциональные 2. Оба вещества неэлектролиты: а) бензол, сахароза в) нитрат натрия, нитрат кальция б) хлорид натрия, глюкоза г) глюкоза, серная кислота 3. Оба вещества электролиты: а) бензол, сахароза в) нитрат натрия, нитрат кальция б) хлорид натрия, глюкоза г) глюкоза, серная кислота 4. Процесс, вызывающий набухание в клетке: а) плазмолиз в) гемолиз б) тургор г) гидратация 5. Формула определения осмотического давления неэлектролита: а) π = iСМRT в) π = МRT б) π = СМRT г) π = imRT 6. Гипертонический раствор: а) Росм> Росм в клетке в) Росм = Росм в клетке б) Росм< Росм в клетке г) Росм = iCMRT 7. Название отношения числа ионизированных молекул к их общему числу …….. 8. Взаимосвязь константы ионизации и степени гидролиза выражает закон: а) Вант-Гоффа в) Аррениуса б) Оствальда г) Каблукова 9. Название условной концентрации, соответственно которой электролит действует в химических реакциях …….. 10. Гипотонический раствор: а) Росм> Росм в клетке в) Росм = Росм в клетке б) Росм< Росм в клетке г) Росм = iCMRT ТЕМА 9. ГЕТЕРОГЕННЫЕ РАВНОВЕСИЯ И ПРОЦЕССЫ. ПРОИЗВЕДЕНИЕ РАСТВОРИМОСТИ, УСЛОВИЯ ОБРАЗОВАНИЯ И РАСТВОРЕНИЯ ОСАДКОВ Теоретические сведения Количество растворенного вещества, необходимое для получения насыщенного раствора в заданном количестве растворителя определяет растворимость этого вещества в данном растворителе. Растворимость – с одной стороны характеризует способность вещества растворяться, определяемую природой вещества и растворителя, температурой и др. факторами, с другой – это количественная характеристика насыщенного раствора в единицах концентрации: моль/дм3 , г/100 г растворителя. Наиболее распространенным растворителем на нашей планете является вода. В воде различают: практически нерастворимые вещества – стекло, металлы, фосфаты Ca и Zn, AgCl, BaSO4, керосин, растительное масло, инертные газы и др.; малорастворимые – гипс,PbSO4 , многие гидроксиды и соли, CH4, O2, N2, бензол, анилин и др.; хорошо растворимые – сахар, хлориды и нитраты щелочных металлов, ацетон, этиловый спирт, NH3,HCl и др (приложение 8). Чем ближе природа веществ, тем лучше они растворяются друг в друге, то есть выполняется эмпирическое правило «подобное растворяется в подобном». Растворимость (S) – способность вещества посылать в раствор свои ионы, это молярность его насыщенного раствора. Абсолютно нерастворимых веществ нет. Определяется концентраций вещества в насыщенном растворе:
S = Например: осадок Ca3(PO4)2 = 3Ca2+ + 2PO43- S(Ca3(PO4)2) = 3S(Ca2+) + 2S(PO43-) S(Ca3(PO4)2) = Считается что малорастворимые соли могут переходить в раствор только в виде ионов. Раствор, находящийся в равновесии с осадком называется насыщенным. При контакте малорастворимого сильного электролита с водой образуется насыщенный раствор – термодинамически устойчивая равновесная система, в которой скорость растворения вещества равна скорости его выделения из раствора (рис. 32): uраств.= uос. AgCl↔ Ag+ + Cl- Применяем закон действующих масс:
Рис. 32. Насыщенный раствор AgCl. Так как Кр и концентрация твердого вещества не изменяется:
В общем случае для малорастворимого электролита KtnAnm произведение растворимости (ПР) определяется стехиометрическим произведением концентраций ионов, находящихся в равновесном (насыщенном) растворе: KtnAnm ↔ nKtm+ + mAnn- осадок раствор
ПР = [Ktm+]n∙[Ann-]m (76) Правило Нернста. ПР - в насыщенном растворе малорастворимого сильного электролита это произведение концентраций его ионов есть величина постоянная при данной температуре. Произведение растворимости зависит от природы малорастворимого электролита, от природы растворителя и температуры. Это количественная характеристика растворения. Чем больше ПР, тем больше растворимость. ПР можно найти зная растворимость. Значения ПР приводятся в справочной литературе (приложение 9). В случае сильного электролита оперируем понятием активности («эффективной концентрации»): a = f∙c
ПР0 = a n (Ktm+) ∙a m (Ann-) = f(Ktm+)∙ f(Ann-)∙ ПР0 (77) где f (или¡) – коэффициенты активности, значение которых приближается к единице при сильном разбавлении. Следовательно, в разбавленных растворах ПР0= ПР. Зависимость ПР от температуры при p,T = const описывается изобарой химической реакции:
Изотерма химического равновесия для гетерогенной системы: ΔsG = -RTln ПР+ RTln[Ktm+]n[ Ann-]m (79)
где [Ktm+]n[ Ann-]m - произведение неравновесных концентраций. Когда [Ktm+]n[ Ann-]m < ПР происходит растворение осадка (раствор ненасыщен); [Ktm+]n[ Ann-]m > ПР идёт процесс образования осадка (раствор пересыщен); [Ktm+]n[ Ann-]m = ПР система находится в равновесном состоянии (раствор насыщен). Равновесием в насыщенном растворе можно управлять. Условия смещения гетерогенного равновесия:
AgCl↔ Ag+ + Cl-
Чтобы растворить осадок надо один из ионов вывести из раствора или один из ионов связываем с образованием: 1. малодиссоциирующего вещества 2. комплекснгого соединения 3. менее растворимого соединения
AgCl↔ Ag+ + Cl-
Чтобы осадок выпадал полнее (уменьшить растворимость) надо ввести одноименные ионы. Осаждение труднорастворимого электролита производится в избытке осадителя. Таким образом, в присутствии избытка одноименных ионов растворимость малорастворимого вещества понижается, и осаждение будет более полным. Малорастворимое вещество выпадает в осадок, если произведение реальных концентраций ионов в растворе больше величины произведения растворимости при данной температуре. 9.2. Контрольные вопросы и задания 1. Какие электролиты называются сильными и какие слабыми? 2. Какая пеличина характеризует процесс ионизации труднорастворимых электролитов? 3. Докажите, исходя из закона действующих масс, что ПР – величина постоянная. 4. Рассчитайте растворимость для веществ с молекулами типа: АВ, А2В, АВ3, А2В3, АВ2. 5. Как превратить концентрацию моль/дм3 в г/дм3 и наоборот? 6. Условия образования и растворения осадков.
Примеры решения задач Пример 1. Вычислите растворимость соли PbI2, если ПР = 8 · 10-9. Решение. Растворимость (S) – способность вещества растворяться. Поэтому растворимость определяется концентрацией вещества в растворе:
PbI2 ↔ Pb2+ + 2I-; ПР = [Pb2+]·[I-]2. Тогда ПР = S·(2S)2 = 4S3 S S 2S
Пример 2. Вычислите ПР AgCl, есл
|
|||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-08-26; просмотров: 2579; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.119 (0.012 с.) |

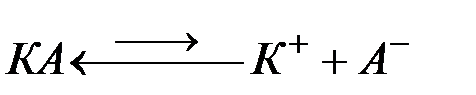


 - степень ионизации. Это отношение числа ионизированных молекул к общему числу:
- степень ионизации. Это отношение числа ионизированных молекул к общему числу: (65)
(65) (66)
(66)
 (68)
(68) (69)
(69)


 Активную (эффективную) концентрацию электролита (количество свободных ионов) называют активностью (Льюис, 1901 г).
Активную (эффективную) концентрацию электролита (количество свободных ионов) называют активностью (Льюис, 1901 г). (70)
(70) и С=а)
и С=а) (71)
(71) (72)
(72)

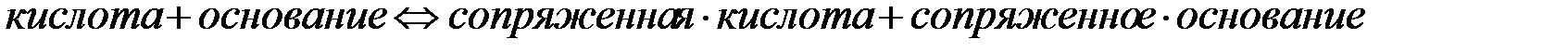 В процессе нейтрализации два основания конкурируют за обладание протонами.
В процессе нейтрализации два основания конкурируют за обладание протонами.

 Почти одновременно с протеолитической теорией Дж. Льюис предложит электронную теорию кислот и оснований. Согласно этой теории основания – соединения, имеющие неподеленные электронные пары и способные их обобществлять с другими молекулами или ионами. Кислоты – вещества, способные акцептировать электронные пары. (В теории Бренседа-Лоури нейтрализация – процесс передачи протона от кислоты к основанию, то здесь – происходит перенос электронной пары – донорно-акцепторное взаимодействие).
Почти одновременно с протеолитической теорией Дж. Льюис предложит электронную теорию кислот и оснований. Согласно этой теории основания – соединения, имеющие неподеленные электронные пары и способные их обобществлять с другими молекулами или ионами. Кислоты – вещества, способные акцептировать электронные пары. (В теории Бренседа-Лоури нейтрализация – процесс передачи протона от кислоты к основанию, то здесь – происходит перенос электронной пары – донорно-акцепторное взаимодействие).
 . Откуда
. Откуда 
 . Откуда
. Откуда 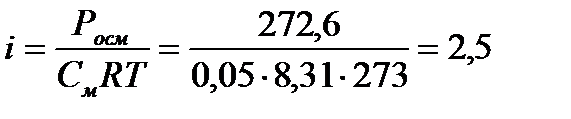 .
.
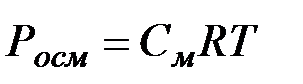 ; Т = 20 + 273 = 293 К;
; Т = 20 + 273 = 293 К;  .
. = 34:33:4:5:1.
= 34:33:4:5:1. =
=  моль/л (К1 – константа диссоциации по первой ступени – табл. величина).
моль/л (К1 – константа диссоциации по первой ступени – табл. величина). . Тогда [S2-] = 1·10-14 моль/л.
. Тогда [S2-] = 1·10-14 моль/л. . Отсюда [Н+] = α · См = 7 · 10-4 · 0,1 = 7 · 10-5 моль/л.
. Отсюда [Н+] = α · См = 7 · 10-4 · 0,1 = 7 · 10-5 моль/л. . Находим рКа = -lg Ka= - lg(1,77 · 10-5) = 5 – lg 1,77 = 5 – 0,25 = 4,75.
. Находим рКа = -lg Ka= - lg(1,77 · 10-5) = 5 – lg 1,77 = 5 – 0,25 = 4,75.

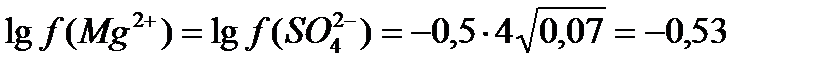 ; f = 0.3
; f = 0.3 ; f = 0,74.
; f = 0,74. (73)
(73) (74)
(74)


 (75)
(75) (78)
(78) моль/дм3.
моль/дм3.


