Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
определение коэффициента расхода воздуха при полном сгорании топливаСодержание книги
Поиск на нашем сайте
42)определение коэффициента расхода воздуха при полном сгорании топлива α опр-ся по извест.сост. сух.прод.сгор. А) полное сгорание *при полн. сгор. тв. Топлив, расход воздуха на горение близок к выходу сух. прод. сгор. -углекислотная ф-ла:α=RO2max /RO2 -кислородная ф-ла: α=21 /(21-O2) *при полн. сгор. жидк. и газов применяются азотные ф-лы -N2<10% : α=N2 /(N2-3.76O2) или α=21 /(21-79О2/N2) -N2>10% :α=(N2-N2г/Vс.г.)/(N2-N2г/Vс.г.-3.76O2) где N2г-объемное % содержание азота в топливе 43)определение коэффициента расхода воздуха при неполном сгорании топлива Неполное сгорание связано с присутствием в прод. сгор. СО,СН4,Н2. Азотные ф-лы в этом случае принимают вид: *N2<10% : α=N2 /(N2-3.76(O2-0.5CО-0,5Н2-2СН4)) или α=21 /(21-79(O2-0.5CО-0,5Н2-2СН4)/(100-(RO2+O2+СО+Н2+СН4)) *N2>10% :α=(N2-N2г/Vс.г.)/(N2-N2г/Vс.г.-3.76(O2-0.5CО-0,5Н2-2СН4)) 44)определение коэффициента расхода окислителя при полном и неполном сгорании топлива Присжиганиии различных топлив на кислородном дутье, на воздухе и в азотокислородных смесях с любым соотношением кислорода и азота коэф. расхода окислителя αок: *полн: αок=(О2+nCO2)/nCO2 *непол:αок=(О2-0.5CО-0,5Н2-2СН4+ n(СО2+СО+СН4))/n(СО2+СО+СН4) где n-коэф,показывающий отношение теор-ки необх-го для горения О2 к объему получаемого СО2 45)энтальпия продуктов сгорания Jг=Jг0+ Jв0(α-1)+ Jз (газообр.прод.сгор.при α=1, избыточный воздух и зола) Iг°=(VRо2*Ссо2 +VN2 *СN2 +Vн2о*Сн2о)tг Iв°= Vв° *Св *tг Iз=Ар*αун*(С*tг)з/100 46)расчет состава продуктов горения с учетом их диссоциации CO2 → CO + 0,5O2 - 286 Мдж/кмоль; H2O пар → H2 + 0,5O2 - 243 Мдж/кмоль Разложение водяного пара возможно и с образованием гидроокиси по реакции: H2O ⇄ 0.5H2 + OH O2→O+O N2→N+N N2+02→2NO Ионные реакции разложения являются эндотермическими. При низких температурах и средних давлениях эти реакции мало влияют на температуру горения и состав продуктов реакции. При температурах выше 2000-2500˚С и невысоких давлениях влияние этих реакций существенно и его необходимо учитывать. При температурах горения не превышающих 2200˚С выход и состав продуктов рассчитывается с учетом диссоциации СО2 и Н2О по реакциям разложения.
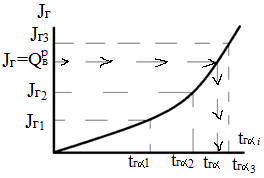
48,49.Расчет адиабатной температуры горения с учетом и без учета диссоциации.(графическим методом) Адибатная температура - температура, которую имели бы продукты сгорания при отсутствии теплопотерь в окружающую среду в процессе сгорания. Адиабатная температура максимальна для стехиометрической смеси. С увеличением коэффициента избытка воздуха на нагрев "избыточного" воздуха затрачивается лишняя теплота, поэтому температура продуктов сгорания уменьшается. Теоретические температуры горения. При нагреве воздуха, подаваемого в топку, или обогащении его кислородом температура горения увеличивается.
|
||||
|
Последнее изменение этой страницы: 2024-06-27; просмотров: 7; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.188.118.20 (0.007 с.) |

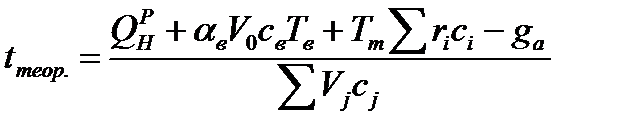 Где св, ci- теплоемкость окисления и компонентов топлива., Tв,Tm-начальная температура окисления и топлива, QнР-низшая теплота сгорания топлива, Vα-выход продуктов сгорания с учетом диссоциаций, Сj-теплоемкость продуктов сгорания с учетом диссоциации, gа- теплота, затрагивания на диссоциацию продуктов сгорания, [кДж/м3]
Где св, ci- теплоемкость окисления и компонентов топлива., Tв,Tm-начальная температура окисления и топлива, QнР-низшая теплота сгорания топлива, Vα-выход продуктов сгорания с учетом диссоциаций, Сj-теплоемкость продуктов сгорания с учетом диссоциации, gа- теплота, затрагивания на диссоциацию продуктов сгорания, [кДж/м3]