Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
СО жалын шебінің құрылымын көрсетіңіз және түсіндіріңіз.Содержание книги
Поиск на нашем сайте
2СО+О2=2СО2реакциясына түскен СО+О2 қоспасын қарастырайық.Температураның, СО,О2, СО2концентрацияларының жалын шебінде таралуы суретте көрсетілген:
Бастапқы қоспа реакция аумағындағы жылу ағыны есебінен қыздырылады.Қыздыру аумағындағы қоспаның құрамы бастапқы қоспамен салыстырғанда реагенттердің диффузиясы әсерінен және жану өнімімен (СО2)араластыру әсерінен өзгереді.Реакция аумағындағы СО мен О2концентрациясы бастапқы қоспа мәнінен көп кіші болады,температураның өсуі реакция жылдамдығының төмендеуін компенсациялайды,себебі негізгі химиялық өзгерістер тар облыста максималды температура-жалын температурасы маңайында жинақталған. Әсерлесетін заттар реакция аумағына диффузия арқылы үздіксіз беріліп отырады және диффузия әсерінен реакция аумағында таратылады. Жану толқынындағы реакцияның толық аяқталуы асимптоталы орындалады, диффузиялық ағындар 0-ге тең болатын облыстағы жану өнімдерінде термодинамикалық тепе-теңдік орнайды,ол қоспаның бастапқы құрамына және Тж-ға сәйкес келеді.Жалындағы реакция кинетикасының ерекшелігі-реакция ұсталу сатыларынан босатылған.Жалында жылудың және активті орталықтардың баяу жиналу жүйесі болмайды.Бір қабаттан екінші қабатқа активті орталықтар диффузиялана алады.Бір жанғыш қоспаның тұтану температурасы Тт 2000К деп қарастырайық,ал байқалатын реакция 1700-2000К аралықта жүреді.Бастапқы температураны көбейту арқылы Тт-ны 3000К-ке дейін арттырамыз;бұл кезде реакция 2300-3000К аралықта өтеді деп болжаймыз, ал Т<2300К ескермеуге болады.Бұл кезде тұтану температурасы Тт3000К болғанда бұрын жылдам реакция деп есептелетін 1700-2000К жүретін реакцияларды (Тт=2000К болғанда)неге ескермиміз деген сұрақ туады.Өте жоғары жану температурасы 1700-2000К-дегі реакция жылдамдығын төмендетпейді,керісінше,жану температурасы маңайында жоғары жылдамдықты тудырады,соған байланысты жалынның таралу жылдамдығы артады.Температура 1700-2000К-ге өзгеретін уақыт аралығы қысқарады.Баяу жанатын қоспаларда (Т=2000К)осы уақыт аралығында барлық жанғыш қоспа реакцияға түсіп кетеді.Жылдам жанатын қоспаларда 1700-2000К аралығында қоспаның болу уақыты қысқарады,сондықтан осы температурада қоспаның аз ғана бөлігі реакцияға қатысады,процестің жылдамдығы Т=2300-3000К температурада өтетін реакция жылдамдығына сәйкес келеді. 10. Жанудың ертедегі теорияларына тоқталыңыз. Б.Льюис және А.Эльбе теорияларын тұжырымдаңыз Жану – бұл 1 миллион жылдан астам уақыттан бері адамзат пайдаланып келе жатқан ең көне технология. Қазіргі уақытта энергияның 90% жану процесінде өндіріледі. Жану – адамзаттың негізгі энергия көзі. Ядролық энергияның пайда болуымен басқа энергия көздерінің рөлі біршама азайды. Оттың табиғаты туралы ойлар тас ғасырының аңыздары сияқты көнеден белгілі. Олар көптеген діндердің дамуында, сондай-ақ химияның ғылым ретінде пайда болуында маңызды рөл атқарды. Жану процесі күрделі. Тіпті қарапайым жалынның өзін жылу және масса алмасу құбылыстарымен бір мезгілде бірге өтетін реакциялардың комплексі ретінде қарастыруға болады 1934 жылы Б.Льюис пен А.Эльбе жалынның таралуын озонның жарылып ыдырау реакциясына қолданған. 1. О3 « О2 + О 2. О + О3 « 2О2 + О2 3. (О2* + О3 « 2О2 + О) Авторлар келесідей болжамдар жасаған: 1. Теңдеу бойынша тепе-теңдік реакция зонасының бойында байқалады және жалын үдеп 2) процеспен анықталады. Сондықтан үздіксіздік теңдеуі былай жазылады:
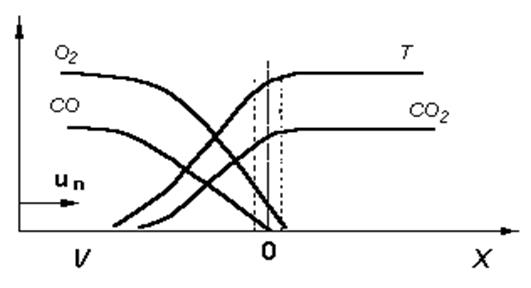
2. b реакцияның аяқталу дәрежесі х координатының сызықты функциясы деген постулатқа бұл тұжырым эквивалент болады: U/T0(1+0,5b+n) = const. U – фронтқа қатысты газдың қозғалыс жылдамдығы Тэнфорд пен Пиз жану зонасы бойынша химиялық реакцияның жүруі Льюис – Элбе сияқты жылу бөліну бойынша жүретін реакцияның аяқталуымен анықталады. Ван-Тиггелен ұсынған жалынның таралуының теориясы Н.Н. Семеновтың тізбекті реакциялардың тармақталу теориясына сәйкес Ван-Тиггелен жалындағы тізбекті реакциялардың жылдамдығы тармақталу мен тізбектің үзілуі ықтималдығының арасындағы қатынаспен анықталады деп қабылдаған. Ван-Тиггелен бойынша, нормаль жану жылдамдығы келесі теңдеумен анықталады: U0 = 4T0/p От негізгі зат деп ең алғаш жалынға байланысты ғылыми пікірді грек философы Гераклит тұжырымдаған. Жануға байланысты алғашқы жұмысты шырақ жалынының құрылысын бақылаған Фрэнсис Бэкон жүргізді. Эмпедоклдың айтуы бойынша, от – ауа, су мен жерді қоса алғанда барлық ғаламның төрт элементінің біреуі. Жану облысында көптеген белгілі химиктер тәжірибе жүргізді. (Вольт, Бертолле, Берцелиус, Дальтон). Одан әрі қарай Томсон, Румфорд және Дэви Король қоғамы үшін таулардың жарылыс мәселелерімен айналысып, жүйелі зерттеулер жасап, нәтижесінде қауіпсіз шам (Дэви шамы) ойлап тапқан. Фарадейдің жану теориялары туралы зерттеулерінің нәтижелері оның көпшілікке белгілі «Шырақтың химиялық тарихы» еңбегінде көрсетілді. Бунзен ашқан жанарғы қазіргі кезге дейін әрбір химиялық зетханаларда кездеседі, сонымен бірге ол ең алғаш жалынның температурасы мен жылдамдығын зерттеген, ал оның жасаған калориметрі қазір жалын энтальпиясын өлшеуде жиі қолданылады. Жану толқынының таралуының физикалық-химиялық теориясы ХІХ ғасырдың 30-40 жылдарында Б.Льюис және А. Эльбе, Я.Б. Зельдович және Д.А. Франк-Каменецкий, Н.Н. Семенов, Гиршфель және т.б. Зерттеушілер еңбектерінің нәтижесінде жасалды. Бұдан бұрынғы теорияларда жану процесін сипаттау үшін өздігінен тұтанудың нақты белгілі бір температурасы болады деген негізделмеген жорамалдар қолданылып жүрді, ол бойынша бұл температурадан төменгі температурада реакция жүрмейді делінген. Бұл өз кезегінде химиялық кинетиканың негізгі түсініктеріне қайшы келді және жану теориясының ішкі құрылымына өзгерістер әкелді. Бұлардың ішінен Таффанелл жұмысы ғана ерекшеленеді, онда реакция жылдамдығының температураға үздіксіз тәуелділігі есепке алынып, жану теориясына сәйкес бірқатар қорытындылар жасалды. Алға жасалған қадамдардың бірі жалынның таралу теориясына химиялық кинетиканың мәндерін енгізу болып табылады.Ол реакцияның орташа жылдамдығын ауыспалы концентрация және температура функцияларымен алмастыруға негізделген.Бұл бағыттағы бірінші зерттеуді 1934 жылы Б.Льюис пен А.Эльбе жалынның таралуын озонның жарылып ыдырау реакциясына қолданып жуық шешімін тапқан.
|
||||
|
Последнее изменение этой страницы: 2024-06-17; просмотров: 10; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.16.82.208 (0.009 с.) |

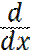 (D
(D 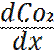 ) -
) -