
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
f-g= jдеп белгілесек, онда:dn/dt = W0 + jnСодержание книги
Поиск на нашем сайте
f-g= jдеп белгілесек, онда:dn/dt = W0 + jn W0-тізбектің пайда болу жылдамдығы f-тізбектің тармақталуының жылдамдық константасы g-тізбектің үзілуінің жылдамдық константасы. Сыртқы шарттардың (температура, қысым) өзгеруі әсерінен екі шамада fжәне g өзгереді, g ға қарағанда көп жағдайда f температураға тәуелді, себебі активті орталықтардың жойылуы үшін Еакт қажеті жоқ.Сондықтан f-g = j айырымы температура өскен кезде таңбасын ауысытырады; төмен температураларда таңбасы теріс болады, жоғары температураларда – оң таңбалы болады.( 2-сурет). j>0 болғанда активті орталықтардың түзілу жылдамдығы мен концентрациясы үздіксіз өседі.Сонымен, j мәні 0-ге айналатын температура Тш болып табылады, одан төмен температурада жарылыс болуы мүмкін емес.осы сапалы түсіндірмелер белгілі бастапқы қысымда жіне бастапқы температура j=0 сәйкес келетін шектік мәннен өткен кезде жарылғыш қоспаның тұтану облысының бар екенін көрсетеді.Әртүрлі j мәніндегі кинетикалық қисықтардың қасиеттерін тереңірек өарастырсақ.Ол үшін теңдеудің t=0 болғанда n=0 шартын қанағаттандыратын интегралын табамыз: n = W0/j (ejt - 1); Реакция жылдамдығы, яғни соңғы өнімнің түзілу жылдамдығы келесі теңдеумен өрнектеледі: W=νfn=(ejt - 1); Мұндағы ν-реакцияға активті орталық қатысқанда соңғы өнімнің неше молекуласы түзілетінін көрсететін бірінші реттік бүтін сан.
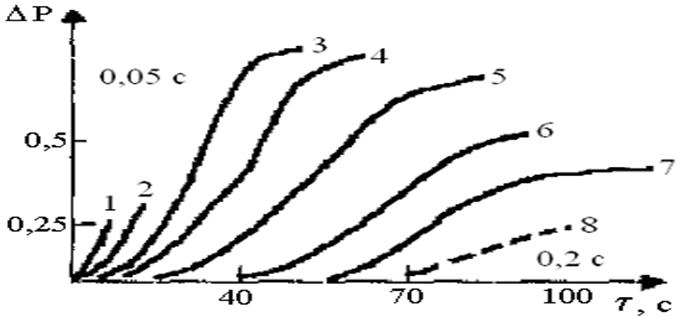
1-сурет.Стехиометриялық 2Н2 + О2 қоспасының кинетикалық қисықтары. Т0 = 485 °С. Бастапқы қысым Р0: 1-қисық – 8,2 мм сын.бағ., индукция периоды 0,2 с; 8-қисық – 5,8 мм сын. бағ., индукция периоды 0,05 с.
7. Жанудың режимдерін сипаттаңыз. Алдын ала дайындалған қоспалардың жануын түсіндіріңіз. Жанудың диффузиялық және кинетикалық режимдері бар. Отынның тотықтырғышқа жұмсалуы нәтижесінде түзілетін жалын-диффузиялық жалын деп аталады (диффузиялық жану, диффузиялық жалын). Отын мен тотықтырғыштың алдын-ала араласқан қоспаларының қоршаған ортаға жұмсалуы нәтижесінде түзілетін жалын-кинетикалық жалын деп аталады (кинетикалық жану, кинетикалық жалын). Бірінші тип үшін диффузия құбылысы, араласу басты рөлге ие (молекулярлы, турбулентті). Екінші тип үшін химиялық реакцияның кинетикасы басты рөлге ие (жалын таралуының жылулық және тізбекті механизмі).Жану-берілген режимде өздігінен жарық және жылу бөле жүретін, бір химиялық қосылыстың басқа химиялық қосылыстарға айналу процесі. tайналу=tараласт+tқыздыру+tх.р, мұндағы tараласт–отынға тотықтырғышты қосу уақыты (араластыру). tқыздыру–жану компоненттерін тұтану температурасына дейін қыздыру уақыты. tх.р–жанудың химиялық реакциясының жүру уақыты. tараласт tараласт=0 tараласт= tх.р жанудың араласқан диффузия-кинетикалық режимі. Химиялық реакцияның жылдамдығын- осы химиялық реакцияның кинетикасы анықтайтынындай, жанудың кинетикалық режимінде жану қарқындылығын (tайналу ) қоспаның температурасы мен қысымы, жанатын және тотықтырғыш құрамға ие жанғыш заттың концентрациясын анықтайды.Жанудың диффузиялық режимі (tайналу ) айналудың геометриялық және гидродинамикалық облысымен, яғни жанатын және тотықтырғыш табиғатымен, араластырудың қарқындылығымен анықталады. Алдын ала дайындалған қоспаны жағу үшін арналған жанарғылар.Көптеген жалындар көлденең қимасы дөңгелек құбыр болып келетін жанарғыларда тұрақтанады. Мұндай жанарғылардың жұмыс істеу принциптері туралы реагенттердің суық қоспасының бағытындакез-келген нүктеде оның бетіне Su жану жылдамдығымен перпендикуляр таралатын үзіліссіз жазық жалын фронтын түзу қабілеті бойынша айтуға болады. Аңын бағытына перпендикуляр болып келетін жазық жалын, қандай да бір қатты денеге жылу беру салдарынан өзгермейтін ағын жылдамдығы жану жылдамдығымен компенсацияланатын Эджертон мен Паулинг және Бидлер мен Хелшердің жанарғыларына ұқсас жанарғы сипатталған. Бұл жанарғының принципиалдысызбанұсқасы 3-суретте келтірілген. Ағын жылдамдығының бірқалыпты таралуы ретсіз таралған аздаған бөгеттердің көмегімен жүзеге асады. Бұл жанарғылардың жұмыс істеу барысында ағынның төменгі жылдамдықтарында тордың артындағы ағыншалар қоспа жалын фронтына келмей тұрып жоғалып кетеді. Мұндай жанарғылар дұрыс жұмыс жасауы үшін температура да аздап төмендеуі тиіс және де ағынның ауытқуы болмау керек. 8.Температура мен концентрация өрістерінің ұқсастығын талдаңыз.Тәжірибе жүзінде байқалатын жалынның таралу жылдамдығының U0 жану температурасына (Тж) тәуелділігі жану зонасында жүретін химиялық реакцияның жылдамдығының U0 шамасын анықтайтын негізгі фактор екенін куәландырады. Сондықтан жалынның таралу құбылысын зерттеу, қарапайым жанғыш жалындар жанатын жоғарғы температурада жүретін химиялық реакцияларды зерттеудің принципиалды мүмкіндігін береді(1500-3000 K). Мұндай зерттеулердің негізінде U0 шамасының жану зонасындағы химиялық реакция жылдамдығына функционалды тәуелділігі жатады. Осы тәуелділікті жалында жүретін процестер мен алып жүру процестерін жылу өткізгіштік пен диффузия бірге қарастыру арқылы келтіруге болады. Бастапқы болып табылатындар:1Жылу өткізгіштік теңдеуі, бірөлшемді есептер үшін стационарлық жалындарда (сәулелену арқылы жылу беру және реактор қабырғасына жылу беру жоқ деп алынғанда) былай жазылады:
Мұндағы
Одан басқа жалындағы газдың орташа молекулалық салмағы (М)М0-ден аз ерекшеленеді деп алуға болады, яи
Осы зат есебінде реакциядағы бір өнім немесе бастапқы заттың біреуі болса, онда сәйкес
|
||||
|
Последнее изменение этой страницы: 2024-06-17; просмотров: 9; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.138.178.162 (0.011 с.) |

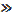 tх.р жанудың диффузиялық режимі (tайналу=tараласт).
tх.р жанудың диффузиялық режимі (tайналу=tараласт). tх.р жанудың кинетикалық режимі (tайналу= tх.р).
tх.р жанудың кинетикалық режимі (tайналу= tх.р).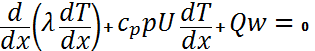 (26)немесе
(26)немесе 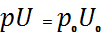 деп алсақ,
деп алсақ,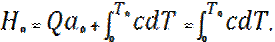 (27)Мұндағы 𝝀- жылу өткізгіштік коэффициенті,
(27)Мұндағы 𝝀- жылу өткізгіштік коэффициенті, 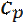 - меншікті жылу сыйымдылық, p- жалын зонасындағы газдың тығыздығы,
- меншікті жылу сыйымдылық, p- жалын зонасындағы газдың тығыздығы, 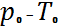 болған кезде, U0 – жалынның нормаль жылдамдығы (жанбаған газға қатысты жалынның қозғалу жылдамдығы),
болған кезде, U0 – жалынның нормаль жылдамдығы (жанбаған газға қатысты жалынның қозғалу жылдамдығы), 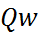 - реакция нәтижесінде жылу бөліну жылдамдығы, Q – реакцияның жылулық эффектісі;2. диффузия теңдеуі, термодиффузияны , яғни диффузияны ескермеген кездегі температуралық градиент қатысқан кезде мына түрде жазылады:
- реакция нәтижесінде жылу бөліну жылдамдығы, Q – реакцияның жылулық эффектісі;2. диффузия теңдеуі, термодиффузияны , яғни диффузияны ескермеген кездегі температуралық градиент қатысқан кезде мына түрде жазылады: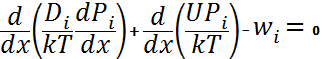 (28)
(28) 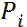 - i-ші заттың парциалды қысымы,
- i-ші заттың парциалды қысымы, 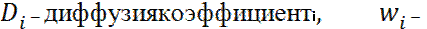 i- заттың өзгеруінің химиялық реакциясының жылдамдығы;3. реакцияның кинетикалық теңдеуі концентрация және температураның функция ретінде әртүрлі заттардың химиялық өзгерісінің жылдамдығымен бейнеленеді және реакцияның химиялық механизмімен анықталады. Тұрақты жалпы қысымда
i- заттың өзгеруінің химиялық реакциясының жылдамдығы;3. реакцияның кинетикалық теңдеуі концентрация және температураның функция ретінде әртүрлі заттардың химиялық өзгерісінің жылдамдығымен бейнеленеді және реакцияның химиялық механизмімен анықталады. Тұрақты жалпы қысымда 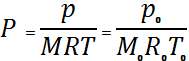 (29)
(29)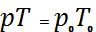 және
және 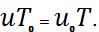 Кейбір жағдайда концентрация өлшемі ретінде берілген заттың бірлік көлемдегі граммен алынған шамасын алады, яғни зат тығыздығы: p=mn=cM (30)мұндағы m- берілген заттың молекулалық массасы; M=m NA - заттың молекулалық салмағы.Немесе берілген заттың парциалды қысымы былай өрнектеледі:
Кейбір жағдайда концентрация өлшемі ретінде берілген заттың бірлік көлемдегі граммен алынған шамасын алады, яғни зат тығыздығы: p=mn=cM (30)мұндағы m- берілген заттың молекулалық массасы; M=m NA - заттың молекулалық салмағы.Немесе берілген заттың парциалды қысымы былай өрнектеледі: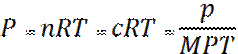 (31) Концентрация берілген заттың бірлік көлемдегі моль санымен өлшенеді, яғни c=
(31) Концентрация берілген заттың бірлік көлемдегі моль санымен өлшенеді, яғни c= 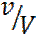 ,
, 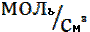 өлшенеді немесе бірлік көлемдегі молекулалар санымен өлшенеді :n=cNA ;
өлшенеді немесе бірлік көлемдегі молекулалар санымен өлшенеді :n=cNA ; 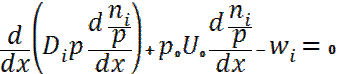 (33)
(33)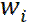 шамасы брутто – реакцияны береді
шамасы брутто – реакцияны береді 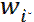 Егер одан басқа келесі шарт орындалса:(-dnбаст/dt)-dnөнім /dt = w және dnаралық/dt=0
Егер одан басқа келесі шарт орындалса:(-dnбаст/dt)-dnөнім /dt = w және dnаралық/dt=0


