

Мы поможем в написании ваших работ!
ЗНАЕТЕ ЛИ ВЫ?
|
Тема 6. 9. Регуляция гликолиза и глюконеогенеза
Содержание книги
- III. Исключение праймеров. Завершение формирования отстающей цепи ДНК
- Тема 3. 4. Биосинтез рнк (транскрипция). Посттранскрипционные модификации рнк
- Тема 3. 5. Трансляция как механизм перевода генетической информации в фенотипические
- Тема 3. 6. Ингибиторы матричных биосинтезов: лекарственные препараты, яды и бактериальные токсины
- Тема 3. 7. Механизмы адаптивной регуляции активности генов у прокариотов и эукариотов
- Тема 3. 8. Механизмы, обеспечивающие разнообразие белков у эукариотов
- Тема 3. 9. Механизмы генетической изменчивости: эволюционная изменчивость, полиморфизм белков. Наследственные болезни
- Тема 3. 10. Использование рекомбинантных днк
- Использование техники рекомбинанатных днк для диагностики и лечения заболеваний
- Инактивация аденилатциклазы и протеинкиназы А
- Последовательность событий передачи сигнала первичных мессенджеров с помощью инозитолфосфатной системы
- Первый этап тканевого дыхания - дегидрирование различных субстратов, образующихся в реакциях катаболизма.
- Тема 5. 4. Сопряжение тканевого дыхания и синтеза атф
- В реакциях цпэ часть энергии не превращается в энергию макроэргических связей атф, А рассеивается в виде теплоты.
- Окислительное декарбоксилирование пирувата
- Кроме того, адф аллостерически активирует некоторые ферменты опк
- Тема 5. 12. Гипоэнергетические состояния
- Желудочный сок не содержит ферментов, расщепляющих пищевые углеводы. Амилаза слюны инактивируется в желудке, так как оптимальное
- Тема 6. 3. Синтез гликогена (гликогеногенез), мобилизация гликогена (гликогенолиз). Регуляция процессов
- Активация гликогенфосфорилазы адреналином посредством аденилатциклазной системы
- В аэробном и анаэробном гликолизе можно выделить два этапа.
- Тема 6. 6. Биологическое значение катаболизма глюкозы. Регуляция процесса
- Анаболическое значение катаболизма глюкозы.
- Тема 6. 7. Пентозофосфатный путь превращения
- А - окислительный этап; б - неокслительный этап в обратном направлении
- Тема 6. 9. Регуляция гликолиза и глюконеогенеза
- Регуляция активности пируваткиназы в печени осуществляется путем фосфорилирования (дефосфорилирования) в зависимости от ритма питания
- Структурная организация межклеточного матрикса (суставной хрящ, базальные мембраны, субэпителиальные слои)
- Гликозилирование лизина под действием гликозилтрансфераз прекращается по мере формирования трехспиральной структуры.
- Патологий, связанных с уменьшением эластичности сосудов. При недостаточной активности металлопротеиназ развивается фиброз тканей и неадекватный иммунный ответ.
- Хондроитинсульфат; 2 - кератансульфат; 3 - коровый белок; гк - гиалуроновая кислота
- Тема 7. 5. Структурная организация межклеточного матрикса (суставной хрящ, базальные мембраны, субэпителиальные слои)
- Регуляция процесса. Амф, гмф, имф, ди- и трифосфаты адениловых и гуаниловых нуклеотидов ингибируют ключевые реакции своего синтезааллостерически по механизму отрицательной обратной связи.
- Частым нарушением катаболизма пуринов является гиперурикемия, которая возникает, когда в плазме крови Концентрация мочевой кислоты превышает норму.
- Синтез цтф из утф осуществляет цтф-синтетаза, используя амидную группу глн и энергию атф для аминирования пиримидинового кольца.
- Тема 10. 3. Биосинтез дезоксирибонуклеотидов.
- Тема 10. 4. Механизмы действия противовирусных и противоопухолевых препаратов на ферменты синтеза рибо- и дезоксирибонуклеотидов
- И рецепторов. Особенно много сфинголипидов в нервной ткани, где они формируют миелиновые оболочки нейронов.
- Тема 8. 3. Хиломикроны - транспортная форма экзогенных жиров
- Модульная единица 2 биосинтез высших жирных кислот и жиров
- Реакции восстановления обеспечивают синтез насыщенного алифатического радикала жирных кислот
- Запасание жиров в жировой ткани - так называемое депонирование жиров - происходит в абсорбтивный период, когда увеличивается соотношение инсулин - глюкагон.
- Первичное ожирение развивается в результате алиментарного дисбаланса - избыточной калорийности питания по сравнению с расходами энергии.
- Модульная единица 3 жиры, жирные кислоты и кетоновые тела как источники энергии. Эйкозаноиды, Строение, синтез и биологические функции
- Скелетные мышцы и почки используют кетоновые тела даже при их низкой концентрации в крови.
- Выведение кетоновых тел, в том числе и ацетона, с мочой (кетонурия), потом выдыхаемым воздухом является способом выведения избытка кетоновых тел из организма и уменьшения таким образом ацидоза.
- Ацетильный остаток переносится с молекулы аспирина на oh-группу фермента и необратимо ингибирует его
- Модульная единица 4 обмен холестерола, его регуляция и транспорт кровью. Дислипопротеинемии. Биосинтез и функции желчных кислот. Желчнокаменная болезнь
- В поддержании гомеостаза холестерола в организме. Биохимия желчнокаменной болезни
- Тема 8. 14. Роль липопротеинов в транспорте
В ПЕЧЕНИ
1. Переключение метаболизма печени с гликолиза на глюконеогенез и наоборот происходит при помощи:
- аллостерических механизмов регуляции активности ключевых ферментов;
- ковалентной модификации ферментов путем фосфорилирования (дефосфорилирования) с участием инсулина и глюкагона;
- индукции (репрессии) синтеза ключевых ферментов, катализирующих реакции субстратных циклов.
Регуляция гликолиза и глюконеогенеза в печени направлена на необратимые стадии гликолиза и глюконеогенеза, которые формируют три субстратных цикла (на рис. 6.20 обозначены I, II, III). Название «субстратный цикл» означает объединение реакций синтеза и распада субстрата.
2. Направление реакций первого субстратного цикла регулируется главным образом концентрацией глюкозы. При пищеварении (абсорбтивный период) концентрация глюкозы в крови повышается (до 120-140 мг/дл, или 7-8 ммоль/л). Активность глюкокиназы в этих условиях максимальна. Вследствие этого ускоряется реакция Глюкоза - Глюкозо-6-фосфат. Поскольку глюкокиназа печени не ингибируется глюкозо-6-фосфатом (в отличие от гексокиназы мышц), то основная часть глюкозо-6-фосфата направляется в гликолиз и на синтез гликогена.
3. Направление реакций второго субстратного цикла зависит от активности фосфофруктокиназы и фосфатазы фруктозо-1,6-бисфосфата. В этом цикле действует фруктозо-2,6-бисфосфат, который одновременно выполняет функцию аллостерического активатора фосфофруктокиназы (регуляторный фермент гликолиза) и аллостерического ингибитора фосфатазы фруктозо- 1,6-бисфосфата (регуляторный фермент глюконеогенеза).
Фруктозо-2,6-бисфосфат образуется в абсорбтивный период путем фосфорилирования фруктозо-6-фосфата при участии бифункционального фермента (БИФ), который в дефосфорилированной форме (БИФ-ОН) проявляет киназную активность (рис. 6.24). Дефосфорилирование БИФ происходит с помощью фермента фосфопротеинфосфатазы, который активируется при высоком инсулин-глюкагоновом индексе за счет инсулинового рецептора.
При низком инсулин-глюкагоновом индексе, характерном для периода голодания, происходит фосфорилирование БИФ (БИФ-ОРО3Н2) с помощью протеинкиназы А, которая активируется вследствие активации аденилатциклазной системы в результате взаимодействия гормона глюкагона с рецепторами. При этом БИФ проявляет фосфатазную активность. В результате
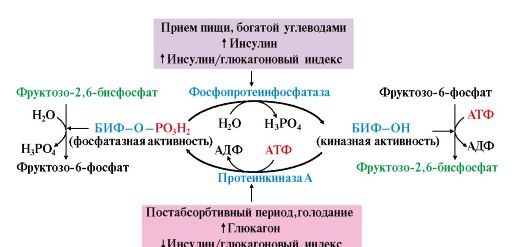 Рис. 6.24. Реакции, катализируемые бифункциональным ферментом (БИФ) в печени. Рис. 6.24. Реакции, катализируемые бифункциональным ферментом (БИФ) в печени.
БИФ катализирует реакции обратимого превращения фруктозо-6-фосфата в фруктозо-2,6-бисфосфат. БИФ может находиться в двух формах: дефосфорилированной (БИФ-ОН) и фосфорилированной (БИФ-ОРО3Н2). БИФ-ОН обладает киназной активностью и способствует образованию фруктозо-2,6-бисфосфата. БИФ-ОРО3Н2 обладает фосфатазной активностью и способствует уменьшению концентрации фруктозо-2,6-бисфосфата и образованию фруктозо-6-фосфата. Фосфорилирование и дефосфорилирование БИФ связано с ритмом питания и регулируется гормонами. Инсулин (абсорбтивный период) активирует фермент фосфопротеинфосфатазу, что приводит к появлению формы БИФ-ОН, а глюкагон (постабсорбтивный период) активирует аденилатциклазную систему, что вызывает активацию протеинкиназы А и появление формы БИФ-ОРО3Н2
Уменьшается количество фруктозо-2,6-бисфосфата, что приводит к замедлению гликолиза и переключению метаболизма на глюконеогенез. Наличие двух активностей (киназной и фосфатазной) у БИФ определило название фермента - «бифункциональный».
БИФ присутствует только в гепатоцитах. Киназную и фосфатазную реакции катализируют разные активные центры БИФ, которые функционируют по очереди в зависимости от состояния фермента фосфорилированного или дефосфорилированного. Превращение фруктозо-2,6-бисфосфата в фрукто- зо-6-фосфат не является обратимым процессом. Образование фруктозо-2,6- бисфосфата требует затрат АТФ, а при образовании фруктозо-6-фосфата из фруктозо-2,6-бисфосфата высвобождается неорганический фосфат.
4. В регуляции третьего субстратного цикла основная роль принадлежит пируваткиназе, фосфорилированная форма которой неактивна, а дефосфорилированная активна (рис. 6.25). Дефосфорилирование пируваткиназы происходит в период пищеварения, когда инсулин активирует фосфопротеинфосфатазу, которая дефосфорилирует пируваткиназу, переводя ее в активное состояние. Следовательно, реакция превращенияфосфоенолпируват в пируват ускоряется при пищеварении (абсорбтивный период). В постабсорбтивном состоянии пируваткиназа при действии глюкагона на печень переходит в фосфорилированное неактивное состояние.
Реакция глюконеогенеза превращения пирувата - оксалоацетат катализитуется биотин-зависимым ферментом - пируваткарбоксилазой с участием АТФ в качестве источника энергии. Регуляция этой реакции осуществляется с помощью аллостерической активации ацетил-КоА.Биологическое значение этого эффекта объясняется тем, что при голодании организм начинает использовать жирные кислоты как источник энергии.
 Рис. 6.25. Регуляция пируваткиназы в печени. Рис. 6.25. Регуляция пируваткиназы в печени.
|